
【题目】下列关于硅单质及其化合物的说法正确的是( )
①硅是构成一些岩石和矿物的基本元素
②水泥、玻璃、水晶饰物都是硅酸盐制品
③高纯度的硅单质广泛用于制作光导纤维
④陶瓷是人类应用很早的硅酸盐材料
A.①②
B.②③
C.①④
D.③④
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】砷为VA族元素,金属冶炼过程产生的含砷有毒废弃物需处理与检测.
(1)冶炼废水中砷元素主要以亚砷酸(H3AsO3)形式存在,可用化学沉降法处理酸性高浓度含砷废水,其工艺流程如下:
已知:I.As2 S3与过量的S2一存在以下反应:As2S3+3S2﹣2AsS ![]()
II.亚砷酸盐的溶解性大于相应砷酸盐
①亚砷酸中砷元素的化合价为 .
②砷酸的电离方程式为 .
③“一级沉砷”中FeSO4的作用是 .
④“二级沉砷”中H2 O2与含砷物质反应的化学方程式为 .
⑤沉淀X为(填化学式).
(2)冶炼废渣中的砷元素主要以As203的形式存在,可用古氏试砷法半定量检测(As的最低检出限为3.0x 10 ﹣6g).
步骤1:取10g废渣样品,粉碎后与锌粉混合,加人H2 SO4共热,生成AsH3气体.
步骤2:将AsH3气体通人AgNO3溶液中,生成银镜和As2 O3 .
步骤3:取1g废渣样品,重复上述实验,未见银镜生成.
①AsH3的电子式为 .
②步骤2的离子方程式为 .
③固体废弃物的排放标准中,砷元素不得高于4.0×10一5gkg一1 , 请通过计算说明该废渣是否符合排放标准 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学--选修5:有机化学基础]秸秆(含多糖物质)的综合应用具有重要的意义.下面是以秸秆为原料合成聚酯类高分子化合物的路线:
回答下列问题:
(1)下列关于糖类的说法正确的是 . (填标号)
a.糖类都有甜味,具有CnH2mOm的通式
b.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
c.用银镜反应不能判断淀粉水解是否完全
d.淀粉和纤维素都属于多糖类天然高分子化合物
(2)B生成C的反应类型为 .
(3)D中官能团名称为 , D生成E的反应类型为 .
(4)F的化学名称是 , 由F生成G的化学方程式为 .
(5)具有一种官能团的二取代芳香化合物W是E的同分异构体,0.5mol W与足量碳酸氢钠溶液反应生成44gCO2 , W共有种(不含立体结构),其中核磁共振氢谱为三组峰的结构简式为 .
(6)参照上述合成路线,以(反,反)﹣2,4﹣己二烯和C2H4为原料(无机试剂任选),设计制备对二苯二甲酸的合成路线 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度和体积不变的密闭容器中,一定质量的C与2mol CO2发生反应:C+CO2=2CO,测得反应后气体压强是反应前气体压强的 ![]() 倍,下列说法中正确的是( )
倍,下列说法中正确的是( )
A.反应后容器内的气体只有CO
B.反应后生成的CO与反应前的CO2的物质的量之比为1:1
C.反应后生成的CO与反应前的CO2的分子数目之比为3:2
D.反应后容器内的气体与反应前的CO2所含的氧原子数目之比为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)某混合物浆液含有Al(OH)3、MnO2和少量Na2CrO4 . 考虑到胶体的吸附作用使Na2CrO4不易完全被水浸出,某研究小组利用设计的电解分离装置(见图),使浆液分离成固体混合物和含铬元素溶液,并回收利用.回答Ⅰ和Ⅱ中的问题.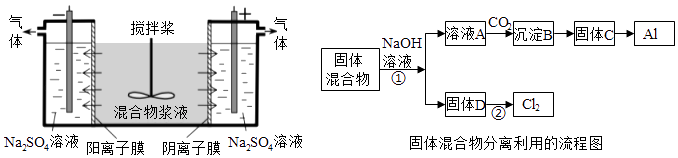
Ⅰ.固体混合物的分离和利用(流程图中的部分分离操作和反应条件未标明)
(1)反应①所加试剂NaOH的电子式为 . B→C的反应条件为 , C→Al的制备方法称为 .
(2)该小组探究反应②发生的条件.D与浓盐酸混合,不加热,无变化;加热有Cl2生成,当反应停止后,固体有剩余,此时滴加硫酸,又产生Cl2 . 由此判断影响该反应有效进行的因素有(填序号) .
a.温度 b.Cl﹣的浓度 c.溶液的酸度
(3)0.1mol Cl2与焦炭、TiO2完全反应,生成一种还原性气体和一种易水解成TiO2xH2O的液态化合物,放热4.28kJ,该反应的热化学方程式为 .
Ⅱ含铬元素溶液的分离和利用
(4)用惰性电极电解时,CrO42﹣能从浆液中分离出来的原因是 , 分离后含铬元素的粒子是;阴极室生成的物质为(写化学式).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1﹣18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题: 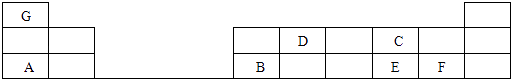
(1)D的元素名称为;
(2)G和F形成化合物的电子式为;
(3)C和E分别形成的气态氢化物中最稳定的是(填写氢化物的化学式)
(4)A最高价氧化物的水化物和B的最高价氧化物的水化物反应的化学方程为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(15分)重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeOCr2O3 , 还含有硅、铝等杂质.制备流程如图所示: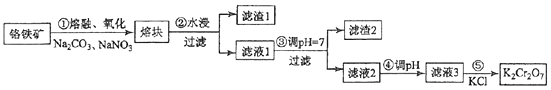
回答下列问题:
(1)步骤①的主要反应为:FeOCr2O3+Na2CO3+NaNO3 ![]() Na2CrO4+Fe2O3+CO2+NaNO2上述反应配平后FeOCr2O3与NaNO3的系数比为 . 该步骤不能使用陶瓷容器,原因是 .
Na2CrO4+Fe2O3+CO2+NaNO2上述反应配平后FeOCr2O3与NaNO3的系数比为 . 该步骤不能使用陶瓷容器,原因是 .
(2)滤渣1中含量最多的金属元素是 , 滤渣2的主要成分是及含硅杂质.
(3)步骤④调滤液2的pH使之变(填“大”或“小”),原因是(用离子方程式表示).
(4)有关物质的溶解度如图所示.
向“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到K2Cr2O7固体.冷却到(填标号)得到的K2Cr2O7固体产品最多.
a.80℃ b.60℃ c.40℃ d.10℃
步骤⑤的反应类型是 .
(5)某工厂用m1 kg 铬铁矿粉(含Cr2O3 40%)制备K2Cr2O7 , 最终得到产品 m2 kg,产率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铁的氧化物(FexO)1.52g溶于足量盐酸中,向所得溶液中通入标准状况下112mL Cl2 , 恰好将Fe2+完全氧化.下列说法正确的是( )
A.FexO溶于足量盐酸后只生成了FeCl3和H2O
B.标准状况下112 mL Cl2的物质的量是5 mol
C.x=0.8
D.通入Cl2后,发生反应的离子方程式:Fe2++Cl2=Fe3++2Cl﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com