
| A.电解水制氢:2H2O电解2H2↑+O2↑ |
| B.高温使水分解制氢:2H2O高温2H2↑+O2↑ |
C.太阳光催化分解水制氢:2H2O 2H2↑+O2↑ 2H2↑+O2↑ |
| D.天然气制氢:CH4+H2O高温CO+3H2 |
科目:高中化学 来源:不详 题型:单选题
 O2(g)===4CO2(g)+5H2O(l) ΔH=-2 878 kJ·mol-1
O2(g)===4CO2(g)+5H2O(l) ΔH=-2 878 kJ·mol-1 O2(g)===4CO2(g)+5H2O(g) ΔH=-2 658 kJ·mol-1
O2(g)===4CO2(g)+5H2O(g) ΔH=-2 658 kJ·mol-1 O2(g)===4CO(g)+5H2O(l) ΔH=-1 746 kJ·mol-1
O2(g)===4CO(g)+5H2O(l) ΔH=-1 746 kJ·mol-1 O2(g)===4CO(g)+5H2O(g) ΔH=-1 526 kJ·mol-1
O2(g)===4CO(g)+5H2O(g) ΔH=-1 526 kJ·mol-1| A.ΔH=-2 878 kJ·mol-1 | B.ΔH=-2 658 kJ·mol-1 |
| C.ΔH=-1 746 kJ·mol-1 | D.ΔH=-1 526 kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

A.图1表示化学反应2S02(g)+O2(g)  2S03(g)的能量变化,该反应的ΔH=A一BkJ/mol 2S03(g)的能量变化,该反应的ΔH=A一BkJ/mol |
B.图2表示其他条件不变时,反应2A(g)+B(g)  c(g) +D(g)在不同压强下随时间的变化 c(g) +D(g)在不同压强下随时间的变化 |
| C.图3表示体积和浓度均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 |
| D.图4表示100 ml O.1 mol·L—Na2C03和NaHC03两种溶液中,分别逐滴滴加O.1 mol·L-HCl,产生CO2的体积随盐酸体积的变化,则b表示NaHCO3溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 HCOOCH3(g)+2H2(g) △H>0
HCOOCH3(g)+2H2(g) △H>0 CH3OH(g) +CO(g) △H>0
CH3OH(g) +CO(g) △H>0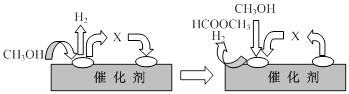


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题





| A.图①表示石墨转变为金刚石是吸热反应 |
| B.图②所示实验可比较非金属性强弱:氯﹥碳﹥硅 |
| C.图③吸收NH3并防倒吸 |
| D.图④两装置中金属电极a、b都有气体产生,可判断金属活动性:a﹤b |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.反应过程a有催化剂参与 |
| B.该反应为放热反应,热效应等于ΔH |
| C.改变催化剂,可改变该反应的活化能 |
| D.有催化剂条件下,反应的活化能等于E1+E2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO2(g)+H2(g),等物质的量的CO(g)和H2O(g)加入密闭容器中反应,平衡时测得结果如下表。
CO2(g)+H2(g),等物质的量的CO(g)和H2O(g)加入密闭容器中反应,平衡时测得结果如下表。| 温度 | 260℃ | 280℃ | 295℃ | 310℃ |
| CO转化率 | 89% | 80% | 75% | 60% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com