
| (n-1.5)mol |
| 2L |
| ( n-0.5)mol |
| 2L |
| (n-1.5)mol |
| 2L |
| ( n-0.5)mol |
| 2L |
| ||
| 5min |
| ||
| 5min |
| 3mol |
| 2L |


科目:高中化学 来源: 题型:
| A、酒精灯着火时可用水扑灭 |
| B、为防止试管破裂,加热固体时试管口一般要略高于试管底 |
| C、不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 |
| D、配制硫酸溶液时,可先在量筒中加入一定体积的水,边搅拌条件下边加入浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、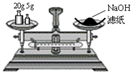 称量氢氧化钠固体 |
B、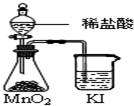 比较MnO2、Cl2、I2的氧化性 |
C、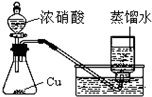 制取少量NO2 |
D、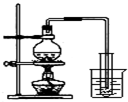 实验室制取蒸馏水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、已知CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-802 kJ/mol,甲烷的燃烧热为802 kJ/mol |
| B、等量H2在O2中完全燃烧,生成H2O(g)比生成H2O(l)放出的热量多 |
| C、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 |
| D、由石墨比金刚石稳定可知:C(金刚石,s)═C(石墨,s)△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯气、二氧化硫均能使品红溶液褪色,说明二者均有氧化性 |
| B、铁与稀硝酸,稀硫酸反应均有气泡产生,说明铁与两种酸均能发生置换反应 |
| C、向溶液中滴加酸化的硝酸钡溶液出现白色沉淀,说明该溶液中一定有硫酸根离子 |
| D、分别充满氯化氢气体,氨气的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 方法一 | CO(g)+2H2(g)?CH3OH(g) |
| 方法二 | CO2(g)+3H2(g)?CH3OH(g)+H2O(g) |
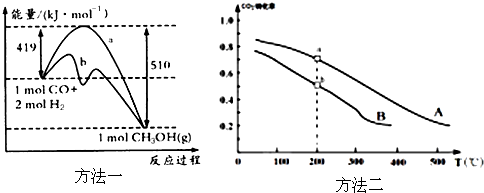
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com