
【题目】设阿伏加德罗常数的值为NA,下列说法中正确的是
A.常温常压下,15g的—12CH3中含有中子数6NA
B.46 g乙醇和46 g甲酸含有的氧原子数均为NA
C.32g甲醇中含有C—H键的数目为4NA
D.标准状况下,1L甲醛完全燃烧所生成的气态产物的分子数为![]()
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】将2.4g某有机物M置于密闭容器中燃烧,定性实验表明产物是CO2、CO和水蒸气。将燃烧产物依次通过浓硫酸、碱石灰和灼热的氧化铜(试剂均足量,且充分反应),测得浓硫酸增重1.44g,碱石灰增重1.76g,氧化铜减轻0.64g。下列说法中不正确的是
A. M的实验式为CH2O
B. 若要得到M的分子式,还需要测得M的相对分子质量或物质的量
C. 若M的相对分子质量为60,则M一定为乙酸
D. 通过红外光谱仪可分析M中的官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)M与Q是同素异形体,由M=Q;△H = -19KJ/mol可知,M比Q________(填稳定、不稳定)。
(2)已知:![]()
![]()
请写出CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式_________________。
(3)在与外界隔离的体系中,自发过程将导致体系的熵__________,(填“增大”、“减小”、“不变”);对于同一种物质,________时熵值最大(填“固态”、“液态”、“气态”)。
(4)某工厂实验室用CO和H2制备CH3OH,其原理为:![]() 该温度下的化学平衡常数表达式__________________;若在298K、398K时化学平衡常数分别为K1、K2,则K1 ___ K2(填“>”、“<”、“=”)。
该温度下的化学平衡常数表达式__________________;若在298K、398K时化学平衡常数分别为K1、K2,则K1 ___ K2(填“>”、“<”、“=”)。
(5)500℃条件下,对于反应![]() ,K=2.33 ,测得某时刻,A(g)、B(g)、C(g)的浓度均为0.5mol/L,则此时v(正) ______ v(逆)(填“>”“<”或“=”)。
,K=2.33 ,测得某时刻,A(g)、B(g)、C(g)的浓度均为0.5mol/L,则此时v(正) ______ v(逆)(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有一包白色固体,可能含有![]() 和
和![]()
![]() 中的一种或多种。下列根据实验事实得出的结论正确的是
中的一种或多种。下列根据实验事实得出的结论正确的是
A.取一定量固体加热,若质量减少,说明原固体中一定含有![]()
B.取一定量固体,向其中加入稀盐酸,有气体生成,说明原固体中一定含有![]()
C.取一定量固体,溶解,向溶液中滴加适量![]() 溶液,观察到有白色沉淀生成,说明原固体中一定含有
溶液,观察到有白色沉淀生成,说明原固体中一定含有![]()
D.取一定量固体,溶解,向溶液中加入适量澄清石灰水,充分反应后观察到有白色沉淀生成,说明原固体中一定含有![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以含锂电解铝废渣(主要成分为LiF、AlF3、NaF,少量CaO等)为原料,生产碳酸锂的工艺流程如下:(已知:常温下,LiOH可溶于水,Li2CO3微溶于水)
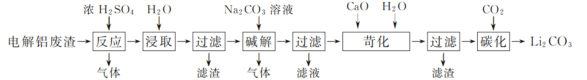
(1)含锂电解铝废渣与浓硫酸在200~400 ℃条件下反应2 h,加水浸取后过滤,得到的滤渣主要成分是________(填化学式)。
(2)流程中浸取后的过滤操作需要趁热在恒温装置中进行,否则会导致Li2SO4的收率下降,原因是________。(已知部分物质的溶解度数据见下表)
温度/℃ | Li2SO4/g | Al2(SO4)3/g | Na2SO4/g |
0 | 36.1 | 31.2 | 4.9 |
10 | 35.4 | 33.5 | 9.1 |
20 | 34.8 | 36.5 | 19.5 |
30 | 34.3 | 40.4 | 40.8 |
40 | 33.9 | 45.7 | 48.8 |
(3)40℃下进行碱解反应,得到粗碳酸锂与氢氧化铝的混合滤渣,生成氢氧化铝的离子方程式为________。
(4)苛化过程中加入的氧化钙将不溶性的碳酸锂转化成氢氧化锂溶液。若氧化钙过量,则可能会造成________。
(5)碳化反应中,CO2的吸收采用了气、液逆流的方式,这样做的优点是________。整个工艺流程中可以循环利用的物质有________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() (x)、
(x)、![]() (y)、
(y)、![]() (z) 互为同分异构体,下列说法错误的是
(z) 互为同分异构体,下列说法错误的是
A.x的同分异构体只有y和z两种
B.z的二氯代物只有三种
C.x、y可使溴的四氯化碳溶液因发生加成反应而褪色
D.x、y、z中只有x的所有原子可能处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定实验室长期存放的Na2SO3固体的纯度,准确称取Wg固体样品,配成250mL溶液。设计了以下两种实验方案:
方案Ⅰ:取25.00mL上述溶液,加入足量的用过量盐酸酸化的BaCl2溶液,过滤、洗涤和干燥沉淀,称得沉淀的质量为m1g。
方案Ⅱ:取25.00mL上述溶液,加入过量的盐酸酸化的Ba(NO3)2溶液,过滤、洗涤和干燥沉淀,称重,其质量为m2g。
(1)配制250mLNa2SO3溶液时,必须用到的实验仪器有:烧杯、玻璃棒、天平、药匙、_______、______。
(2)写出Na2SO3固体氧化变质的化学方程式______________。
(3)方案Ⅰ加入过量的盐酸酸化的BaCl2溶液,目的是___________,在过滤前,需要检验是否沉淀完全,其操作是______________。
(4)方案Ⅰ中,若滤液浑浊,将导致测定结果____________(填“偏高”或“偏低”)。
(5)若操作正确,结果为m1<m2,试分析原因是_________。
(6)取25.00mL上述溶液,用cmol/L酸性KMnO4溶液滴定测定Na2SO3的纯度,已知酸性条件下,KMnO4通常被还原为Mn2+滴定达到终点时的现象为___________,若达到滴定终点时用去VmL KMnO4溶液,则Na2SO3固体的纯度表达式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学购买了一瓶“84消毒液”,包装说明如下,下列分析不正确的是( )

A.“84消毒液”保存时不能敞口放置,需要密封保存
B.该“84消毒液”中NaClO的物质的量浓度约为4mol·L-1
C.取100mL该“84消毒液”稀释100倍后用以消毒,稀释后的溶液中c(Na+)约为0.04mol·L-1
D.欲用NaClO固体配制含25% NaClO的消毒液480mL,需要称量的NaClO固体质量为142.8g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以SO2、软锰矿(主要成分MnO2,少量Fe、Al、Ca及Pb的化合物等)、氨水及净化剂等为原料可制备MnSO4溶液和Mn3O4,主要实验步骤如下:

步骤Ⅰ:如图所示装置,将SO2通入B中的软锰矿浆液中(MnO2+SO2 = MnSO4)。
步骤Ⅱ:充分反应后,在不断搅拌下依次向三口烧瓶中加入适量纯净的MnO2、MnCO3,最后加入适量Na2S沉铅等重金属。
步骤Ⅲ:过滤得MnSO4溶液。
(1)装置A用于制取SO2,反应的化学方程式为_____。
(2)装置B中反应应控制在90~100℃,适宜的加热方式是_____。
(3)装置C的作用是_____。
(4)“步骤Ⅱ”中加入纯净MnO2的目的是_____,用MnCO3调节溶液pH时,需调节溶液pH范围为_____(该实验条件下,部分金属离子开始沉淀和沉淀完全的pH如下)。
金属离子 | Fe2+ | Fe3+ | Al3+ | Mn2+ |
开始沉淀pH | 7.04 | 1.87 | 3.32 | 7.56 |
沉淀完全pH | 9.18 | 3.27 | 4.9 | 10.2 |
(5)已知:①用空气氧化Mn(OH)2浊液可制备Mn3O4[6Mn(OH)2+O2![]() 2Mn3O4+6H2O],主要副产物为MnOOH;反应温度和溶液pH对产品中Mn的质量分数的影响如下图所示:
2Mn3O4+6H2O],主要副产物为MnOOH;反应温度和溶液pH对产品中Mn的质量分数的影响如下图所示:
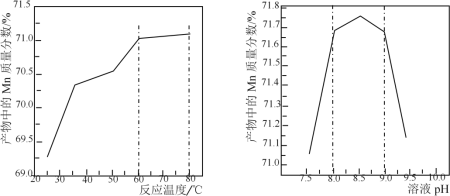
②反应温度超过80℃时,Mn3O4产率开始降低。
③Mn(OH)2是白色沉淀,Mn3O4呈黑色;Mn3O4、MnOOH中锰的质量分数理论值依次为72.03%、62.5%。
请补充完整由步骤Ⅲ得到的MnSO4溶液,并用氨水等制备较纯净的Mn3O4的实验方案:_____,真空干燥6小时得产品Mn3O4。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com