
【题目】(1)M与Q是同素异形体,由M=Q;△H = -19KJ/mol可知,M比Q________(填稳定、不稳定)。
(2)已知:![]()
![]()
请写出CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式_________________。
(3)在与外界隔离的体系中,自发过程将导致体系的熵__________,(填“增大”、“减小”、“不变”);对于同一种物质,________时熵值最大(填“固态”、“液态”、“气态”)。
(4)某工厂实验室用CO和H2制备CH3OH,其原理为:![]() 该温度下的化学平衡常数表达式__________________;若在298K、398K时化学平衡常数分别为K1、K2,则K1 ___ K2(填“>”、“<”、“=”)。
该温度下的化学平衡常数表达式__________________;若在298K、398K时化学平衡常数分别为K1、K2,则K1 ___ K2(填“>”、“<”、“=”)。
(5)500℃条件下,对于反应![]() ,K=2.33 ,测得某时刻,A(g)、B(g)、C(g)的浓度均为0.5mol/L,则此时v(正) ______ v(逆)(填“>”“<”或“=”)。
,K=2.33 ,测得某时刻,A(g)、B(g)、C(g)的浓度均为0.5mol/L,则此时v(正) ______ v(逆)(填“>”“<”或“=”)。
【答案】不稳定 ![]() 增大 气态
增大 气态 ![]() > >
> >
【解析】
(1)M与Q是同素异形体,由M=Q;△H = -19KJ/mol可知,M所具有的能量高,M比Q不稳定;
(2)已知:①![]() ②
②![]()
根据盖斯定律①×2-②得:CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式![]() ;
;
(3)在与外界隔离的体系中,自发过程将导致体系的熵增大;对于同一种物质,气态时熵值最大;
(4)平衡常数:可逆化学反应达到平衡状态时生成物与反应物的浓度(方程式系数幂次方)乘积比或反应产物与反应底物的浓度(方程式系数幂次方)乘积比。![]() 该温度下的化学平衡常数表达式
该温度下的化学平衡常数表达式![]() ;
;
该反应是放热反应,升高温度,平衡逆向移动,若在298K、398K时化学平衡常数分别为K1、K2,则K1 > K2。
(5)500℃条件下,对于反应![]() ,K=2.33 ,测得某时刻,A(g)、B(g)、C(g)的浓度均为0.5mol/L,此时的浓度商为:Qc=
,K=2.33 ,测得某时刻,A(g)、B(g)、C(g)的浓度均为0.5mol/L,此时的浓度商为:Qc=![]() <K,反应正向进行,则此时v(正)> v(逆)。
<K,反应正向进行,则此时v(正)> v(逆)。


科目:高中化学 来源: 题型:
【题目】为了验证Fe3+的性质,某化学兴趣小组设计了下图所示的一组实验,其中实验方案设计错误的是( )

A. 只有④ B. 只有③
C. ③和④均错误 D. 全部错误
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应不属于氧化还原反应的是 ( )
A.3Fe + 4H2O(g) ![]() Fe3O4 + 4H2
Fe3O4 + 4H2
B.3NO2 +H2O = 2HNO3+ NO
C.Ca(OH)2+SO2 = CaSO3 + H2 O
D.Cu+2H2SO4 (浓)![]() CuSO4+SO2↑+ 2H2O
CuSO4+SO2↑+ 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3H2O2 + 2H2CrO4 = 2Cr(OH)3 + 3O2 ↑+ 2H2O
(1)其中Cr被___________,H2O2作____________剂。
(2)_____________是氧化产物,_______________发生还原反应。
(3)反应转移了0.3mol电子,则产生的气体在标准状态下体积约为__________。
(4)用单线桥或双线桥法标明电子转移的方向和数目。_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度的恒容绝热闭容器中进行如下可逆反应![]() 下列叙述中,能说明反应已达到化学平衡状态的是
下列叙述中,能说明反应已达到化学平衡状态的是
①A、B、C的分子数之比为1:2:3
②单位时间内生成 amolA,同时生成3amolC
③![]() 的物质的量浓度不再变化
的物质的量浓度不再变化
④![]() :
:![]() :
:![]() :2:3
:2:3
⑤混合气体的密度不再变化
⑥容器内的压强不再变化
A.②③⑥B.③④⑥C.②③D.①②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作对应的现象不符合事实的是( )
A.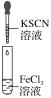 向FeCl3溶液中滴入KSCN溶液,溶液颜色变红
向FeCl3溶液中滴入KSCN溶液,溶液颜色变红
B.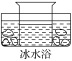 将混有少量氯化钾的硝酸钾饱和溶液在冰水中冷却,氯化钾晶体先析出
将混有少量氯化钾的硝酸钾饱和溶液在冰水中冷却,氯化钾晶体先析出
C.![]() 向装有10 mL溴水的分液漏斗中加入5 mL正己烷,光照下振荡后静置,应该为萃取后分层,下层无色,上层有色
向装有10 mL溴水的分液漏斗中加入5 mL正己烷,光照下振荡后静置,应该为萃取后分层,下层无色,上层有色
D.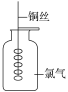 将灼热的铜丝伸入盛有氯气的集气瓶中,铜丝剧烈燃烧,产生棕黄色的烟
将灼热的铜丝伸入盛有氯气的集气瓶中,铜丝剧烈燃烧,产生棕黄色的烟
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A.醋酸溶液与氢氧化钠反应:![]()
B.铜溶于浓硝酸:![]()
C.将过量的二氧化碳通入烧碱溶液:![]()
D.Ba(OH)2溶液与硫酸铜溶液反应:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的值为NA,下列说法中正确的是
A.常温常压下,15g的—12CH3中含有中子数6NA
B.46 g乙醇和46 g甲酸含有的氧原子数均为NA
C.32g甲醇中含有C—H键的数目为4NA
D.标准状况下,1L甲醛完全燃烧所生成的气态产物的分子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.0molPCl3(g)和1.0molCl2(g)充入体积不变的密闭容器中,在一定条件下发生反应:PCl3(g)+Cl2(g)PCl5(g),达到平衡时,PCl5为0.40mol。如果此时移走1.0 mol PCl3和0.50mol Cl2,在相同温度下再达平衡时PCl5的物质的量是
A.0.2 molB.0.4 mol
C.小于0.2 molD.大于0.20 mol,小于0.40 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com