
【题目】下列有关叙述正确的是( )
A.乙二酸与乙二醇在浓硫酸的作用下可以发生酯化反应生成八元环酯
B.新制备的氢氧化铜悬浊液可以鉴别 乙醇、乙酸、乙醛
C.乙炔、乙苯、聚乙烯、乙醇、乙醛都能使酸性KMnO4褪色
D.取某卤代烃少许与氢氧化钠溶液共热,然后加硝酸银溶液,看是否有白色沉淀可以验证某卤代烃中是否含有氯元素。
科目:高中化学 来源: 题型:
【题目】氨在化肥生产、贮氢及燃煤烟气脱硫脱硝等领域用途非常广泛。
(1)尿素[CO(NH2)2]与氰酸铵(NH4CNO)互为___________;(选填:“同一物质”或“同系物”或“同分异构体”)氰酸铵属于_______化合物(选填:“离子”或“共价”)。
(2)液氨是一种贮氢材料,已知:断开1mol共价键吸收的能量数据如表
共价键 | H—H | N—H | N≡N |
kJ·mol-1 | 436 | 390.8 | 946 |
则合成氨反应:N2(g) + 3H2 (g)= 2NH3(g) ,生成2mol氨气放出 _________kJ热量,若1molN2与3molH2在一定条件下反应,达到平衡时放出36.32kJ热量,则此时NH3所占的体积分数为______ 。如图装置通直流电,液氨可电解释放氢气,该过程中能量转化方式为由电能转化为_____能。

(3)氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和NH3,在一定条件下发生反应:6NO(g) + 4NH3(g) ![]() 5N2(g) +6H2O(g)。
5N2(g) +6H2O(g)。
①能说明该反应已达到平衡状态的标志是_______(不定项选择)。
a.反应速率4v ( NH3) =5v ( N2)
b.容器内压强不再随时间而发生变化
c.容器内N2的物质的量分数不再随时间而发生变化
d.容器内n(NO)∶n(NH3)∶n(N2)∶n(H2O) = 6∶4∶5∶6
②某次实验中测得容器内NO及N2的物质的量随时间变化如图所示,图中v (正)与v (逆)相等的点为_________(选填字母)。
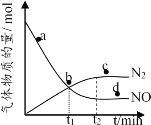
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯碳酸锰在电子工业中有着重要的应用,湿法浸出软锰矿(主要成分为MnO2,含有少量Fe、Al、Mg等杂质元素)制备高纯碳酸锰的流程如下:其中除杂过程包括:①向浸出液中加入一定量的试剂X,调节浸出液的pH为3.5~5.5;②再加入一定量的软锰矿和双氧水,过滤;③…下列说法正确的是(已知室温下:Kap[Mg(OH)2]=1.8×10-11,Kap[Al(OH)3]=3.0×10-34,Kap[Fe(OH)3]=4.0×10-38。)
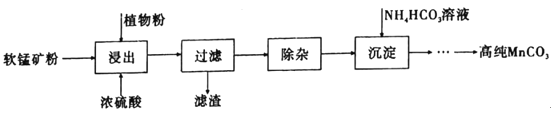
A.浸出时加入植物粉的作用是作为还原剂
B.除杂过程中调节浸出液的pH为3.5~5.5可完全除去Fe、Al、Mg等杂质
C.试剂X可以是MnO、MnO2、MnCO3等物质
D.为提高沉淀MnCO3步骤的速率可以持续升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据反应原理设计的应用,不正确的是
A. CO32- + H2O ![]() HCO3-+ OH- 热的纯碱溶液清洗油污
HCO3-+ OH- 热的纯碱溶液清洗油污
B. Al3+ + 3H2O ![]() Al(OH)3(胶体)+ 3H+ 明矾净水
Al(OH)3(胶体)+ 3H+ 明矾净水
C. SnCl2 + H2O ![]() Sn(OH)Cl↓ + HCl 配制氯化亚锡溶液时加入氢氧化钠
Sn(OH)Cl↓ + HCl 配制氯化亚锡溶液时加入氢氧化钠
D. TiCl4+ (x+2)H2O(过量) ![]() TiO2·x H2O↓ + 4HCl 用TiCl4制备TiO2
TiO2·x H2O↓ + 4HCl 用TiCl4制备TiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科罗拉多大学的克利斯托(S.Cristol)等人合成了一种有机分子,这种分子让他想起罗马的两面神Janus—罗马的守门神,克利斯托的同事迈金泰(Macintyre)就建议将该分子叫做Janusene。该有机物的结构简式如图所示:
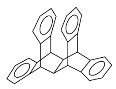
下列说法正确的是( )
A.该有机物属于苯的同系物
B.该有机物完全燃烧生成CO2和H2O的物质的量之比为15∶11
C.该有机物的一氯代物只有4种
D.该有机物只能发生取代反应而不能发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知还原性:![]() 。向含amolKI和amolK2SO3的混合液中通入bmolCl2充分反应
。向含amolKI和amolK2SO3的混合液中通入bmolCl2充分反应![]() 不考虑Cl2与I2之间的反应
不考虑Cl2与I2之间的反应![]() 。
。
![]() 当
当![]() 时,反应中转移电子的物质的量范围为________________
时,反应中转移电子的物质的量范围为________________![]() 用a表示
用a表示![]() 。
。
![]() 当
当![]() 时,I-的物质的量为_________mol。
时,I-的物质的量为_________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙三个容器中最初存在的物质及数量如图所示,三个容器最初的容积相等,温度相同,反应中甲、丙的容积不变,乙中的压强不变,在一定温度下反应达到平衡。下列说法正确的是
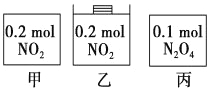
A. 平衡时各容器内c(NO2)的大小顺序为乙>甲>丙
B. 平衡时N2O4的百分含量:乙>甲=丙
C. 平衡时甲中NO2与丙中N2O4的转化率相同
D. 平衡时混合物的平均相对分子质量:甲>乙>丙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com