
【题目】下列现象不能用“相似相溶规则”原理解释的是( )
A.氯化氢易溶于水
B.氯气易溶于氢氧化钠溶液
C.碘易溶于四氯化碳
D.碘难溶于水
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】用50mL 0.50molL﹣1盐酸与50mL 0.55molL﹣1 NaOH溶液,在如图所示的装置中进行中和反应,测定强酸与强碱反应的反应热. 
起始温度t1/℃ | 终止温度t2/℃ | 温度差 | |||
HCl | NaOH | 平均值 | |||
1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
2 | 24.5 | 24.2 | 24.45 | 27.6 | 3.15 |
3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
(1)在该实验中,量取50mL盐酸或NaOH溶液,需要用到的玻璃仪是;
(2)装置中大、小烧杯之间填满碎泡沫塑料的目的是;
(3)某同学实验记录的数据如上表所示,其中记录的终止温度是指温度;
(4)计算该实验发生中和反应时放出的热量为kJ[中和后生成的溶液的比热容c=4.18J(g℃)﹣1 , 稀溶液的密度都为1gcm﹣3];
(5)如果用50mL 0.55mol/L的氨水(NH3H2O)代替NaOH溶液进行上述实验,通过测得的反应热计算中和热,其中和热△H会偏大,其原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用键能的大小来解释的是( )
A.N元素的电负性较大,但N2的化学性质很稳定
B.稀有气体一般难发生反应
C.HF,HCl,HBr,HI的稳定性逐渐减弱
D.F2比O2更容易与H2反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100mL 0.01molL﹣1HA溶液中逐滴加入0.02molL﹣1MOH溶液,图中所示曲线表示,混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中,不正确的是( ) 
A.HA的电离方程式为:HA=H++A﹣
B.MOH为一元弱碱
C.K点对应的溶液中有:c(MOH)+c(M+)=0.02molL﹣1
D.N点对应的溶液中有:c(M+)=c(A﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A是来自石油的重要有机化工原料,此物质可以用来衡量一个国家石油化工发展水平.C在一定条件下也会生成D,D能使石蕊溶液变红;E是具有果香味的有机物,F是一种高分子化合物,可制成多种包装材料. 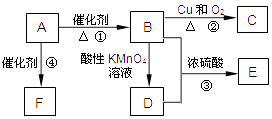
(1)A物质的结构简式为 .
(2)B→C的反应类型:;
(3)反应③的化学方程式为 .
(4)请设计一个简单的实验,以验证C物质存在该官能团的方法 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应3Cl2+6NaOH=5NaCl+NaClO3+3H2O,以下叙述正确的是( )
A.Cl2是氧化剂,NaOH是还原剂
B.被氧化的Cl原子和被还原的Cl原子的物质的量之比为5∶1
C.Cl2既做氧化剂又做还原剂
D.氧化剂得电子数与还原剂失电子数之比为5∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于CH4的叙述中不正确的是
A. CH4是无色、无味、极难溶于水的气体
B. CH4的键长相等,键角相同,正四面体结构
C. CH4能使酸性高锰酸钾溶液褪色
D. CH4和Cl2在光照条件下反应得到多种油状物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一包铁粉和氧化铜混合均匀的粉末样品4.40g,加入50mL稀硫酸恰好充分反应后,得到只含一种金属阳离子的浅绿色溶液和1.28g固体铜.并放出H2 . 试计算:
(1)固体铜的物质的量为mol,该样品中铁粉和氧化铜的物质的量之比为 .
(2)硫酸的物质的量的浓度molL﹣1 , 产生H2在标准状况下的体积L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A.标况下,22.4L的Cl2与足量水反应中电子转移了2NA
B.0.1mol/LK2SO4溶液中含有0.2NA个阳离子
C.常温常压下,22.4LO2气体的分子数小于NA
D.20g D2O所含的中子数为9NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com