
����Ŀ���л���A������ʯ�͵���Ҫ�л�����ԭ�ϣ������ʿ�����������һ������ʯ�ͻ�����չˮƽ��C��һ��������Ҳ������D��D��ʹʯ����Һ��죻E�Ǿ��й���ζ���л��F��һ�ָ߷��ӻ�������Ƴɶ��ְ�װ���ϣ� 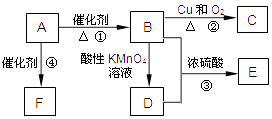
��1��A���ʵĽṹ��ʽΪ ��
��2��B��C�ķ�Ӧ���ͣ���
��3����Ӧ�۵Ļ�ѧ����ʽΪ ��
��4�������һ����ʵ�飬����֤C���ʴ��ڸù����ŵķ��� ��
���𰸡�
��1��CH2=CH2
��2��������Ӧ
��3��CH3COOH+CH3CH2OH ![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
��4��ȡ����C���Թ��У�����������Һ��ˮԡ���ȣ�����������������������������ͭ��Һ��������ש����ɫ������������ȩ��
���������⣺A������ʯ�͵���Ҫ�л�����ԭ�ϣ������ʿ�����������һ������ʯ�ͻ�����չˮƽ������A��H2C=CH2 �� E�Ǿ��й���ζ���л��E��������ʹ���Ӧ����������B��Dһ������һ���Ǵ���B�ܱ���������D��A��Ӧ����B��̼ԭ�Ӹ������䣬����B��CH3CH2OH��D��CH3COOH��ͭ�����������������£�CH3CH2OH��������������C������C��CH3CHO���������Ҵ�����������Ӧ����EΪCH3COOCH2CH3 �� A��Ӧ����F��F��һ�ָ߾����ϩ�����Ӿ۷�Ӧ���ɸ߾���FΪ ![]() ����1��ͨ�����Ϸ���֪��AΪCH2=CH2 �� ���Դ��ǣ�CH2=CH2����2��B��������������C�����Է�Ӧ������������Ӧ�����Դ��ǣ�������Ӧ����3���÷�ӦΪ�Ҵ��������������Ӧ����Ӧ����ʽΪCH3COOH+CH3CH2OH
����1��ͨ�����Ϸ���֪��AΪCH2=CH2 �� ���Դ��ǣ�CH2=CH2����2��B��������������C�����Է�Ӧ������������Ӧ�����Դ��ǣ�������Ӧ����3���÷�ӦΪ�Ҵ��������������Ӧ����Ӧ����ʽΪCH3COOH+CH3CH2OH ![]() CH3COOCH2CH3+H2O�����Դ��ǣ�CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O�����Դ��ǣ�CH3COOH+CH3CH2OH ![]() CH3COOCH2CH3+H2O����4��CΪ��ȩ��������������Ӧ������������ͭ����Һ������ȩ��ȩ��������鷽��Ϊȡ����C���Թ��У�����������Һ��ˮԡ���ȣ�����������������������������ͭ��Һ��������ש����ɫ������������ȩ����
CH3COOCH2CH3+H2O����4��CΪ��ȩ��������������Ӧ������������ͭ����Һ������ȩ��ȩ��������鷽��Ϊȡ����C���Թ��У�����������Һ��ˮԡ���ȣ�����������������������������ͭ��Һ��������ש����ɫ������������ȩ����
���Դ��ǣ�ȡ����C���Թ��У�����������Һ��ˮԡ���ȣ�����������������������������ͭ��Һ��������ש����ɫ������������ȩ����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�������������һ����̼�������з�Ӧ��Fe2O3��s��+3CO��g��2Fe��s��+3CO2��g��
��1���ٸ÷�Ӧ��ƽ�ⳣ������ʽΪ��K= ��
�ڸ��¶��£���2Lʢ��Fe2O3��ĩ���ܱ�������ͨ��CO���壬10min�������˵�����11.2g����10min��CO��ƽ����Ӧ��Ϊ ��
��2��˵���÷�Ӧ�Ѵﵽƽ��״̬�� ��
a��CO��CO2������������������������ȣ�
b��CO����CO2�����������ٸı�
c��CO����CO2�����������50%
��3��I2O5��ʹH2S��CO��HCl�������������ڶ����ⶨCO�ĺ�������֪��
2I2��s��+5O2��g��=2I2O5��s����H1=��75.56kJmol��1
2CO��g��+O2��g��=2CO2��g����H2=��566.0kJmol��1
д��CO��g����I2O5��s����Ӧ����I2��s����CO2��g�����Ȼ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й�ҩƷ�ı����ʹ�ò���ȷ���ǣ� ��
A.��ˮʢ�ڴ�ĥɰ��������ϸ��ƿ��
B.����ͭ��ĩ���Ȼ��Ƶ�ҩƷ�����ڸ�������
C.���������ˮ���ܷⱣ��
D.��̼���Ƶζ�����ʱ��Na2CO3ҺӦʢ����ʽ�ζ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪2SO2��g��+O2��g��2SO3��g����H=��198.0 kJmol��1 �� ����500��ʹ����������£���Ӧ���ݻ��̶����ܱ������н��У������й�˵����ȷ���ǣ� ��
A.�÷�Ӧ�����£���ʼʱ�������г���2molSO2��1molO2 �� ��Ӧƽ��ʱ�������ͷ�198.0 kJ������
B.�ﵽƽ��ʱ��SO2��SO3��Ũ��һ�����
C.��Ӧ��ϵ�У����������ܶȱ��ֲ��䣬��Ӧ�ﵽƽ��
D.����ѹǿ�������¶������ڼӿ췴Ӧ���ʣ��������¶ȶ�ƽ��ת���ʲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��ȥ�����е�CaCl2��MgCl2��Na2SO4 �Լ���ɳ�����ʣ�ijͬѧ�����һ���Ʊ����ε�ʵ�鷽�����������£�![]()
��1���ж�BaCl2�ѹ����ķ�������
��2���ڢ��У���ص����ӷ���ʽ����
��3��Ϊ���龫�δ��ȣ�������230mL0.2mol/L NaCl(����)��Һ��������������ƽ��ȡ���ι��������Ϊ �� ��Ҫ�IJ�����������Ͳ�� ��
��4������NaCl(����)��Һʱ�����������в�������ɽ��ƫ�͵�����
A������ʱNaCl�ѳ��� B����ƽ����������ʴ
C������ҡ��ʱ��Һ���½��ּ�ˮ D������ʱ���ӿ̶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������á��������ܹ���ԭ�����͵��ǣ� ��
A.�Ȼ���������ˮ
B.��������������������Һ
C.�����������Ȼ�̼
D.��������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڵ��NaClˮ��Һ��˵����ȷ���� �� ��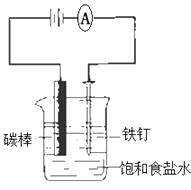
�ٵ�����ΪCl2��Na
�ڵ������У�̼��һ����������ɫ����
�۵��һ��ʱ�����̼����������Һ�еμӷ�̪��Һ����Һ�ʺ�ɫ
�ܵ��һ��ʱ�����������������Һ�еμӷ�̪��Һ����Һ�ʺ�ɫ
A.�٢�
B.�٢�
C.�ڢ�
D.�ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������һ�����Լ�ǿ���������ᣬ�������Ʊ��������Ρ�������ʯ�ᴿ�ȷ��森
�������ϵõ������йظ��������Ϣ��
���� | ����ʽ | ��� | �е� |
������ | HClO4 | ��ɫҺ�� | 130�� |
��ҵ�������������ͬʱ���������������ƣ���ҵ������ͼ��
��1�������ٵ������� ��
��2��Ca��ClO��2��ClO2��NaClO��NaClO2�Ⱥ��Ȼ����ﶼ�dz��õ���������Ư������Ϊ���Ƕ�����
��3����Ӧ������Ͷ��ʱ��������Ũ���ᣬ�����Ŀ�� ��
��4����Ӧ�����з�����Ӧ�����ӷ���ʽΪ ��
��5��ijѧϰС��ģ�ҵ����ͼ�е�������̣���Һ������ʱ�����ռ���Ʒ�Ի��HClO4��Ʒ����������һ�����Ƿ������˵������ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����к�����NaCl��Na2SO4��Na2CO3�����ʵ�NaNO3��Һ�����ʵ����Լ���ȥ���ʣ��õ�������NaNO3�����ʵ��������ͼ��ʾ��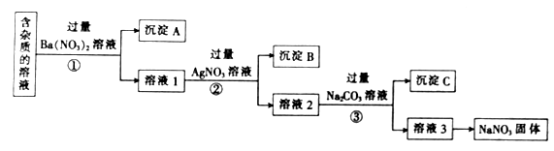
��1������A����Ҫ�ɷ���(�ѧʽ)��
��2�����з�Ӧ�Ļ�ѧ����ʽ����
��3���٢ڢ��о����еķ����������
��4��ʵ����������ʵ���õ�NaNO3��������480 mL 0.40 mol.L-1NaNO3��Һ��
��������ҺǰҪ�ȼ��㣬���ȡNaNO3����g��
��ijͬѧת����Һ�IJ�����ͼ��ʾ��ͼ���������������ձ���,��ͬѧ�����еĴ�������
�����ý�ͷ�ιܶ���ʱ,��С�ļ�ˮ�����˿̶��ߣ���Ӧ�ò�ȡ�Ĵ�����������
�����в�����,���������������Һ��Ũ��ƫ�͵���(����ĸ)��
a.û��ϴ���ձ��Ͳ�����
b.����ʱ,���ӿ̶���
c.ϴ�Ӻ������ƿ�в�����������ˮ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com