


 ��ǰ�κ�ͬ����ϰϵ�д�
��ǰ�κ�ͬ����ϰϵ�д� ����С��ҵϵ�д�
����С��ҵϵ�д� �Ƹ�С״Ԫ����������ϰ��ϵ�д�
�Ƹ�С״Ԫ����������ϰ��ϵ�д� �ɹ�ѵ���ƻ�ϵ�д�
�ɹ�ѵ���ƻ�ϵ�д� ����ѵ����ֱͨ�п�����ϵ�д�
����ѵ����ֱͨ�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��V��B2��=0.8mol/�� L?s�� |
| B��V��A2��=0.8mol/�� L?s�� |
| C��V��C��=0.6mol/�� L?s�� |
| D��V��D��=0.6mol/�� L?s�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Xռ������������������� |
| B����λʱ������a molX��ͬʱ����3a molY |
| C��X��Y��Z��Ũ�Ȳ��ٱ仯 |
| D��X��Y��Z�ķ�������Ϊ1��3��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A����������ǻ���� |
| B���������ǹ������þ�Ļ���� |
| C����ɫ�����ҵ���Ҫ�ɷ����������� |
| D��K+��[Al��OH��4]-��SiO32-һ����������ҺX�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Al��OH��3 | Fe��OH��2 | Fe��OH��3 | |
| ��ʼ����ʱ | 3.4 | 6.3 | 1.5 |
| ��ȫ����ʱ | 4.7 | 8.3 | 2.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��CH4��CH3CH2CH3���ܽ��ʯ��ʯī����뭡�뮡�밣���16O��17O��18O�����Ҵ���CH3CH2OH���ͼ��ѣ�CH3OCH3������������O2���������O3����
��CH4��CH3CH2CH3���ܽ��ʯ��ʯī����뭡�뮡�밣���16O��17O��18O�����Ҵ���CH3CH2OH���ͼ��ѣ�CH3OCH3������������O2���������O3����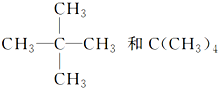
| ��� | ͬλ�� | ͬϵ�� | ͬ�������� | ͬ���칹�� |
| ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��д�����ķ���ϩ�ڴ����������ºϳɾ��ķ���ϩ�ķ�Ӧ����ʽ
��д�����ķ���ϩ�ڴ����������ºϳɾ��ķ���ϩ�ķ�Ӧ����ʽ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �ѣ�Ti������Ϊ��������֮��ĵ�����������ͼ��ʾ�����ѳ����ȼ�ͼ״�����ɲ�ҵ�����Դ�������Դ�����ʣ����ٻ�����Ⱦ������д���пհף�
�ѣ�Ti������Ϊ��������֮��ĵ�����������ͼ��ʾ�����ѳ����ȼ�ͼ״�����ɲ�ҵ�����Դ�������Դ�����ʣ����ٻ�����Ⱦ������д���пհף��鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com