
【题目】亚硫酸盐是一种常见食品添加剂,为检验某食品中亚硫酸盐含量,某研究小组设计了如下两种实验流程:
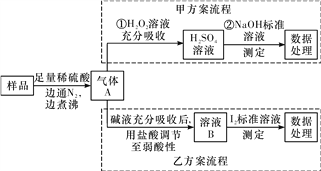
(1)气体A的主要成分是________(填化学式),加热煮沸时必须先向烧瓶中加入碎瓷片,其目的是______________________;边通入N2边煮沸的目的是________________。
(2)写出甲方案第①步反应的离子方程式:________________________。
(3)若用盐酸代替稀硫酸处理样品,则按乙方案实验测定的结果______(填“偏高”、“偏低”或“无影响”)。
(4)若亚硫酸盐为Na2SO3,取样品w g,按乙方案测得消耗0.0100 mol·L-1I2溶液V mL,则样品中含Na2SO3的质量分数是__________(用含w、V的代数式表示)。
【答案】 SO2 防止加热煮沸时暴沸 将生成的SO2全部赶出 SO2+H2O2===2H++SO![]() 无影响 1.26V×10-3/w
无影响 1.26V×10-3/w
【解析】(1)亚硫酸盐与稀硫酸反应生成气体SO2,为防止液体加热时暴沸,一般可加入碎瓷片;由于装置中会有残留的SO2,所以边通入N2边煮沸的目的是将生成的SO2全部赶出;(2)SO2具有还原性,可被氧化剂H2O2所氧化,反应的离子方程式为SO2+H2O2=SO42-+2H+;(3)用盐酸代替硫酸,生成的SO2气体中混有少量HCl,因SO2用碱液吸收后需再用盐酸调节溶液至弱酸性,因此混合气体中含有HCl,对实验结果无影响;(5)反应的离子方程式为H2O+SO32-+I2=SO42-+2H++2I-,则SO2~SO32-~I2,需要碘的物质的量是0.01000molL-1×V×10-3L=10-5mol,所以样品中含Na2SO3的质量分数是![]() 。
。


科目:高中化学 来源: 题型:
【题目】已知反应Cu(s)+2Ag+(aq)===Cu2+(aq)+2Ag(s)为自发进行的氧化还原反应,将其设计成如右图所示的原电池,下列说法中正确的是( )

A. 铜电极是正极,其电极反应为Cu-2e-===Cu2+
B. 当铜电极质量减少0.64 g时,电解质溶液中有0.02 mol电子通过
C. 装置盐桥中可装有含琼脂的KCl饱和溶液
D. 银电极上发生还原反应,电极质量增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】污水处理的主要方法有:①中和法;②化学沉淀法;③氧化还原法;④过滤法。其中属于化学方法的有( )。
A. ①②③ B. ①②④
C. ②③④ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3和纯净的O2在一定条件下发生反应:4NH3(g)+3O2(g)2N2(g)+6H2O(g),现向一容积不变的2 L密闭容器中充入4 mol NH3和 3 mol O2,4 min后达到平衡,测得生成的H2O(g)占混合气体体积的40%,则下列说法不正确的是(假设反应前后温度保持不变)
A. 平衡时压强是起始压强的15/14倍
B. 平衡时NH3的浓度为1 mol/L
C. 该过程中v(O2)=0.225 mol/(L·min)
D. 达平衡时消耗O2 1.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题:
(1)根据结构对有机物进行分类,有助于对其性质的掌握。
a.![]() b.
b.![]() c.
c.![]()
上述有机物与苯互为同系物是________(填字母代号),写出苯与液溴发生反应的化学方程式:_______________________________________。
(2)苯在一定条件下可与浓HNO3发生如下反应:C6H6+HO—NO2![]() C6H5-NO2+H2O,该反应的反应类型是____________________。
C6H5-NO2+H2O,该反应的反应类型是____________________。
(3)生活中常用食醋除去暖瓶内的水垢(主要成分是CaCO3),反应的化学方程式为2CH3COOH+CaCO3===(CH3COO)2Ca+CO2↑+H2O。通过这个事实,你得出醋酸与碳酸的酸性强弱关系是:醋酸________碳酸(填“>”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】巧妙的实验设计有助于更好地解决问题。下列装置不能达到实验目的的是
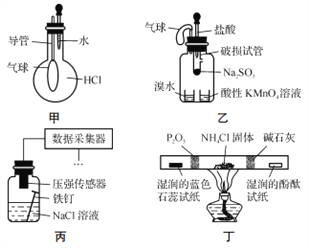
A. 用装置甲验证HCl气体易溶于水
B. 用装置乙验证SO2具有漂白性
C. 用装置丙采集到的压强数据判断铁钉发生析氢腐蚀还是吸氧腐蚀
D. 用装置丁检验NH4Cl分解产生的气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知298K时反应2SO2(g)+O2(g)═2SO3(g)△H=-197kJmol-1,在相同温度下向一密闭容器中加入2molSO2和1molO2,达化学平衡时放出热量为a1kJ;向另一容积相同的密闭容器中通入1molSO2和0.5molO2,达化学平衡时放出热量为a2kJ,则下列关系式中正确的是( )
A. 2a2>a1>197 B. 2a2<a1<197 C. 2a2=a1>197 D. 2a2=a1=197
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废液是用稀硝酸腐蚀锌板后得到的 ,某化学兴趣小组拟用该废液(含有少量的Cl-、Fe3+)制取Zn(NO3)2·6H2O的过程如下:
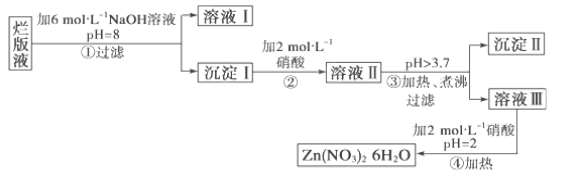
已知:Zn(NO3)2·6H2O是一种无色晶体,水溶液呈酸性,Zn(NO3)2能与碱反应,得到的产物Zn(OH)2具有两性,Fe3+在PH=3.7时就能完全沉淀。
(1)该废液溶质的主要成分是________(填化学式)。
(2)在操作①中保持pH=8的目的是______________________。
(3)沉淀Ⅰ的成分是___________________________。
(4)操作③中加热、煮沸的目的是________________________;
(5)操作④保持pH=2的目的是__________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从葡萄籽中提取的原花青素结构为:有关原花青素的下列说法不正确的( )
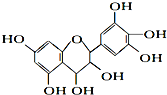
A.该物质既可看作醇类,也可看作酚类
B.1mol该物质可与4mol Br2反应
C.1mol该物质可与7mol Na反应
D.1mol该物质可与7mol NaOH反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com