
【题目】商代炼铜时,所用的矿物原料主要是孔雀石,主要燃料是木炭,在温度1000℃左右冶炼,可能涉及的反应有:
①Cu2(OH)2CO3![]() 2CuO+CO2↑+H2O;②2CuO+C
2CuO+CO2↑+H2O;②2CuO+C![]() 2Cu+CO2↑;③CuO+CO
2Cu+CO2↑;③CuO+CO![]() Cu+CO2;④CO2+C
Cu+CO2;④CO2+C![]() 2CO。
2CO。
(1)从四种基本反应类型来看,①②④的反应类型分别为①____________,②____________,④____________。
(2)从氧化还原反应的角度看,属于氧化还原反应的有____________。
(3)反应③中,____________发生氧化反应,__________发生还原反应。
(4)请在下图中用斜线表示反应③所属的区域。
 ;_______
;_______
【答案】分解反应 置换反应 化合反应 ②③④ CO CuO 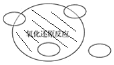
【解析】
⑴①Cu2(OH)2CO3![]() 2CuO+CO2↑+H2O是分解反应,无化合价变化,是非氧化还原反应,
2CuO+CO2↑+H2O是分解反应,无化合价变化,是非氧化还原反应,
②2CuO+C![]() 2Cu+CO2↑是置换反应,碳化合价升高,是氧化还原反应
2Cu+CO2↑是置换反应,碳化合价升高,是氧化还原反应
③CuO+CO![]() Cu+CO2中碳化合价升高,是氧化还原反应,
Cu+CO2中碳化合价升高,是氧化还原反应,
④CO2+C![]() 2CO是化合反应,碳单质中碳元素的化合价升高,是氧化还原反应,
2CO是化合反应,碳单质中碳元素的化合价升高,是氧化还原反应,
故答案为分解反应;置换反应;化合反应;
⑵从氧化还原反应的角度看,属于氧化还原反应的有②③④,
故答案为②③④;
③反应③中,一氧化碳中碳元素化合价升高发生氧化反应,氧化铜中铜元素化合价降低发生还原反应,
故答案为CO;CuO;
⑷③不属于四种基本反应类型,但是氧化还原反应,因此在图中
 ,
,
故答案为 。
。


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
【题目】金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制钠的工业方法,其反应原理是:2NaCl(熔融)![]() 2Na+Cl2↑。回答下列有关单质钠的问题:
2Na+Cl2↑。回答下列有关单质钠的问题:
(1)下列各项中属于保存金属钠的正确方法是____。
A.放在棕色瓶中 B.放在细沙中
C.放在水中 D.放在煤油中
(2)钠长时间放在空气中,最后的产物主要成分是____。
A.Na2O B.Na2O2 C.NaOH D.Na2CO3
(3)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应(如图Ⅰ所示),请写出该反应的化学方程式____________,生成物的颜色为____。将该试管冷却后直立,滴加几滴水(如图Ⅱ所示),发生反应的化学方程式为____________,检验该反应产生的气体的方法是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如下图所示(图中的ΔH表示生成1 mol产物的数据)。根据上图回答下列问题:
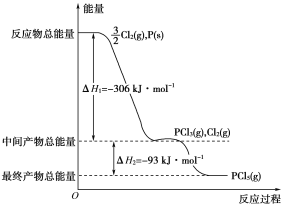
(1)P和Cl2反应生成PCl3的热化学方程式是__________________________
(2)PCl5分解成PCl3和Cl2的热化学方程式是_________________________
(3)P和Cl2分两步反应生成1 mol PCl5的ΔH3=________,P和Cl2一步反应生成1 mol PCl5的ΔH4______ΔH3(填“大于”“小于”或“等于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A.《化学与生活》
化学科学与材料、人体健康和环境保护等密切相关。
(1)践行“绿水青山就是金山银山”理念,实现人与自然和谐共生。
①下列做法会加剧雾霾天气的是_____(填字母)。
a.禁烧秸秆 b.潮汐发电 c.燃煤供暖
②下列污水处理的方法中只涉及物理方法的是_____(填字母)。
a.活性炭吸附法 b.氧化还原法 c.中和法
③下列措施不属于城市生活垃圾无害化处理的是_____(填字母)。
a.封闭式焚烧 b.露天堆放 c.卫生填埋
④处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S,发生反应的化学方程式为____________。
(2)营养均衡、合理用药是人体健康的保证。
现代医学研究表明,甘蔗中含有丰富的糖分、水分,此外,还含有对人体新陈代谢非常有益的各种维生素、脂肪、蛋白质、有机酸(苹果酸、柠檬酸)、氨基酸、钙、铁、磷、钾、铜、锌、镁、硒等物质。
①钙、锌、磷、钾元素中属于人体所需微量元素的是_____(填元素符号)。
②人体需要的营养素主要有糖类、油脂、蛋白质、无机盐、维生素和_____(填名称)。
③_____(填字母)能促进人体对Ca2+的吸收。
a.维生素A b.维生素C c.维生素D
④甘蔗中所含丝氨酸、赖氨酸为人体自身不能合成,该类氨基酸被称为_____ 氨基酸。
⑤苹果酸、柠檬酸属于_____(填字母)
a.酸味剂 b.甜味剂 c.着色剂
⑥以下药物可以治疗胃酸分泌过多的是_____(填字母)。
a.阿司匹林 b.泡腾片 c.复方氢氧化铝片
(3)创新发展材料推动人类社会的进步。2019年1月3日10时26分,由中国航天科技集团有限公司研制的嫦娥四号探测器成功着陆在月球背面预选着陆区。

①嫦娥四号探测器采用大量CFRP(碳纤维增强塑料)。CFRP属于_____(填字母)。
a.金属材料 b.无机非金属材料 c.复合材料
②嫦娥四号探测器的承力梁采用轻质钛合金构件。下列不属于钛合金性质的是_____(填字母)。
a.高强度 b.高密度 c.高韧性
③嫦娥四号探测器的飞行仪表板多采用有机玻璃材料。有机玻璃受热易熔化,易于加工成型,属于_____(填“热固性”或“热塑性”)塑料。
④机场建设需要大量的钢材、水泥、玻璃等建筑材料,其中生产水泥和玻璃所需的共同原料是_______(填化学式)
B.有机化学基础
⑴ 根据分子中所含官能团可预测有机化合物的性质。
① 分子中所有原子位于同一条直线上的是_____(填字母)。
a.乙烷 b.乙烯 c.乙炔
② 能发生水解反应的有机物是_____(填字母)。
a.CH3CH2Br b.CH3CH2OH c.葡萄糖
③ 鉴别苯与甲苯适宜的试剂是_____(填字母)。
a.水 b.KMnO4酸性溶液 c.NaOH溶液
④ 下列化合物中,能发生酯化反应的是_____(填字母)。
a.CH3CHO b.HCOOCH3 c.CH3OH
⑤ 能鉴别![]() 和
和![]() 两种物质的试剂是_____(填字母)。
两种物质的试剂是_____(填字母)。
a.FeCl3溶液 b.金属钠 c.饱和NaHCO3溶液
⑵自从四苯乙烯(TPE)的聚集诱导发光(AIE)现象被报道以来,这一与常规荧光分子聚集诱导荧光淬灭(ACQ)性质截然不同的特性引起了科研工作者的广泛兴趣。以下是TFE的一种合成路线(部分试剂及反应条件省略):

① A的名称是_____;B中官能团的名称是_____,D中官能团的名称是_____;
② B→C的反应类型为_____; E→F的化学方程式是_____。
③ W是D的同分异构体,具有下列结构特征:ⅰ.属于萘(![]() )的一元取代物;ⅱ.存在羟甲基(-CH2OH)。写出W的一种可能的结构简式:_____。
)的一元取代物;ⅱ.存在羟甲基(-CH2OH)。写出W的一种可能的结构简式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一化工厂以废铁屑为原料制备FeCl3溶液,用作印刷电路铜板腐蚀剂,并对溶液B进行电解处理的实验流程如图:

(1)试剂a应选用________(填写名称);
(2)步骤Ⅰ用到的主要玻璃仪器有漏斗、________(填写仪器名称);
(3)写出步骤Ⅱ中主要反应的化学方程式____________________;
(4)实验室制取气体E的离子方程式是________________________,欲对气体E进行干燥和吸收,需选用下列装置中的________(填写序号);

(5)如何用化学方法检验气体E?______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 代表阿伏加德罗常数的值。下列说法正确的是( )
代表阿伏加德罗常数的值。下列说法正确的是( )
A. 2.24L水蒸气与足量的![]() 反应,生成氧气的分子数为0.05
反应,生成氧气的分子数为0.05![]()
B. 常温常压下,3.6![]() 中所含的中子数为2
中所含的中子数为2![]()
C. 0.1mol淀粉[(C6H10O5)n]完全水解消耗的水分子数为0.1![]()
D. 将0.1mol![]() 溶于适量水,溶液中
溶于适量水,溶液中![]() 粒子总数为0.1
粒子总数为0.1![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯、丙烯等低碳烯烃是重要的基本化工原料,随着我国国民经济的发展,对低碳烯烃的需求日渐攀升。回答下列问题:
(1)MTP(甲醇制丙烯)工艺是目前重要的化工技术。主反应为![]()
![]() 。反应历程可按下列催化过程进行:
。反应历程可按下列催化过程进行:
![]()
![]() 则
则![]() =___________。
=___________。
(2)MTP工艺中存在等多个副反应。其他条件都相同时,在某催化剂的作用下,反应温度对甲醇转化率和产物选择性的影响如图所示。已知:
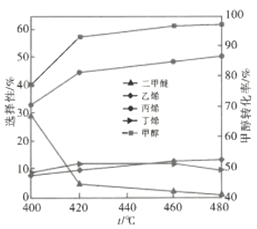
①主、副反应均为放热反应,且均为有水蒸气生成的气体分子数增加的反应
②选择性=(生成目的产物所消耗的原料量/转化掉的原料量)×100%
据图分析,若欲显著提高乙烯的选择性,不宜采取的措施是___________(填“改变温度”或“改变催化剂”);图中温度低于480℃时甲醇的转化率___________(填“是”或者“不是”)对应温度下的平衡转化率,判断理由是___________;下列措施中可提高甲醇平衡转化率的是___________(填标号)。
A.增大甲醇浓度
B.减小压强
C.用干燥剂吸收水蒸气
D.减小反应的平衡常数
(3)恒容条件下,若反应温度为460℃,![]() 初始浓度为
初始浓度为![]() mol
mol![]() ,平衡转化率为
,平衡转化率为![]() ,丙烯的选择性为48.3%,水蒸气的平衡浓度为
,丙烯的选择性为48.3%,水蒸气的平衡浓度为![]() ,则丙烯的平衡浓度为_____________,主反应
,则丙烯的平衡浓度为_____________,主反应![]() 的平衡常数K(460℃)的计算式为___________。
的平衡常数K(460℃)的计算式为___________。
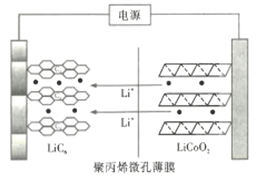
(4)丙烯可用于制备聚丙烯,聚丙烯微孔薄膜可用作锂离子电池的隔膜。某种锂离子电池充电时的示意图如图所示。![]() 中的
中的![]() 穿过隔膜向左迁移并嵌入石墨(用
穿过隔膜向左迁移并嵌入石墨(用![]() 表示)中。放电时
表示)中。放电时![]() 中的
中的![]() 又脱嵌向右迁移,则该电池放电时负极的电极反应式为___________。
又脱嵌向右迁移,则该电池放电时负极的电极反应式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验。
实验一 制取氯酸钾和氯水
利用如图所示的实验装置进行实验。

(1)制取实验结束后,取出B中试管冷却结晶,过滤,洗涤。该实验操作过程需要的玻璃仪器有______。
(2)若对调B和C装置的位置,_____(填“可能”或“不可能”)提高B中氯酸钾的产率。
实验二 氯酸钾与碘化钾反应的研究
(3)在不同条件下KClO3可将KI氧化为I2或KIO3。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
试管编号 | 1 | 2 | 3 | 4 |
0.20molL-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
6.0molL-1H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
实验现象 |
①系列a实验的实验目的是______。
②设计1号试管实验的作用是______。
③若2号试管实验现象是溶液变为黄色,取少量该溶液加入______溶液显蓝色。
实验三 测定饱和氯水中氯元素的总量
(4)根据下列资料,为该小组设计一个简单可行的实验方案(不必描述操作过程的细节):_____。
资料:①次氯酸会破坏酸碱指示剂;
②次氯酸或氯水可被SO2、H2O2和FeCl2等物质还原成Cl-。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0.01 mol的酸性混合溶液中加入0.01 mol铁粉,经搅拌后发生的变化应是 ( )
A. 铁溶解,析出0.01 mol Ag和0.005 mol Cu
B. 铁溶解,析出0.01 mol Ag并放出H2
C. 铁溶解,析出0.01 mol Ag,溶液中不再有Fe3+
D. 铁溶解,析出0.01 mol Ag,溶液中不再有Cu2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com