
��14�֣�ʪ����п��ұ�����̿�����ͼ���Ա�ʾ��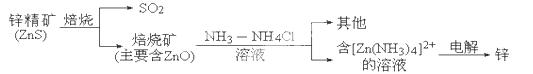
��ش��������⣺
��1����֪:N2(g)��2H2(g)===N2H4(l) ��H��a kJ��mol��1���÷�Ӧ�����Է����У���a 0(�����������������).
��2��ZnS���յķ�Ӧ2ZnS��3O2 2SO2��2ZnO���漰�������У�����������Ӧ�������� ���������Ӽ��Ļ������� .
2SO2��2ZnO���漰�������У�����������Ӧ�������� ���������Ӽ��Ļ������� .
��3��������������п�ĵ缫��ӦʽΪ___________________________.
��4��������SO2����Ba(NO3)2��Һ���գ����ֲ������Ϊ��ҵԭ�ϣ��䷴Ӧ�����ӷ���ʽΪ .
��5��п-���������﮵����ȣ����д�������ߡ��ɱ��͡�û�а�ȫ�������ŵ㡣�õ�ص��ܷ�ӦΪ2Zn��O2===2ZnO���������ҺΪKOH��Һ�����ĵ缫��ӦʽΪ ��25��ʱ���Ըõ��Ϊ��Դ����������������ͭ�����缫���500 mL 0.1mol/L CuSO4��Һ��һ��ʱ����жϵ�Դ���Ե缫���ﲢ������������缫��������Ϊ9.6 g����������Ҫ________L����(����ɱ�״��)����õ�ء�
��1��������2��ZnS��SO2����3��Zn[��NH3��4]2++2e-=Zn+4NH3����
��4��3SO2+3Ba2++2H2O+2NO3-=3BaSO4��+2NO��+4H+����5��Zn-2e-+2OH-=ZnO+H2O�� 4.2L��
���������������1�����ݻ�ѧ��Ӧ������оݦ�H��T��S���������ȵ��ؼ��ٵķ�Ӧ���κ������¶������Է����У��÷�Ӧ��һ���ؼ�С�ķ�Ӧ�����Ե��÷�ӦΪ���ȷ�Ӧ��a��0ʱ���÷�Ӧ���κ������¶������Է����У���2����������ԭ��Ӧ�У�ZnS����Ԫ�صĻ��ϼ��ɡ�2�����ߵ�0�ۣ�����������Ӧ�����ý����ͷǽ���Ԫ��֮���γɵĻ�ѧ�������Ӽ�����ZnS��ZnO��SO2���ڹ��ۻ����ֻ���й��ۼ�����3�������У�������Zn[��NH3��4]2+�������Ϸ����õ��ӵĻ�ԭ��Ӧ����ⷴӦʽΪ��Zn[��NH3��4]2++2e-=Zn+4NH3������4��������������������Ժ����ᱵ��Һ֮�䷢��������ԭ��Ӧ���õ���ɫ�������ᱵ��NO���壬���ӷ���ʽΪ3SO2+3Ba2++2H2O+2NO3-=3BaSO4��+2NO��+4H+����5����п-�������ԭ��صĸ������ǽ���п����ʧ���ӵ�������Ӧ���ڼ��Ի����£��缫��ӦʽΪ��Zn-2e-+2OH-=ZnO+H2O���Ըõ��Ϊ��Դ����������������ͭ�����缫���500mL 0.1mol/L CuSO4��Һ����������Cu-2e-=Cu2+����������Cu2++2e-=Cu���Ե缫���ﲢ������������缫��������Ϊ9.6g������ٵ�ͭ�����ɵ�ͭ����4.8g��0.075mol��ת�Ƶ�����0.15mol�����ݷ�Ӧ2Zn+O2�T2ZnO����ת�Ƶ�����4molʱ������������1moL������ת�Ƶ�����0.15molʱ������������0.0375moL����������ǿ����ἰ�����֮һ���������Ŀ����������0.0375moL��5��22.4L/mol=4.2L��
���㣺���黯ѧ��Ӧ������жϣ�������ԭ��Ӧ�����ӻ�������ۻ�����ĸ���绯ѧԭ����Ӧ�ã����ӷ���ʽ�͵缫��Ӧʽ����д��


 ���ʿ��ÿ��ֳɳ�ϵ�д�
���ʿ��ÿ��ֳɳ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��������Һ�У����и��������ܴ�����������ҺΪ��ɫ������
| A��Na+��K+��OH����Cl�� | B��Na+��Cu2+��SO42����NO3�� |
| C��Mg2+��Na+��SO42����Cl�� | D��K+��Na+��NO3����CO32�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�������ӷ���ʽ��д��ȷ����
| A�����⻯�Ƶ�ˮ�⣺HS����H2O === S2����H3O�� |
| B��Fe(OH)3�����������Fe(OH)3��3H��=== Fe3����3H2O |
| C����������������ʴ�ĸ�����Ӧʽ��O2��4e����2H2O === 4OH�� |
| D��̼�������Һ�е��������ռ���Һ��HCO3����OH��=== CO32����H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��6�֣�������з�Ӧ�����ӷ���ʽ��
��1����NaHSO4��Һ����μ���Ba(OH)2��Һ��ʹԭ��Һ�е�SO42��ǡ����ȫ������
��2����������Һ����μ���Ba(OH)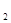 ��Һ����Al3+ǡ��ȫ������ʱ��
��Һ����Al3+ǡ��ȫ������ʱ��
��3����Ca(HCO3) 2��Һ�м��������NaOH��Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(14��)Na��Cu��O��Si��S��Cl�dz���������Ԫ�ء�
��1��Naλ��Ԫ�����ڱ��� ���ڵ� �壻S�Ļ�̬ԭ�Ӻ����� ��δ�ɶԵ��ӣ�Si�Ļ�̬ԭ�Ӻ�������Ų�ʽΪ ��
��2���á�����������գ�
| ��һ������ | ���Ӱ뾶 | �۵� | ���� |
| Si S | O2�� Na�� | NaCl Si | H2SO4 HClO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ij��ɫ��ҺX����Na+��Ag+��Ba2+��Al3+��[Al(OH)4]--�� MnO4����CO32-- ��SO42���е�������������ϣ�ȡ��Һ���������������飺���ѧ���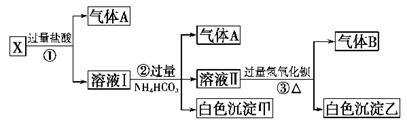
��1������A�ijɷ��ǣ�_________________������B�ijɷ���_____________
��2)X��Һ��һ�����ڵ������ǣ�____________________________
��3)д������ٷ�����Ӧ���������ӷ�Ӧ����ʽ��_________________________
��4��д��������γɰ�ɫ���������ӷ���ʽ��______________________
��5)д����ɫ�����ҵĿ�����ɣ�____________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��16�֣�±�����Ҫ�ɷ���MgCl2�������Fe2+��Fe3+��Mn2+���������ӡ���±��Ϊԭ�ϰ���ͼ��ʾ���̽������������Ƶ���������þ��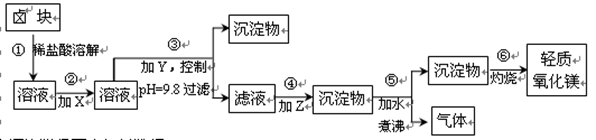
�������ϵ��±�������ݣ�
| ��1�� �����������������pH | ��2�� ԭ�ϼ۸�� | |||
| ���� | ��ʼ���� | ������ȫ | ���� | �۸�Ԫ/�֣� |
| Fe(OH)3 | 2.7 | 3.7 | a��ƯҺ����25.2%NaClO�� | 450 |
| Fe(OH)2 | 7.6 | 9.6�~ | b��˫��ˮ����30%H2O2�� | 2400 |
| Mn(OH)2 | 8.3 | 9.8 | c���ռ��98%NaOH�� | 2100 |
| Mg(OH)2 | 9.6 | 11.1 | d�������99.5%Na2CO3�� | 600 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�Ի�����(FeS2)�������ƺ�������Һ��Ϸ�Ӧ�Ʊ������������壬����ˮ���ջ�ö���������Һ���ڴ˹�������Ҫ�������˵��¶ȣ� ���¶Ȳ���������Ӧ���ӣ�Ӱ������ClO2����Ĵ��ȣ��һ�Ӱ��ClO2����������ʡ����������ͼ��ʾ����ش���������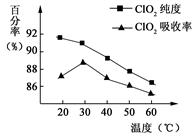
��1����ͼ��֪����Ӧʱ��Ҫ���Ƶ������¶��� �棬�ﵽ��Ҫ���ȡ�����˴�ʩ�� ��
��2����֪���������е���Ԫ�������������±�ClO3��������SO42����д���Ʊ��������ȵ����ӷ���ʽ�� ��
��3��ijУ��ѧѧϰС�����ԡ�m(ClO2)/m(NaClO3)����Ϊ����ClO2���ʵ�ָ�ꡣ��ȡNaClO3��Ʒ����6��0g��ͨ����Ӧ�����տɵ�400 mL ClO2��Һ��ȡ��20 mL������37��00 mL 0��500mol��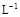 (NH4)2Fe(SO4)2 ��Һ��ַ�Ӧ������Fe2+����0��0500 mol��
(NH4)2Fe(SO4)2 ��Һ��ַ�Ӧ������Fe2+����0��0500 mol��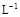 K2Cr2O7����Һ�ζ����յ㣬����20��00 mL����Ӧԭ�����£�
K2Cr2O7����Һ�ζ����յ㣬����20��00 mL����Ӧԭ�����£�
4H++ClO2+5Fe2+=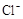 +5Fe3+ +2H2O 14H+ +
+5Fe3+ +2H2O 14H+ +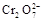 +6 Fe2+ =2Cr3+ + 6 Fe3+ +7H2O
+6 Fe2+ =2Cr3+ + 6 Fe3+ +7H2O
�Լ���ClO2�ġ����ʡ�����д��������̣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ʳ���к���һ������þ���������ʣ��ӵ����е����ʧ��Ҫ���������ʡ�ˮ�֡������е������Լ����ա����ȶ�����ġ���֪��
�����ԣ�IO3-��Fe3����I2����ԭ�ԣ�S2O32-��I��
3I2��6OH��=5I����IO3-��3H2O
KI��I2 KI3
KI3
(1)ijѧϰС��Լӵ��ν���������ʵ�飺ȡһ����ij�ӵ���(���ܺ���KIO3��KI��Mg2����Fe3��)������������ˮ�ܽ⣬����ϡ�����ữ����������Һ��Ϊ3�ݡ���һ����Һ�еμ�KSCN��Һ���Ժ�ɫ���ڶ�����Һ�м�����KI���壬��Һ�Ե���ɫ����CCl4��ȡ���²���Һ���Ϻ�ɫ����������Һ�м�������KIO3����μӵ����Լ�����Һ����ɫ��
�ټ�KSCN��Һ�Ժ�ɫ���ú�ɫ������ (�û�ѧʽ��ʾ)��CCl4�����Ϻ�ɫ�������� (�õ���ʽ��ʾ)��
�ڵڶ�����Һ�м�������KI�����Ӧ�����ӷ���ʽΪ �� ��
(2)KI��Ϊ�ӵ����ʳ���ڱ�������У����ڿ��������������ã�������������ʧ��д����ʪ������KI��������Ӧ�Ļ�ѧ����ʽ�� ��
��I2����KI��Һ���ڵ��������£����Ƶ�KI3��H2O����������Ϊʳ�μӵ���Ƿ���ʣ� (��ǡ���)����˵�����ɣ� ��
(3)Ϊ����ӵ���(����KI)���ȶ��ԣ��ɼ��ȶ������ٵ����ʧ�������������п�����Ϊ�ȶ������� ��
| A��Na2S2O3 | B��AlCl3 |
| C��Na2CO3 | D��NaNO2 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com