
【题目】关于由锌片、铜片和稀硫酸组成的原电池的说法中,正确的是 ( )
A.电解质溶液的pH保持不变
B.电流方向是由锌片流向铜片
C.锌片作正极,发生还原反应
D.锌片质量逐渐减少,铜片上有气泡产生
科目:高中化学 来源: 题型:
【题目】有关![]() 分子结构的下列叙述中,正确的是( )
分子结构的下列叙述中,正确的是( )
A. 除苯环外的其余碳原子有可能都在一条直线上 B. 所有的原子都在同一平面上
C. 12个碳原子不可能都在同一平面上 D. 12个碳原子有可能都在同一平而上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途具有对应关系的是
性质 | 用途 | |
A | 液氨气化吸热 | 可用作制冷剂 |
B | NH4HCO3受热易分解 | 可用作氮肥 |
C | 二氧化硅能与HF反应 | 可用作光导纤维 |
D | 二氧化硫能使溴水褪色 | 可用作漂白剂 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】六价铬[Cr(Ⅵ)]有剧毒,废水中的Cr2O![]() 常用铁氧磁体法除去,即把过量的FeSO4·7H2O加入含Cr2O
常用铁氧磁体法除去,即把过量的FeSO4·7H2O加入含Cr2O![]() 的废水中,调节pH<4,Fe2+将Cr(Ⅵ)还原为Cr3+。
的废水中,调节pH<4,Fe2+将Cr(Ⅵ)还原为Cr3+。
(1)写出上述Fe2+还原Cr2O![]() 的离子方程式,并标明电子转移的方向和数目:________________。
的离子方程式,并标明电子转移的方向和数目:________________。
(2)若调节溶液的pH为8~10,将析出相当于Fe(Ⅱ)[Fe(Ⅲ)xCr2-x]O4(磁性材料铁氧体)的沉淀,由此可确定x=_____________。
(3)Cr3+在过量的NaOH溶液中会转化为CrO![]() ,写出这一转化的离子方程式:______________,由此可知Cr(OH)3呈_________(选填“酸”、“碱”或“两”)性。
,写出这一转化的离子方程式:______________,由此可知Cr(OH)3呈_________(选填“酸”、“碱”或“两”)性。
(4)根据(2)的结果,若废水中Cr(Ⅵ)按CrO3计,欲除去废水中的Cr(Ⅵ),m(FeSO4·7H2O)∶m(CrO3)=___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组气体,经充分反应后,原来的气体有剩余的是 ( )
A.1molNH3和1molHCl混合
B.1molNO和0.5molO2混合
C.1molSO2和1molH2S混合
D.等体积的NO和NO2被足量烧碱溶液吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作:
A.在天平上准确称取烧碱样品wg,在烧坏中加蒸馏水溶解
B.在250mL容量瓶中定量成250mL烧碱溶液
C.用移液管移取25.00 mL烧碱溶液于锥形瓶中并滴加几滴甲基橙指示剂
D.将物质的量浓度为 Cmol/L 的标准盐酸 溶液装入酸式滴定管,调整液面,记下开始刻度数为Vml
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点耗酸体积 V1ml
回答下列问题:
(1)操作中的雏形瓶下垫一张白纸的作用是__________________。
(2)操作中液面应调整到零刻度或零刻度以下(稍下)的某一刻度,尖嘴部分应___________。
(3)滴定终点时锥形瓶内溶液颜色变化是__________。
(4)若酸式滴定管没有用标准 润洗,会对测定结果有何影响_____________(填偏高、偏低或无影响,其他操作均正确)。
(5)该烧碱样品的纯度计算式是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列有机物中,经催化加氢后不能生成2-甲基戊烷的是
A.CH3C(CH3)=CHCH2CH3 B.CH2=C(CH3)CH2CH2CH3
C.CH3CH=CHCH(CH3)CH3 D.CH2=CHCH(CH3)CH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除去杂质的方法正确的是( )
①除去乙烷中少量的乙烯:催化剂条件下通入H2
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液、干燥、蒸馏;
③除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶;
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏。
A.①② B.②④ C.③④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
实验一 焦亚硫酸钠的制取
采用下图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2=Na2S2O5
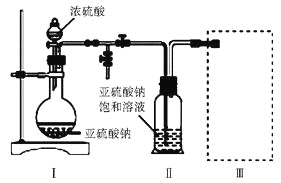
(1)装置Ⅰ中产生气体的化学方程式为____________________________。
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是____________。
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为______(填字母)。
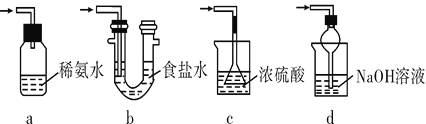
实验二 焦亚硫酸钠的性质
Na2S2O5溶于水即生成NaHSO3。
(4)证明NaHSO3溶液中HSO![]() 的电离程度大于水解程度,可采用的实验方法是________(填字母)。
的电离程度大于水解程度,可采用的实验方法是________(填字母)。
a.测定溶液的pH
b.加入Ba(OH)2溶液
c.加入盐酸
d.加入品红溶液
e.用蓝色石蕊试纸检测
(5)检验Na2S2O5晶体在空气中已被氧化的实验,是检验__________的存在(填离子符号)。
实验三 葡萄酒中抗氧化剂残留量的测定
(6)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:
(已知:滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI)

①按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为____________g·L-1。
②在上述实验过程中,若有部分HI被空气中氧化氧化,则测得结果________(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com