
【题目】现代传感信息技术在化学实验中有广泛的应用。某小组用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理![]() 如图所示
如图所示![]() ,并测定电离平衡常数Kb.
,并测定电离平衡常数Kb.
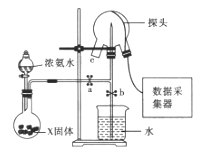
(1)实验室可用浓氨水和X固体制取![]() ,X固体可以是_________;
,X固体可以是_________;
A.生石灰 ![]() 无水氯化钙
无水氯化钙 ![]() 五氧化二磷
五氧化二磷 ![]() 碱石灰
碱石灰
(2)检验三颈瓶集满![]() 的方法是________________________________________。
的方法是________________________________________。
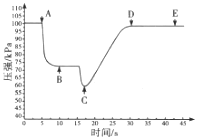
(3)关闭a,将带有装满水的胶头滴管的橡皮塞塞紧c口,______________,引发喷泉实验,电脑绘制三颈瓶内气压变化曲线如图所示。图中 ___点时喷泉最剧烈。
(4)从三颈瓶中用 ____________![]() 填仪器名称
填仪器名称![]() 量取20.00mL氨水至锥形瓶中,用0.05000mol/LHCl滴定。用pH计采集数据、电脑绘制滴定曲线并测定电离平衡常数Kb.
量取20.00mL氨水至锥形瓶中,用0.05000mol/LHCl滴定。用pH计采集数据、电脑绘制滴定曲线并测定电离平衡常数Kb.
【答案】![]() 将湿润的红色石蕊试纸靠近瓶口c,试纸变蓝色,证明
将湿润的红色石蕊试纸靠近瓶口c,试纸变蓝色,证明![]() 已收满或将蘸有浓盐酸的玻璃棒靠近瓶口c,有白烟生成,证明
已收满或将蘸有浓盐酸的玻璃棒靠近瓶口c,有白烟生成,证明![]() 已收满 打开b,挤压胶头滴管使水进入烧瓶 C 碱式滴定管或20mL移液管
已收满 打开b,挤压胶头滴管使水进入烧瓶 C 碱式滴定管或20mL移液管
【解析】
(1)实验室可用浓氨水和固体氢氧化钠或生石灰或碱石灰反应制取氨气;
(2)检验三颈瓶集满![]() 的操作规范答题;
的操作规范答题;
(3)使烧瓶内外形成压强差;
(4)准确量取液体可以用滴定管或20mL移液管。
(1)实验室可用浓氨水和固体氢氧化钠或生石灰或碱石灰反应制取氨气,故AD正确,
故答案为:AD;
(2)检验三颈瓶集满![]() 的操作是:将湿润的红色石蕊试纸靠近瓶口c,试纸变蓝色,证明
的操作是:将湿润的红色石蕊试纸靠近瓶口c,试纸变蓝色,证明![]() 已收满或将蘸有浓盐酸的玻璃棒靠近瓶口c,有白烟生成,证明
已收满或将蘸有浓盐酸的玻璃棒靠近瓶口c,有白烟生成,证明![]() 已收满,
已收满,
故答案为:将湿润的红色石蕊试纸靠近瓶口c,试纸变蓝色,证明![]() 已收满或将蘸有浓盐酸的玻璃棒靠近瓶口c,有白烟生成,证明
已收满或将蘸有浓盐酸的玻璃棒靠近瓶口c,有白烟生成,证明![]() 已收满;
已收满;
(3)关闭a,将带有装满水的胶头滴管的橡皮塞塞紧c口,打开b,挤压胶头滴管使水进入烧瓶,引发喷泉实验,进行喷泉实验时在瓶内压强最小的时候最剧烈,从图2中看出C点压强最小故C点最激烈,
故答案为:打开b,挤压胶头滴管使水进入烧瓶;C;
(4)准确量取液体可以用滴定管或20mL移液管,故可用碱式滴定管或20mL移液管,
故答案为:碱式滴定管或20mL移液管。


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
【题目】同温同压下两相同圆底烧瓶中分别充满①NH3,②NO2倒扣于水中进行喷泉实验,经充分反应后,瓶内溶液的物质的量浓度为
A. ①>② B. ①<② C. ①=② D. 不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中,反应aA(g)≒bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
A.平衡向正反应方向移动了B.物质A的转化率减少了
C.物质B的质量分数减小了D.a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作达不到预期目的是( )
![]() 用乙醇与3mol/L的H2SO4混合共热制乙烯;
用乙醇与3mol/L的H2SO4混合共热制乙烯;
![]() 将饱和食盐水滴入盛有电石的烧瓶中制乙炔;
将饱和食盐水滴入盛有电石的烧瓶中制乙炔;
![]() 将苯和溴水混合后加入Fe粉制溴苯;
将苯和溴水混合后加入Fe粉制溴苯;
![]() 分馏石油时将温度计的水银球位于蒸馏烧瓶的支管口处,实验室制乙烯则是伸入到混合液中;
分馏石油时将温度计的水银球位于蒸馏烧瓶的支管口处,实验室制乙烯则是伸入到混合液中;
![]() 制硝基苯时,应先加浓硝酸,再加浓硫酸,待液体冷却后再加苯;
制硝基苯时,应先加浓硝酸,再加浓硫酸,待液体冷却后再加苯;
![]() 将
将![]() 与NaOH的醇溶液共热制备CH3-CH=CH2
与NaOH的醇溶液共热制备CH3-CH=CH2
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是

A. 正极反应为AgCl +e-=Ag +Cl-
B. 放电时,交换膜右侧溶液中有大量白色沉淀生成
C. 若用NaCl溶液代替盐酸,则电池总反应随之改变
D. 当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷的价电子排布为 3s23p3,P 与 Cl 形成的化合物有 PCl3、PCl5,对此判断正确的是
A.磷原子最外层有三个未成对电子,故只能结合三个氯原子形成 PCl3
B.PCl3 分子是平面结构
C.PCl5 分子中的 P—Cl 键都是 π 键
D.磷原子最外层有三个未成对电子,但是能形成 PCl5,说明传统的价键理论存在缺陷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钨是熔点最高的金属,是重要的战略物资。自然界中黑钨矿石的主要成分是铁和锰的钨酸盐(FeWO4、MnWO4),还含少量Si、P的化合物。由黑钨矿冶炼钨的工艺流程如下图:
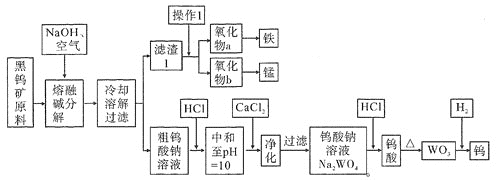
已知:
①滤渣1的主要成份是Fe3O4、MnO2。
②上述流程中,除最后一步外,其余步骤钨的化合价未变。
③常温下,钨酸难溶于水,钨酸钙(CaWO4)微溶于水。
回答下列问题:
⑴钨酸盐(FeWO4、MnWO4)中钨元素的化合价为________,为了加快黑钨矿在空气中熔融碱分解速率,可以采取_____________措施(写出其中一种即可)。
⑵请写出FeWO4在熔融条件下发生碱分解反应生成Fe3O4的化学方程式_________________________。
⑶操作1是工业上分离矿石的一种物理方法,此方法是_____________________________。上述流程中向粗钨酸钠溶液中加HCl调pH = 10后,溶液中的杂质阴离子为SiO32-、PO43-等,则“净化”过程中,加CaCl2的作用是____________________________________________。
⑷磷有两种同素异形体白磷和红磷,白磷有剧毒,不慎沾到皮肤上,可取少量胆矾配制成CuSO4溶液冲洗解毒。白磷可与热的CuSO4溶液反应生成Cu3P(Cu为+1价),反应方程式如下![]() 未配平
未配平![]() 。若反应中被氧化的P4的物质的量为1mol,则反应消耗的CuSO4的物质的量为________。
。若反应中被氧化的P4的物质的量为1mol,则反应消耗的CuSO4的物质的量为________。
CuSO4 + P4 + H2O = Cu3P + H2SO4+ H3PO4(未配平)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)可以制取多种化工试剂,以下为草酸钴晶体和氯化钴晶体的制备流程,回答下列问题:

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等.
②沉淀I中只含有两种沉淀。
③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表.
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中Co2O3发生反应的离子反应方程式为___________。
(2)NaClO3在浸出液中发生的离子反应方程式为_________________。
(3)加入Na2CO3调PH至5.2,目的是__________________________;萃取剂层含锰元素,则沉淀II的主要成分为_____________。
(4)操作I包括:将水层加入浓盐酸调整PH为2~3,___________、____________、过滤、洗涤、减压烘干等过程。
(5)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量硝酸酸化的硝酸银溶液,过滤、洗涤、干燥,测沉淀质量。通过计算发现粗产品中CoCl2·6H2O质量分数大于100%,其原因可能是____________________(回答一条原因即可)。
(6)将5.49g草酸钴晶体(CoC2O4·2H2O)置于空气中加热,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表.
温度范围/℃ | 固体质量/g |
150~210 | 4.41 |
290~320 | 2.41 |
经测定,整个受热过程,只产生水蒸气和CO2气体,则290~320℃温度范围,剩余的固体物质化学式为__。
[已知: CoC2O4·2H2O的摩尔质量为183g·mol-1]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,某可逆反应达到平衡,其平衡常数为K= ![]() ,恒容时,升高温度,H2的浓度减小,则下列说法正确的是
,恒容时,升高温度,H2的浓度减小,则下列说法正确的是
A.该反应的化学方程式为CO(g)+H2O(g) ![]() CO2(g)+H2(g)
CO2(g)+H2(g)
B.升高温度,K值减小
C.升高温度,逆反应速率减小
D.该反应的焓变为正值
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com