
����Ŀ����֪H2O2��KMnO4��NaClO��K2Cr2O7������ǿ�����ԡ�����Һ�е�Cu2����Fe2����Fe3������Ϊ�����������Һ��pH�ֱ�Ϊ6.4��9.6��3.7�����к�FeCl2���ʵ��Ȼ�ͭ����(CuCl2��2H2O)��Ϊ��ȡ������CuCl2��2H2O�����Ƚ����Ƴ�ˮ��Һ��Ȼ��ͼʾ��������ᴿ��
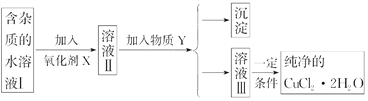
��ش��������⣺
(1)��ʵ�����ʺϵ�������X��________(�����)��
A��K2Cr2O7�������������� B��NaClO
C��H2O2 D��KMnO4
(2)����Y��________��
(3)��ȥFe3�����й����ӷ���ʽ��____________________��_______________________��
(4)����������Ŀ����____________________________________________��
(5)����ܲ���ֱ�������ᾧ�õ�CuCl2��2H2O���壿________��Ӧ��β�����_____��
���𰸡� C CuO[��Cu(OH)2��CuCO3��Cu2(OH)2CO3] Fe3����3H2O![]() Fe(OH)3��3H�� CuO��2H��===Cu2����H2O[��Cu(OH)2��2H��===Cu2����2H2O��] ��Fe2������ΪFe3�����������ɳ�������Cu2������ ���� Ӧ��HCl�����м�������
Fe(OH)3��3H�� CuO��2H��===Cu2����H2O[��Cu(OH)2��2H��===Cu2����2H2O��] ��Fe2������ΪFe3�����������ɳ�������Cu2������ ���� Ӧ��HCl�����м�������
��������(1)������������Ŀ���ǽ�Fe2+����ΪFe3+�������ܴ����µ����ʣ�����õ���������H2O2��H2O2����ԭ������H2O��û�д����µ����ʣ���K2Cr2O7��NaClO��KMnO4��������µ����ʣ��ʴ�ѡC��
(2)��Һ���е�����ΪFeCl3��CuCl2������ˮ��ʹ��Һ�������ԣ�ҪʹFe3+������Cu2+�������������������ӳ�����pH��ͬ����������Һ�м������CuO[��Cu(OH)2��CuCO3��Cu2(OH)2CO3]������Һ�����ȣ�ʹ��Һ��pH=3.7����ʱFe3+������Cu2+δ������ͬʱҲ��������µ����ʣ��ʴ�Ϊ����CuO[��Cu(OH)2��CuCO3��Cu2(OH)2CO3]��
(3)Fe3+����ˮ�ⷴӦ��Fe3����3H2O![]() Fe(OH)3��3H���������CuO��Cu(OH)2��ˮ��õ���H+��Ӧ����ʹˮ��ƽ�������ƶ�������Fe3+ȫ��ת��ΪFe(OH)3���������ӷ���ʽΪ��CuO��2H��===Cu2����H2O[��Cu(OH)2��2H��===Cu2����2H2O��]��
Fe(OH)3��3H���������CuO��Cu(OH)2��ˮ��õ���H+��Ӧ����ʹˮ��ƽ�������ƶ�������Fe3+ȫ��ת��ΪFe(OH)3���������ӷ���ʽΪ��CuO��2H��===Cu2����H2O[��Cu(OH)2��2H��===Cu2����2H2O��]��
(4)����������Ŀ���ǽ�Fe2+����ΪFe3+���ڽϵ͵�pH�¿���ʹFe3+��������Cu2+ ���룬��������Fe2+ ��Fe2+����ʱ��pHΪ9.6�����pH������Cu2+Ҳ��������������Cu2+���ʴ�Ϊ����Fe2������ΪFe3�����������ɳ�������Cu2�����롣
(5) CuCl2����ˮ�⣺CuCl2+2H2O![]() Cu(OH)2+2HCl��ˮ�ⷴӦΪ���ȷ�Ӧ��ֱ�Ӽ��������ᾧ��ƽ�������ƶ�����HCl���ӷ���Ҳ��ʹƽ�������ƶ����������ɵ���Cu(OH)2����������CuCl2��2H2O���壬��˱�������Cu2+��ˮ�⣬����ͨ��HCl����������������Ũ�ȣ�ʹƽ�������ƶ����Ӷ�����Cu2+��ˮ�����ʴ�Ϊ�����ܡ�Ӧ��HCl�����м���������
Cu(OH)2+2HCl��ˮ�ⷴӦΪ���ȷ�Ӧ��ֱ�Ӽ��������ᾧ��ƽ�������ƶ�����HCl���ӷ���Ҳ��ʹƽ�������ƶ����������ɵ���Cu(OH)2����������CuCl2��2H2O���壬��˱�������Cu2+��ˮ�⣬����ͨ��HCl����������������Ũ�ȣ�ʹƽ�������ƶ����Ӷ�����Cu2+��ˮ�����ʴ�Ϊ�����ܡ�Ӧ��HCl�����м���������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʯī˫���ӵ����һ��ȫ�µͳɱ�����Ч��ء�ԭ��Ϊ��A1Li+Cx(PF6)![]() Al+xC+Li++PF6-����ؽṹ��ͼ��ʾ������˵����ȷ����
Al+xC+Li++PF6-����ؽṹ��ͼ��ʾ������˵����ȷ����

A. �ŵ�ʱ�����·�е�������﮵缫�ƶ�
B. �ŵ�ʱ��������ӦΪCx(PF6)+e-=xC+PF6-
C. ���ʱ��Ӧ����ʯī�缫���Դ��������
D. ���ʱ������·��ͨ��1 mol���ӣ�������������9 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��������ʮ�����ʣ��� H2O���� �������� Mg���� H2SO4���� CaO���� CuSO4���� ��ơ��� Ca(OH)2���� �ƾ����� NaHCO3���������ڻ�������_____(����ţ���ͬ)���������������_________�����������_____�����ڼ����_________�������ε���_____��
(2)�û�ѧ������գ�
��ԭ�ӵĽṹʾ��ͼ_____��Na2O2����Ԫ�صĻ��ϼ�Ϊ_____��5�����������_____��
(3)NH4+��Ħ������Ϊ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ��Ĥ��ؿɳ�ȥ��ˮ�е������ƺͶ��ȱ��ӣ�![]() ������ԭ������ͼ��ʾ������˵����ȷ����
������ԭ������ͼ��ʾ������˵����ȷ����

A. BΪ��ص�������������ԭ��Ӧ
B. ���������B���ص��߾�С��������A��
C. A���ĵ缫��ӦʽΪ:![]()
D. �����·����0.2mole-ת��ʱ��A�������ӵ�H+����ĿΪ0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ��������ͷ���ijЩ����Ԫ�ػ�ѧ���ʵ�չ��
B. Na2O�����������ӵĸ�����Ϊ1��1
C. ���Ȼ�����Һ�м��������ˮ��Ӧ��ʵ����Al3����3NH3��H2O===Al(OH)3����3NH![]()
D. �������ʵ����������ƺ������Ʒֱ�Ͷ�뵽�����ҵ�������ˮ�У��õ��������������ֱ���a%��b%��������Һ����a��b�Ĺ�ϵ��a<b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���ˮ��˵������ȷ��
A. ���κ������£���ˮ��������
B. ���κ������£���ˮ��pH=7
C. ��95��ʱ����ˮ�� c��H+����l0��7mol/L
D. ��ˮ�м������� NaOH���壬ˮ�ĵ��������ƶ���c��OH��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������200mL MgCl2��AlCl3�Ļ��Һ������c��Mg2+��=0.2mol��L��1 ��c��Cl����=1.3 mol��![]() ��ҪʹMg2+ת����Mg��OH��2����ʹMg2+��Al3+���뿪����������Ҫ4 mol��L��1��NaOH��Һ
��ҪʹMg2+ת����Mg��OH��2����ʹMg2+��Al3+���뿪����������Ҫ4 mol��L��1��NaOH��Һ
A. 140mL B. 120mL C. 100mL D. 80mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС���о���������������ʱ���ı��ܱ�������ijһ������A2��g��+3B2��g��2AB3��g����ѧƽ��״̬��Ӱ�죬�õ���ͼ��ʾ�����ߣ�ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ����������ж���ȷ����
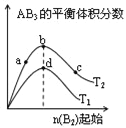
A. ͼ��T2һ������T1
B. ͼ��b������һ������d������
C. �ﵽƽ��ʱ��A2��ת���ʴ�СΪ��c��b��a
D. �����������ʹ״̬d��Ϊ״̬b
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com