
【题目】(1)现有下列十种物质:① H2O、② 空气、③ Mg、④ H2SO4、⑤ CaO、⑥ CuSO4、⑦ 碘酒、⑧ Ca(OH)2、⑨ 酒精、⑩ NaHCO3,其中属于混合物的是_____(填序号,下同),属于氧化物的是_________,属于酸的是_____,属于碱的是_________,属于盐的是_____。
(2)用化学用语填空:
氯原子的结构示意图_____;Na2O2中氧元素的化合价为_____;5个磷酸根离子_____;
(3)NH4+的摩尔质量为_____。
【答案】②⑦ ①⑤ ④ ⑧ ⑥⑩ 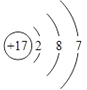
![]() 5PO43- 18g/mol
5PO43- 18g/mol
【解析】
(1)由两种或两种以上物质组成的是混合物,由两种元素组成,其中一种是氧元素的化合物是氧化物,溶于水电离出的阳离子全部是氢离子的化合物是酸,电离出的阴离子全部是氢氧根离子的化合物是碱,由金属阳离子或铵根离子与酸根离子组成的化合物是盐。
(2)根据氯元素的质子数以及核外电子排布分析;根据正负价代数和为0分析;离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其元素符号前加上相应的数字;
(3)根据摩尔质量和相对原子质量或相对分子质量的关系判断。
(1)①H2O是氧化物;②空气是混合物;③Mg是金属单质;④H2SO4是酸;⑤CaO是氧化物;⑥CuSO4是盐;⑦碘酒是混合物;⑧Ca(OH)2是碱;⑨酒精是有机物;⑩NaHCO3是盐。其中属于混合物的是②⑦,属于氧化物的是①⑤,属于酸的是④,属于碱的是⑧,属于盐的是⑥⑩。
(2)氯元素核电荷数是17,最外层电子数是7,则氯原子的结构示意图为 。Na2O2中钠元素是+1价,则根据正负价代数和为0可知氧元素的化合价为-1价;5个磷酸根离子可表示为5PO43-;
。Na2O2中钠元素是+1价,则根据正负价代数和为0可知氧元素的化合价为-1价;5个磷酸根离子可表示为5PO43-;
(3)NH4+的相对质量是18,所以其摩尔质量为18g/mol。


科目:高中化学 来源: 题型:
【题目】A、B、C、D都是中学化学中的常见物质,其中A、B、C均含有同一种元素,A是一种强碱,C为厨房中的用品,在—定条件下相互转化关系如图(部分反应中的水己略去)。下列有关B、C的说法正确的是

A. 可以用BaCl2或CaCl2稀溶液或Ba(OH)2稀溶液鉴别B、C两种溶液
B. 分别取等质量的B、C两种固体与等体积等浓度盐酸反应,产生气体的速率一样
C. 取agB、C的混合物充分加热,固体质量减重bg,由此可计算出混合物中B的质量分数
D. 取a gB、C的混合物与足量稀硫酸充分反应,逸出的气体碱石灰完全吸收,增重bg,由此可计算出混合物中B的质量分数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1×105Pa、298K时,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是( )
A.H2O(g) = H2(g) + 1/2O2(g) △H= +242kJ·mol-1
B.2H2(g) + O2(g) = 2H2O(l) △H= +484kJ·mol-1
C.H2(g) + 1/2O2(g) = H2O(g) △H= +242kJ·mol-1
D.2H2(g) + O2(g) = 2H2O(g) △H= +484kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各图示与对应的描述相符合的是

A. 图甲表示分别稀释pH=11的NaOH溶液和氨水时溶液pH的变化,图中b>a=100
B. 图乙表示某化学平衡的移动,在t1时改变的条件一定是加入催化剂
C. 图丙表示平衡2NO2(g)![]() N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化
N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化
D. 图丁表示CH3COOH溶液中通入NH3至过量的过程中溶液导电性的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要 0.5mol·L-1 的 NaOH 溶液 480mL,现欲配制此溶液,有以下仪器:①烧杯② 100mL 量筒 ③100mL 容量瓶④胶头滴管⑤玻璃棒⑥托盘天平(带砝码)⑦药匙
(1)配制时,必须使用的仪器有__(填代号),还缺少的仪器是 。该实 验中两次用到玻璃棒,其作用分别是_________________,__________________ 。
(2)配制溶液时,一般可以分为以下几个步骤: ① 称量、②计算、 ③溶解、 ④倒转摇匀、⑤ 转移、⑥洗涤、⑦定容、⑧冷却,其正确的操作顺序为__(用序号填 空),其中在①操作中需称量 NaOH 的质量为______________g。
(3)下列操作结果会使溶液的物质的量浓度偏低的是_________。
A.没有将洗涤液转入容量瓶中
B.称量时用了生锈的砝码
C.定容时,俯视容量瓶的刻度线
D.定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度
(4)若某学生用托盘天平称量药品时,在托盘天平左盘放有 20g 砝码,天平达平衡时游码的位置如图,则该同学所称量药品的实际质量为_________g。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于SO2的叙述中,正确的是( )
A.SO2的摩尔质量是64g
B.1molSO2中所含分子数约为6.02×1023
C.1molSO2的质量是64g/mol
D.常温常压下,1mol SO2的体积为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性。将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,需溶液的pH分别为6.4、9.6、3.7。现有含FeCl2杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按图示步骤进行提纯:
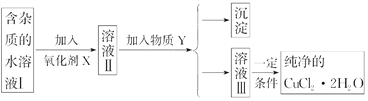
请回答下列问题:
(1)本实验最适合的氧化剂X是________(填序号)。
A.K2Cr2O7 B.NaClO
C.H2O2 D.KMnO4
(2)物质Y是________。
(3)除去Fe3+的有关离子方程式是____________________、_______________________。
(4)加氧化剂的目的是____________________________________________。
(5)最后能不能直接蒸发结晶得到CuCl2·2H2O晶体?________,应如何操作?_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构如图所示,下列说法正确的是
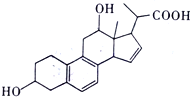
A. 该有机物的分子式为C21H24O4
B. 该有机物共有四种官能团,分别是:羟基、羧基、苯环、碳碳双键
C. 该有机物最多消耗NaOH与NaHCO3的物质的量比为1:1
D. 1mol 该有机物与足量金属钠反应,生成33.6L氢气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com