
【题目】下列说法或表示法正确的是
A.若反应2AB(g)C(g)+3D(g)在高温下能自发进行,其逆反应在低温下能自发进行,则该正反应的H<0、S>0
B.在101KPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,则表示氢气燃烧热的热化学方程式为2H2(g)+O2(g)=2H2O(l) H=-571.6kJ/mol
C.一定条件下,反应2SO2(g)+O2(g)=2SO3(g)H<0达到平衡后,升高体系温度反应重新达到平衡前,有2v正(O2)>v逆(SO3)
D.酸与碱恰好完全反应生成正盐的c(H+)=c(OH-)=10-6mol/L的溶液一定呈中性
科目:高中化学 来源: 题型:
【题目】已知2H2O2(1)=2H2O(1)+O2(g)反应过程中的能量变化曲线如图所示,下列说法不正确的是

A. 该反应的△H<0,△S>0
B. 途径Ⅱ与途径I相比,可能是加了催化剂
C. 其他条件相同时,产生相同体积的氧气时放出的热量:途径I >途径Ⅱ
D. 其他条件相同时,产生相同体积的氧气所需的时间:途径I>途径Ⅱ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CoCl2·6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2·6H2O的工艺流程如下:

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②酸性条件下,ClO3-不会氧化Co2+,ClO3-转化为Cl-;
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
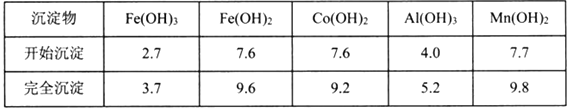
④CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶生成无水氯化钴。
请回答:
(1)“加Na2CO3调pH至5.2”,过滤所得到的沉淀Ⅹ成分为___________。
(2)萃取剂对金属离子的萃取率与pH的关系如图所示,萃取剂使用的适宜pH范围是___________。(填选项序号字母)
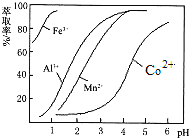
A 1.0~2.0 B 2.5~3.5 C 4.0~5.0
(3)为测定粗产品中CoCl2·6H2O含量,称取2g的粗产品溶于水,配成100mL溶液,取出20mL置于锥形瓶,加入K2CrO4做指示剂( Ag2CrO4为砖红色沉淀),用0.2mol/L的AgNO3溶液滴定至终点,重复2-3次,平均消耗AgNO3标准溶液10.00mL。该粗产品中CoCl2·6H2O的质量分数为___________。用K2CrO4做指示剂时,需要控制溶液pH值为6.5~10.5,试分析原因______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(亚硝酸钠(NaNO2)是工业盐的主要成分,在漂白、电镀等方面应用广泛。实验室利用下图装置制备亚硝酸钠,并测定所制亚硝酸钠的纯度。(加热装置及部分夹持装置已略去)
Ⅱ.亚硝酸钠纯度的测定。
当Na2O2完全反应后,E中产生的固体除NaNO2外,还可能有NaNO3。测定亚硝酸钠纯度的步骤如下:
步骤一:取反应后的固体4.30 g溶于稀硫酸,向所得溶液中加入足量KI,将溶液中的NO2-和NO3-全部还原为NO,并通入足量N2,将NO全部赶出,最后将溶液稀释至1000 mL。
步骤二:取上述所得溶液10 mL,用淀粉作指示剂,用0.050 mol/L的Na2S2O3标准液滴定,发生的反应为I2+2Na2S2O3=2NaI+Na2S4O6,最终消耗Na2S2O3溶液体积为16.00 mL。
(1)步骤二中达到滴定终点的标志为______________________。
(2)混合固体中NaNO2的质量分数为________。(保留三位有效数字)
(3)若在滴定终点读取滴定管刻度时,仰视标准液液面,则测得亚硝酸钠的纯度________。(填“偏高”“偏低”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组利用甲酸钠(HCOONa)制备Na2S2O4并测定产品的纯度,实验装置(夹持、加热仪器略)如图

将反应液分离提纯得到Na2S2O4产品,取产品mg溶于水,并定容为100mL,取25.00mL加入锥形瓶中,加入NaOH溶液及指示剂,用cmol·mol-1的K3[Fe(CN)6]标准溶液进行滴定{4K3[Fe(CN)6]+2Na2S2O4+8NaOH=3K4[Fe(CN)6]+4Na2SO3+Na4[Fe(CN)6]+4H2O},滴定至终点时,消耗标准液VmL。则产品的纯度为________(写出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠是一种高效氧化剂漂白剂,主要用于纸浆漂白、水处理等;工业上生产NaClO2有多种方法,某工业生产的流程如图所示:
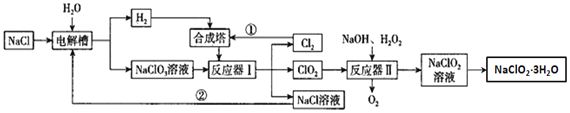
请回答下列问题:
为了测定NaClO2·3H2O的纯度,取上述合成产品10g溶于水配成500mL溶液,取出10mL溶液于锥形瓶中,再加入足量酸化的KI溶液,充分反应后加入2~3滴淀粉溶液,用0.264mol/LNa2S2O3标准液滴定,锥形瓶中溶液___(填颜色变化),且半分钟内不发生变化,说明滴定达终点,用去标准液20.00mL,试样纯度是否合格___(填“合格”或“不合格”,合格纯度在90%以上)。提示:2Na2S2O3+I2=Na2S4O6+2NaI。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 乳酸薄荷醇酯(![]() )仅能发生水解、氧化、消去反应
)仅能发生水解、氧化、消去反应
B. 乙醛和丙烯醛(![]() )不是同系物,它们与氢气充分反应后的产物也不是同系物
)不是同系物,它们与氢气充分反应后的产物也不是同系物
C. 淀粉和纤维素在酸催化下完全水解后的产物都是葡萄糖
D. CH3COOCH2CH3与CH3CH2COOCH3互为同分异构体,1H-NMR谱显示两者均有三种不同的氢原子且三种氢原子的比例相同,故不能用1H-NMR来鉴别
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将0.1000 mol·L-1盐酸滴入20.00 mL 0.100 0mol·L-1的某一元碱MOH溶液中,溶液的pH随加入盐酸体积变化曲线如下图所示。下列有关说法不正确的是( )

A.该一元碱的电离方程式为MOH = M++OH-
B.a、b、c三点中,b点水的电离程度最大
C.室温下,MOH的电离常数Kb=1×10-5 mol·L-1
D.b点:c (M+)=c (Clˉ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
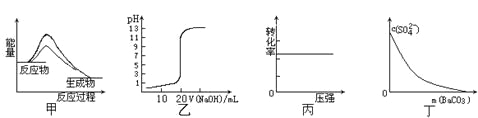
A.图甲表示使用催化剂后,该反应的ΔH变小
B.图乙表示0.10mol·L-1NaOH溶液滴定20.00mL0.10mol·L-1CH3COOH溶液所得到的滴定曲线
C.图丙表示反应H2(g) + I2(g)![]() 2HI(g)中H2的转化率随压强的变化
2HI(g)中H2的转化率随压强的变化
D.图丁表示在饱和Na2SO4溶液中逐步加BaCO3固体后,溶液中c(SO42-)的浓度变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com