
【题目】某短周期元素原子的次外层有8个电子,该元素可能是( )
A. O B. N
C. Mg D. C
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案科目:高中化学 来源: 题型:
【题目】镍在金属羰基化合物(金属元素和CO中性分子形成的一类配合物)、金属储氢材料(能可逆地多次吸收、储存和释放H2的合金)等领域用途广泛。
(1)基态Ni原子核外电子排布式为__________________________。
(2)Ni(CO)4中镍元素的化合价为__________,写出与CO互为等电子体的带一个单位正电荷的阳离子为:_______。Ni(CO)4的一氯代物有2种,其空间构型为_______________ o
(3)一种储氢合金由镍与镧(La)组成,其晶胞结构如图所示,则该晶体的化学式为_____________

(4)下列反应常用来检验Ni2+,请写出另一产物的化学式:_______________。

与Ni2+配位的N原子有__________个,该配合物中存在的化学键有_________(填序号)。
A.共价键 B.离子键 C.配位键 D.金属键 E.氢键
(5)Ni与Fe的构型相同(体心立方堆积),Ni的摩尔质量为M g/mol,阿伏加德罗常数为NA,密度为a g/cm3Ni原子的半径为_________pm(金属小球刚性相切)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的分离与提纯是化学实验研究常用的方法。下列混合体系分离提纯对应的方法不正确的是( )
选项 | A | B | C | D |
混合 体系 | 溴水 | 酒精与水 | 固体碘和氯化铵 | 混有少量KCl的KNO3粉末 |
分离 方法 | 萃取、分液 | 加生石灰,蒸馏 | 加热 | 配成热的饱和溶液,降温结晶 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①20g NaOH溶于水形成500mL溶液,所得溶液的物质的量浓度是_________mol/L。
②标准状况下,44.8LNH3溶于水形成1L溶液,所得溶液的物质的量浓度是_____mol/L。
③配制500mL 0.5 molL-1的盐酸,需要标准状况下的HCl气体多少_____升?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了保护环境,充分利用资源,可将工业废弃物转变成重要的化工原料。
请回答下列问题:
(1)可用NaClO3氧化酸性FeCl2废液得到FeCl3,FeCl3具有净水作用,但腐蚀设备。
①写出NaClO3氧化酸性FeCl2的离子方程式:__________________________。
②若酸性FeCl2废液中:c(Fe2+)=2.0×10-2 mol∕L,c(Fe3+)=1.0×10-3 mol∕L,c(Cl-)=5.3×10-2 mol∕L,则该溶液的pH约为_________。
③FeCl3净水的原理是:_________________(用离子方程式及适当文字回答);FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是_________(用离子方程式表示)。
(2)可用废铁屑为原料,按下图的工艺流程制备聚合硫酸铁(PFS),PFS是一种新型的
絮凝剂,处理污水比FeCl3高效,且腐蚀性小。
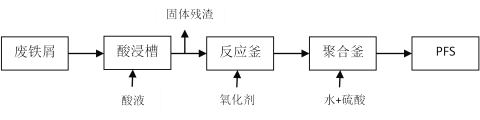
①酸浸时最合适的酸是______________。
②反应釜中加入的氧化剂,下列试剂中最合适的是____________(填标号)。
a.HNO3 b.KMnO4 c.Cl2 d.H2O2
检验其中Fe2+是否完全被氧化,应选择____________________(填标号)。
a.K3[Fe(CN)6]溶液 b.Na2SO3溶液 c.KSCN溶液
③生成PFS的离子方程式为:xFe3++yH2O Fex(OH)y(3x-y)++yH+欲使平衡正向移动可采用的方法是____________(填标号)。
a.加入NaHCO3 b.降温 c.加水稀释 d.加入NH4Cl
(3)废铁屑在一定条件下,可制得FeS2(二硫化亚铁)纳米材料,该材料可用于制造高容量锂电池,电池放电时的总反应为4Li+FeS2=Fe+2Li2S,维持电流强度为1A,a电池工作1小时,理论上消耗FeS2__________g。(已知1mol电子的电量为96500C)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2017江苏]某科研小组采用如下方案回收一种光盘金属层中的少量Ag(金属层中其他金属含量过低,对实验的影响可忽略)。

已知:①NaClO溶液在受热或酸性条件下易分解,如:3NaClO![]() 2NaCl+NaClO3
2NaCl+NaClO3
②AgCl可溶于氨水:AgCl+2NH3·H2O ![]() Ag(NH3) 2++ Cl +2H2O
Ag(NH3) 2++ Cl +2H2O
③常温时N2H4·H2O(水合肼)在碱性条件下能还原Ag(NH3)2+:
4Ag(NH3) 2++N2H4·H2O![]() 4Ag↓+N2↑+4
4Ag↓+N2↑+4![]() +4NH3↑+H2O
+4NH3↑+H2O
(1)“氧化”阶段需在80℃条件下进行,适宜的加热方式为__________________。
(2)NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,该反应的化学方程式为________________。 HNO3也能氧化Ag,从反应产物的角度分析,以HNO3代替NaClO的缺点是_____________________。
(3)为提高Ag的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并_______________________。
(4)若省略“过滤Ⅰ”,直接向冷却后的反应容器中滴加10%氨水,则需要增加氨水的用量,除因过量NaClO与NH3·H2O反应外(该条件下NaClO3与NH3·H2O不反应),还因为_________________。
(5)请设计从“过滤Ⅱ”后的滤液中获取单质Ag的实验方案:________________________(实验中须使用的试剂有:2 mol·L1水合肼溶液,1 mol·L1H2SO4)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.10 g 46%的乙醇水溶液中所含氢原子数目为1.2NA
B.标准状况下,2.24 L氯气溶于水发生反应,转移的电子数目为0.1NA
C.石墨电极电解CuSO4 溶液,阴极上有4 mol电子转移,阴极上有NA个O2
D.25 ℃时,100 mL pH=13的Ba(OH)2溶液中OH的数目为0.02NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com