
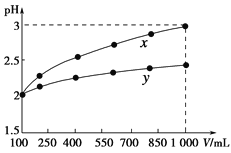
【题目】pH=2的两种一元酸x和y,体积均为100 mL,稀释过程中pH与溶液体积的关系如下图所示。分别滴加NaOH溶液(c=0.1 mol·L-1)至pH=7。消耗NaOH溶液的体积为Vx、Vy则( )
A.x为弱酸,Vx<VyB.x为强酸,Vx>Vy
C.y为弱酸,Vx<VyD.y为强酸,Vx>Vy
【答案】C
【解析】
由图可知,pH=2的两种一元酸x和y,均稀释10倍,x的pH为3,y的pH<3,则x为强酸,y为弱酸;发生中和反应后pH=7,为中性,x与NaOH反应生成不水解的正盐,而y与NaOH反应生成水解显碱性的正盐,且酸的物质的量越大消耗NaOH越多,以此来解答。
由图可知,pH=2的两种一元酸x和y,均稀释10倍,x的pH为3,y的pH<3,则x为强酸,y为弱酸;pH=2的x,其浓度为0.01mol/L,与NaOH发生中和反应后pH=7,为中性,则0.01mol/L×0.1L=0.1mol/L×V碱,解得V碱=0.01L,而pH=2的y,其浓度大于0.01mol/L,若二者恰好生成正盐,水解显碱性,为保证溶液为中性,此时y剩余,但y的物质的量大于x,y消耗的碱溶液体积大,体积大于0.01L,则Vx<Vy;
故选:C。


科目:高中化学 来源: 题型:
【题目】由以下粒子结构示意图得出的结论正确的是( )

A.④表示的是阳离子
B.①③属于同种元素,②④属于同种元素
C.②④形成的化合物是Al2O3
D.①③的化学性质相似
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将11.2g铜粉和镁粉的混合物分成两等份,其中一份加入200mL的稀硝酸中并加热,固体和硝酸恰好完全反应,并产生标准状况下的NO气体2.24L;将另一份在空气中充分加热,最后得到mg固体。下列有关说法:①c(HNO3)=2mol·L-l ②c(HNO3)=0.5mol·L-l ③m=8.0 ④m=7.2。其中正确的是( )
A.①④B.①③C.②④D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(![]() )是一种新型、高效、多功能水处理剂,且不会造成二次污染。
)是一种新型、高效、多功能水处理剂,且不会造成二次污染。
查阅资料:
①![]() 为紫色固体,微溶于
为紫色固体,微溶于![]() 溶液,具有强氧化性,在酸性或中性溶液中快速产生
溶液,具有强氧化性,在酸性或中性溶液中快速产生![]() ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。
②![]() 与
与![]() 溶液在20℃以下反应生成
溶液在20℃以下反应生成![]() ,在较高温度下则生成
,在较高温度下则生成![]() 。
。
(1)实验室常利用氯气制备![]() 后与
后与![]() 、
、![]() 反应制备
反应制备![]() 。根据下列仪器,请你组装合理、简洁的实验装置,所用装置的接口连接顺序是________。
。根据下列仪器,请你组装合理、简洁的实验装置,所用装置的接口连接顺序是________。



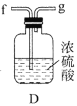


(2)写出装置A中发生反应的离子方程式________。
(3)三颈烧瓶用冰水浴的原因是________,A处盛放![]() 的仪器名称是________。
的仪器名称是________。
(4)将实验得到的![]() 再加入饱和
再加入饱和![]() 溶液中,可析出紫黑色的
溶液中,可析出紫黑色的![]() 粗晶体,其原因是________。
粗晶体,其原因是________。
(5)用滴定法测定所制粗![]() 的纯度(杂质与
的纯度(杂质与![]() 不反应):取
不反应):取![]() 粗
粗![]() 样品,加入足量硫酸酸化的
样品,加入足量硫酸酸化的![]() 溶液,充分反应后,用
溶液,充分反应后,用![]() 标准溶液滴定生成的I2,滴定消耗标准溶液的体积为
标准溶液滴定生成的I2,滴定消耗标准溶液的体积为![]() 。涉及的反应有:
。涉及的反应有:![]() ,
,![]() 。
。
①滴定时选用的指示剂是________,滴定终点的现象是________。
②制得粗![]() 的纯度是________。
的纯度是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若室温下0.1mol·L-1NaX溶液中pH=9,则该溶液中发生水解反应的X-占全部X-的( )
A.0.01%B.0.09%C.1.0%D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据所学化学反应原理,解决以下问题:
(1)依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池,可以提供稳定的电流.装置如图所示,其中盐桥中装有琼脂-饱和KCl溶液。
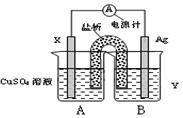
回答下列问题:
①电极X的材料和电解质溶液Y分别为________、________;
②盐桥中K+移向________(填A或B);
③银电极发生的电极反应式为________;
④该电池工作时,假设电路中有0.1mol电子转移,则X电极质量改变量为________克。
(2)已知:C(s)+O2(g)═CO2(g) △H1=-396.5kJmol-1;
H2(g)+![]() O2═H2O(g) △H2=-241.8kJmol-1;
O2═H2O(g) △H2=-241.8kJmol-1;
CO(g)+![]() O2(g)═CO2(g) △H3=-283.0kJmol-1.
O2(g)═CO2(g) △H3=-283.0kJmol-1.
根据盖斯定律写出单质碳和水蒸气生成水煤气的热化学方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】富硼渣中含有镁硼酸盐(2MgO·B2O3)、镁硅酸盐(2MgO·SiO2)及少量Al2O3、FeO 等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸(H3BO3)晶体的一种工艺流程如下:
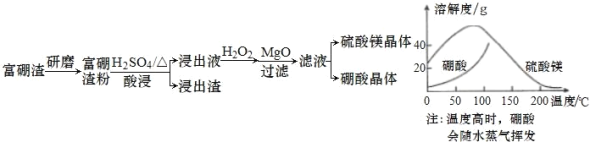
为了获得晶体,会先浓缩溶液接近饱和,然后将浓缩液放入高压釜中,控制温度进行结晶(硫酸镁与硼酸溶解度随温度的变化如图)。下列说法错误的是
A.该工艺流程中加快反应速率的措施有 2 种
B.在高压釜中,先降温结晶得到硼酸晶体,再蒸发结晶得到硫酸镁晶体
C.“酸浸”中镁硼酸盐发生反应2MgO·B2O3+2H2SO4+H2O![]() 2MgSO4+2H3BO3
2MgSO4+2H3BO3
D.加入“MgO”后过滤,所得滤渣主要是Al(OH)3 和Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用锂电池“固定![]() ”的电化学装置如图所示,在催化剂的作用下,该电化学装置放电时可将
”的电化学装置如图所示,在催化剂的作用下,该电化学装置放电时可将![]() 转化为
转化为![]() 和
和![]() ,充电时选用合适的催化剂,只有
,充电时选用合适的催化剂,只有![]() 发生氧化反应,释放出
发生氧化反应,释放出![]() 和
和![]() 。下列说法正确的是( )
。下列说法正确的是( )
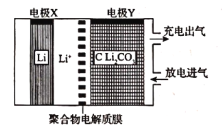
A.该电池放电时,![]() 向电极
向电极![]() 方向移动
方向移动
B.该电池充电时,每转移![]() 的电子,理论上阳极产生
的电子,理论上阳极产生![]()
C.该电池放电时,每转移![]() 电子,理论上有
电子,理论上有![]() 参加反应
参加反应
D.该电池充电时,阳极电极反应式为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com