
下列说法正确的是
A.润洗酸式滴定管时应从滴定管上口加入3~5mL所要盛装的酸溶液,倾斜着转动滴定管,使液体润湿其内壁,再从上口倒出,重复2~3次
B.向酒精灯内添加酒精时,不能多于容积的2/3,若不慎洒出的酒精在桌上燃烧,应迅速用水灭火
C.探究温度对反应速率的影响时,应先将硫代硫酸钠溶液、硫酸溶液分别在水浴中加热,然后混合
D.在“金属析氢腐蚀”实验中,外面缠绕着铜丝的铁钉上产生气泡多,在铁钉周围出现血红色现象(溶液中滴加几滴KSCN溶液)
科目:高中化学 来源:2014-2015江苏省扬州市高二上学期期末化学(必修)试卷(解析版) 题型:选择题
以下食品中的有机成分属于高分子化合物的是
A.谷类中含有的淀粉 B.植物油、动物脂肪中含有的油脂
C.食醋中含有的醋酸 D.酒中含有的酒精
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省新余市高一上学期期末考试化学试卷(解析版) 题型:实验题
如图中,A是氯气的发生装置,B、C是净化气体的装置,B装置中装有饱和食盐水,D中装铁丝网;反应后E的底部有棕色固体聚集;F是吸收多余气体的装置。

(1)上述装置中有一处错误,请指出是 处(用字母表示)。
(2)B装置的作用是 ,C装置中需要加入 。
(3)写出A中发生反应的离子方程式 ,写出D中发生反应的化学方程式 。
(4)如果A中产生氯气3.36L(标准状况),请计算:被氧化的HCl的物质的量 。
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省新余市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.向Al2(SO4)3溶液中加入过量的氨水:Al3++4NH3·H2O =AlO2—+ 4NH4++2H2O
B.铁与稀盐酸反应: 2Fe+6H+ = 2Fe3++3H2↑
C.氢氧化钡和稀硫酸: Ba2++2OH—+2H++SO42—=BaSO4↓+2H2O
D.将钠加入水中: Na+2H2O=Na++2OH—+H2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省六校高三3月联考理综化学试卷(解析版) 题型:选择题
已知某溶液中含有下列8种离子中的5种(忽略水的电离及离子的水解):K+、Cu2+、Al3+、Fe2+、Cl-、CO32-、NO3-、SO42-,且5种离子的物质的量浓度相等。为了进一步探究该水溶液的组成,某同学进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察无紫色火焰。
②另取溶液加入足量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
③另取溶液加入BaCl2溶液,有白色沉淀生成。
根据上述实验,以下推测正确的是
A.无法确定溶液中是否存在Cu2+离子
B.原溶液中不含K+、Al3+、CO32-等离子
C.根据步骤②只能确定溶液中一定存在NO3-离子
D.步骤③所得到的白色沉淀共有2种钡盐
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省遂宁市高三第二次诊断考试化学试卷(解析版) 题型:填空题
(14分)A、B、C、D、E、F为前四周期原子序数依次增大的非稀有气体元素。其中:A的一种单质是自然界最硬的物质;B与A同周期且基态原子中s能级与p能级上的电子数相等;C于B同主族;D为同周期电负性最大的元素;E为使用最为广泛的金属;F的基态原子中没有单电子。请回答下列有关问题:
(1)写出E的基态原子的价层电子排布式 ;
(2)AB2的水化物中A的杂化方式为 ,CD2的空间构型为 ;
(3)K3[E(CN)6](此处C为碳元素符号)中配位数为 ,配体的电子式为 ;
(4)某矿石主要成分甲的晶胞如图,甲能与水反应,则甲的化学式为 ,属于 晶体;

(5)CD2与CB3可以合成广泛用于有机合成的化合物CBD2,同时得到另一种与臭氧互为等电子体的化合物,写出该反应的化学方程式 ;
(6)纳米颗粒E3B4在磁性录像带、磁性存储器、磁性光盘、铁氧体磁芯、波导管和变压器等方面应用广泛,制取该颗粒时,将0.3mol/L ESO4 的水溶液和0.4mol/L ECl3的水溶液以体积比2∶1进行混合。根据E3B4的组成分析按此用量混合可能的原因是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省遂宁市高三第二次诊断考试化学试卷(解析版) 题型:选择题
下列有关物质的性质和该性质的应用均正确的是
A.二氧化硫具有还原性,用二氧化硫水溶液吸收溴蒸气
B.氢氟酸具有强酸性,用氢氟酸蚀刻玻璃
C.氨气具有氧化性,用浓氨水检验Cl2管道是否泄漏
D.钠的金属性比钾强,工业上用钠制取钾(Na+KCl  K↑+NaCl)
K↑+NaCl)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省怀化市高三第一次模拟考试理综化学试卷(解析版) 题型:实验题
某实验小组用下图所示装置制备一硝基甲苯(包括对硝基甲苯和邻硝基甲苯)

反应原理:
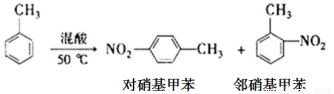
实验步骤:①浓硫酸与浓硝酸按体积比1:3配制混合溶液(即混酸)共40mL;
②在三颈瓶中加入13g甲苯(易挥发),按图所示装好药品和其他仪器;
③向三颈瓶中加入混酸;
④控制温度约为50℃-55℃,反应大约10min,三颈瓶底有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯,经提纯最终得到对硝基甲苯和邻硝基甲苯共15g。
相关物质的性质如下:
密度/g·cm-3 | 沸点/℃ | 溶解性 | |
甲苯 | 0.866 | 110.6 | 不溶于水 |
对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
(1)仪器A的名称是________。
(2)配制混酸的方法是 。
(3)若实验后在三颈瓶中收集的产物较少,可能的原因是: 。
(4)本实验采用水浴加热,水浴加热的优点是 。
(5)分离反应后产物的方案如下:

操作1的名称是 ,操作2中不需要用到下列仪器中的 。(填序号)
a.冷凝管
b.酒精灯
c.温度计
d.分液漏斗
e.蒸发皿
(6)本实验中邻、对硝基甲苯的产率为________(结果保留小数点后一位数字)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省泉州市高三3月月考理综化学试卷(解析版) 题型:选择题
四种短周期元素在周期表中的位置如图,其中X元素的原子最外层电子数等于其电子层数。下列说法不正确的是
Z | W | ||
X | Y |
A.X位于元索周期表中第3 周期、ⅢA族
B.原子半径:X > Z > W
C.最简单气态氢化物的热稳定性:W > Y
D.Y的最高价氧化物可以和W的最简单氢化物反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com