
| | | | | | | | |
| | | | A | D | | E | |
| | | G | | | J | L | |
科目:高中化学 来源:不详 题型:填空题

| 元素 | Na | Mg | Al | Si | P | S | Cl |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在周期表中位于第四周期、第VIA族 |
| B.单质可能做半导体材料 |
| C.金属性比同主族的铅强 |
| D.最高价氧化物对应的水化物是强酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.某元素原子最外层只有一个电子,则它一定是IA元素 |
| B.任何原子或离子的组成中都含有质子 |
| C.质子数相同的微粒一定属于同一种元素 |
| D.构成原子核的微粒中都含有中子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.Na+、Fe3+、Cl 、SCN 、SCN 能大量共存于同一溶液中 能大量共存于同一溶液中 |
B.碳酸氢钠溶液与足量的氢氧化钡溶液混合后,其离子方程式为:HCO3 + Ba2+ + OH + Ba2+ + OH ="=" BaCO3↓+H2O ="=" BaCO3↓+H2O |
C.若R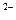 和M+的电子层结构相同,则原子序数的比较为:R>M 和M+的电子层结构相同,则原子序数的比较为:R>M |
D.若X原子中的质子数为a,中子数为b,则X的质量数为: |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题



查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 甲判断 | 乙判断 |
| A | 某化合物溶于水能导电 | 该化合物是电解质 |
| B | 某过程发生能量变化 | 该过程发生化学反应 |
| C | 钠原子核外电子数比铝少 | 钠的金属性比铝强 |
| D | 两种元素同一主族 | 两种元素的原子最外层电子数相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com