
����Ŀ������������FeCl3��Һ�ֱ�μӵ����������У��õ����ַ�ɢϵ�����������⣺
�ף�����FeCl3��Һ�μӵ���ˮ�У�
�ң�����FeCl3��Һ�μӵ�NaOH��Һ�У�
��������FeCl3��Һ�μӵ���ˮ�С�
��1����������������еõ����ɫ��Һ�壬��Ӧ�Ļ�ѧ����ʽΪ___________
��2������ķ����жϱ����Ƿ�ɹ��Ʊ����壬��д����صIJ���������ͽ���__________
��3���������ı�����μ���ϡ���ᣬ�����һϵ�б仯��
���ȳ��ֺ�������ͬ������ԭ��Ϊ_______________
��������仯�õ��ͼ���ͬ����Һ���˷�Ӧ�����ӷ�Ӧ����ʽΪ_______
��4������м���缫ͨ���_______����ɫ�������������������������
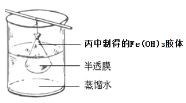
��5��������ͼ��ʾ��װ�ó�ȥFe��OH��3�����е������������ᴿFe��OH��3���壬ʵ��������費�ϸ����ձ��е�����ˮ����������ˮ���ɴκ�ȡ�����ձ��е�Һ�壬�����м���AgNO3��Һ����_______����ʵ��������˵����Fe��OH��3�����е����������Ѿ���ȫ��ȥ��
���𰸡�FeCl3+3H2O![]() Fe��OH��3�� ���壩+3HCl ǿ�����䣬���й�������ͨ·�����Ѿ��Ʊ��ɹ� ����Fe��OH��3������������ʻᷢ���۳�������γɺ��ɫ���� Fe��OH��3 +3H+ =Fe3++3H2O ���� �����ְ�ɫ����
Fe��OH��3�� ���壩+3HCl ǿ�����䣬���й�������ͨ·�����Ѿ��Ʊ��ɹ� ����Fe��OH��3������������ʻᷢ���۳�������γɺ��ɫ���� Fe��OH��3 +3H+ =Fe3++3H2O ���� �����ְ�ɫ����
��������
��1�������������������Ʊ�ԭ����д��ѧ��Ӧ����ʽ��
��2�����ݽ������ʼ�����������ԭ���������
��3�����ݽ�������ʼ�ʵ��������������д������ӷ���ʽ��
��4�����ݽ��������������������
��5������ͼʾװ�ü������Ӽ��鷽���������
��1��������Һ�μӵ���ˮ�У�����������еõ����ɫ��Һ��Ϊ�����������壬��Ӧ�Ļ�ѧ����ʽΪ��FeCl3+3H2O![]() Fe(OH)3�� ���壩+3HCl���ʴ�Ϊ��FeCl3+3H2O
Fe(OH)3�� ���壩+3HCl���ʴ�Ϊ��FeCl3+3H2O![]() Fe(OH)3�� ���壩+3HCl��
Fe(OH)3�� ���壩+3HCl��
��2��������ж����ЧӦ������жϱ����Ƿ�ɹ��Ʊ�����IJ�������ǿ�����䣬���й�������ͨ·�����Ѿ��Ʊ��ɣ��ʴ�Ϊ��ǿ�����䣬���й�������ͨ·�����Ѿ��Ʊ��ɹ���
��3�������ڽ�����������ʻᷢ���۳�������γɺ��ɫ�����������������������ᷢ����Ӧ�����Ȼ�����ˮ�������ܽ⣬�˷�Ӧ�����ӷ�Ӧ����ʽΪFe(OH)3 +3H+ =Fe3++3H2O���ʴ�Ϊ������Fe(OH)3������������ʻᷢ���۳�������γɺ��ɫ������Fe(OH)3 +3H+ =Fe3++3H2O��
��4��������������Ľ���������ɣ��������м���缫ͨ���������Ӧ�������������ʴ�Ϊ��������
��5����Ϊ�������������ӷ�Ӧ���ɰ�ɫ�Ȼ������������Ը�������ˮ���ɴκ�ȡ�����ձ��е�Һ�壬�����м�����Һ���������ְ�ɫ������˵���ý����е����������Ѿ���ȫ��ȥ��
�ʴ�Ϊ�������ְ�ɫ������


 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��W�ǵ�������Ԫ�أ���������������Ӧ��ˮ��������ˮ���õ�Ũ�Ⱦ�Ϊ0.010mol/L����Һ����pH��25�棩���ӦԪ��ԭ�Ӱ뾶�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ� ��

A. �����ӵİ뾶��X>Z>W
B. ����̬�⻯����ȶ��ԣ�Z>W>Y
C. Y���ʿ����������뵼�����
D. n =2-lg2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���ֳ�������A(�ؿ��к����ڶ��Ľ���)��B(��ɫ����)�ֱ���������X��Y������Ӧ����ת����ϵ��ͼ��ʾ������DΪ����ɫ���塣
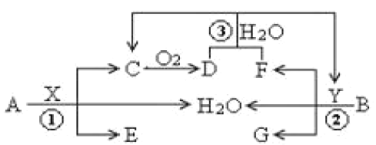
�ش��������⣺
��1����Ӧ�۵����ӷ�Ӧ����ʽΪ___��
��2��6.4gB�����X��Һ(8mol /L��60mL)��ַ�Ӧ�����ɵĻ�ԭ������C��D����Ӧ����Һ������XΪn mol ����ʱ��Һ������X�������ӵ����ʵ���Ϊ___mol��
��3��������A��Y��ϡ��Һ�ܷ�����Ӧ������W�����ڹ���W��ת����ϵ��ͼ��ʾ(����������ȥ)������N�Ǻ���ɫ�Ļ����
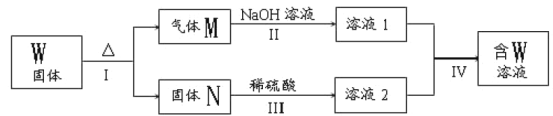
��M�����ֻ�������ɣ����к��Уƣ�����ͨ��BaCl2��Һ��ʵ��������___��
��������ӦI�õ�16 g����Σ�����������Mǡ�ñ�0.3L1mol��L��1 NaOH��Һ��ȫ���յ���Һ1����Ӧ���з�����Ӧ�����ӷ���ʽ��____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��Ϊ̽��������������ʣ�����ͼ��ʾװ�ý���ʵ�顣

��ش��������⣺
��1��װ��A��ʢ���������Ƶ�����������__________����Ӧ�Ļ�ѧ����ʽΪ_______________��
��2��װ��B�е�������__________________����Ӧ�����ӷ���ʽΪ_________________��
��3��װ��C�е�������____________________��������˵������������е�������________________________��
��4��װ��D��Ŀ����̽������������Ʒ�����õĿ����ԣ�д��ʵ�����������_____________��
��5��β���ɲ���__________��Һ���ա�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����mg Na������������ȼ�գ����ɹ��������Ϊ��m��3.55��g����mg Na��������Ӧ�����ɹ��������Ϊ��������
�٣�m��0.8��g���ڣ�m��1.0��g���ۣ�m��1.2��g���ܣ�m��1.6��g���ݣ�m��1.4��g
A.���٢�B.���٢�C.���ۢ�D.�٢ڢۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�ֺϳ�ijҩ���м���Z�ķ������¡�����˵����ȷ����
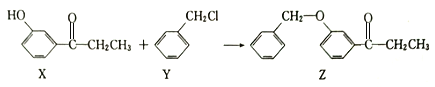
A. 1molX�����������ˮ�е�2molBr2 B. Y���Է�����ȥ��Ӧ
C. Z������̼ԭ�ӿ�����ͬһƽ�� D. ��FeCl3��Һ���Լ���Z���Ƿ����X
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С�����������װ�ã���֤������̼���������Ʒ�Ӧʱ��Ҫ��ˮ�Ӵ���
��װ�÷�����
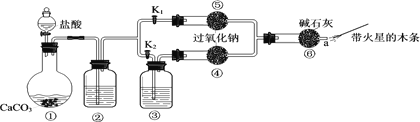
��1��װ�����з�Ӧ�����ӷ���ʽ��______��
��2��װ�â��е��Լ���______������ţ���
a������Na2CO3��Һ b������NaHCO3��Һ c��ŨH2SO4
��3��װ�â��е��Լ���______��
������ʵ�飩����1�����ɼ�K2���ر�K1����Һ©�������������ᣬ�������ǵ�ľ������a���� ����2�����ɼ�K1���ر�K2����Һ©�������������ᣬ�������ǵ�ľ������a����
��4������1�Ͳ���2�У�a�������ǵ�ľ��������ʵ������ֱ���______��
��5���������Ƹ�������̼��Ӧ�Ļ�ѧ����ʽ��______��
��ʵ�鷴˼��
��6����ͬѧ������ɣ�������ʵ�鲻����֤����ˮ����ʱ�������Ƹ�������̼�����˻�ѧ��Ӧ������������______��
��7����Ҫ�����ʵ������ǣ�ȡ���з�Ӧ����������壬______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�������ܶ�Ϊ1.25 gmL��1����������Ϊ36.5%��Ũ��������240 mL 0.1 molL��1�����ᣬ��ش��������⣺
��1��Ũ��������ʵ���Ũ��Ϊ________________________��
��2������240 mL 0.1 molL��1������
Ӧ��ȡŨ�������/mL | Ӧѡ������ƿ�Ĺ��/mL |
__________ | __________ |
��3������ʱ������ȷ�IJ���˳���ǣ�����ĸ��ʾ��ÿ����ĸֻ����һ�Σ�__________��
A����30 mLˮϴ���ձ��ڱںͲ�����23�Σ�ϴ��Һ��ע������ƿ����
B������Ͳ��ȷ��ȡ�����Ũ���������������ձ��У��ټ�������ˮ��Լ30 mL�����ò���������������ʹ���Ͼ���
C��������ȴ�������ز�����ע������ƿ��
D��������ƿ�ǽ�����ҡ��
E�����ý�ͷ�ιܼ�ˮ��ʹ��Һ��Һ��ǡ����̶�������
F������������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶���12 cm��
��4����ʵ�������������������������������ʵ���Ũ���к�Ӱ�죨�ƫ�ߡ���ƫ�͡����䡱��
������ϡ��������ձ�δϴ��__________________________________________��
������ƿ��ԭ����������ˮ____________________________________________��
�۶���ʱ���ӹ۲�Һ��________________________________________________��
��5����ʵ������г������������δ�����
�ٶ���ʱ������ˮʱ�����˿̶�________________________________________��
��������ƿ��ת����Һʱ��������Һ����________________________________��
�۶���ҡ�Ⱥ���Һ���½�____________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�����г�����NaCl��Na2SO4�����ʡ��о�С�����������ʵ��װ�ã�ͨ���������ᷴӦ���ɵ�m(CO2)���ⶨ����Ϊm gij��ҵ����Ĵ��ȣ�����������ȷ����
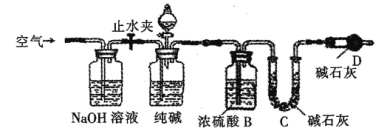
A.ͨ��������Ӧǰ��װ��B����������ȡm(CO2)
B.ͨ��������Ӧǰ��װ��C����������ȡm(CO2)
C.ͨ��������Ӧǰ��װ��C��D����������ȡm(CO2)
D.ͨ��������Ӧǰ��װ��D����������ȡm(CO2)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com