
【题目】对可逆反应 2A(s)+3B(g) ![]() C(g)+2D(g);ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
C(g)+2D(g);ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
A.加入催化剂,B的转化率提高
B.升高温度,平衡向逆反应方向移动,v(正)减小
C.压强增大一倍,平衡不移动,v(正)、v(逆)不变
D.恒温恒容充入 Ne,容器内压强增大,V(正)、V(逆)均不变
【答案】D
【解析】
A. 加入催化剂,反应速率加快,平衡不移动;
B. 该反应为放热反应,升高温度,平衡逆向移动;
C. 该反应为等体积反应,增大压强,反应速率加快,平衡不移动;
D. 充入Ne,容器内压强增大,但各物质浓度不变,平衡不移动。
A. 加入催化剂,反应速率加快,平衡不移动,B的转化率,A项错误;
B. 该反应为放热反应,升高温度,反应速率加快,平衡逆向移动,因此V(正)、V(逆)均增大,B项错误;
C. 该反应为等体积反应,增大压强, v(正)、v(逆) 均加快,但平衡不移动,C项错误;
D. 充入Ne,容器内压强增大,但各物质浓度不变,平衡不移动,V(正)、V(逆)均不变,D项正确;
答案选D。


科目:高中化学 来源: 题型:
【题目】在一定条件下,对于密闭容器中进行的反应:X(g) + Y(g)![]() 2Z(g),下列说法能充分说明该反应已达到化学平衡状态的是 ( )
2Z(g),下列说法能充分说明该反应已达到化学平衡状态的是 ( )
A.X、Y、Z的浓度相等B.正、逆反应速率均等于零
C.X、Y、Z在容器中共存D.X、Y、Z的浓度均不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学能在一定条件下可转化为电能。
(1)如图所示装置中锌片是______(填“正极”或“负极”),其电极反应式是______。溶液中H+移向______(填“锌”或“石墨”)电极。
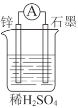
(2)下列反应通过原电池装置,可实现化学能直接转化为电能的是______(填序号)。
①2H2+O2=2H2O②HCl+NaOH=NaCl+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知t℃时AgCl的Ksp=2×10-10;在t℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )
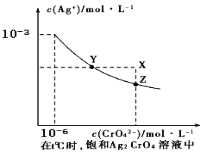
A. 在t℃时,Ag2CrO4的Ksp为1×10-9
B. 在饱和Ag2CrO4溶液中加入K2CrO4可使溶液由Y点到X点
C. 在t℃时,以0.01 mol/L AgNO3溶液滴定20 mL0.01 mol/LKCl和0.01 mol/L的K2CrO4的混和溶液,Cl-先沉淀
D. 在t℃时,AgCl的溶解度大于Ag2CrO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中,正确的是( )
A.甲烷的燃烧热为 890.3 kJmolˉ1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=+890.3 kJmolˉ1
B.稀盐酸和稀氢氧化钠溶液混合, 其热化学方程式为:H++OH-=H2O; △H =-57.3 kJmolˉ1
C.已知 H2 燃烧热为 142.9kJmolˉ1 ,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(1);△H =-285.8 kJmolˉ1
D.500℃、30MPa 下,将 0.5mol N2 和 1.5molH2 置于密闭的容器中充分反应生成 NH3(g),放热 19.3kJ,其热化学方程式为:N2(g) + 3H2(g) ![]() 2NH3(g) ;△H=-38.6kJ· mol-1
2NH3(g) ;△H=-38.6kJ· mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.已知氢气的燃烧热为285.8kJ/mol,相应的热化学方程式为H2(g)+1/2O2(g)=H2O(g),△H=-285.8 kJ/mol
B.中和相同体积、相同物质的量浓度的①硫酸,②盐酸和③醋酸所需相同浓度的NaOH溶液的体积关系:V1>V2=V3
C.稀氨水中部分粒子的浓度大小关系:c(NH3·H2O)>c(OH-)>c(NH4+)>c(H+)
D.1mol/LNaX和1mol/LNaY两种盐溶液中c(X-)=c(Y-)+c(HY),则HX为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬烯是一种食用香料,其结构简式如图所示,下列有关柠檬烯的说法正确的是( )

A.它的一氯代物有 7 种
B.它与足量氢气反应后生成的分子中所有的碳原子可能在同一平面上
C.它与足量的溴水反应后,产物的化学式为:C10H14Br4
D.一定条件下,它可以发生加成、取代、氧化等反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼是一种强还原剂,用NaClO与NH3反应可用于生产肼(N2H4),其反应的化学方程式为:NaClO+2NH3= N2H4+NaCl+H2O。
⑴生产1000 g质量分数为25.6%的肼溶液最少需要___________L(标准状况)NH3。
⑵工业次氯酸钠溶液中含有氯酸钠会影响所得肼的产品质量。测定次氯酸钠样品中的氯酸钠含量的方法如下:取10.00 mL 碱性NaClO溶液试样,加入过量H2O2,将次氯酸钠完全还原(ClO3-在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性),加热煮沸,冷却至室温,加入硫酸至酸性,再加入0.1000 mol·L-1 硫酸亚铁标准溶液30.00 mL,充分反应后,用0.01000 mol·L-1酸性K2Cr2O7溶液滴定至终点(Cr2O72-被还原为Cr3+),消耗该溶液20.00 mL。
①用H2O2与次氯酸钠反应的离子方程式为___________。
②实验中加热煮沸的目的是___________。
③计算样品中NaClO3的含量(以g·L-1表示),写出计算过程。___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列比较中正确的是
A. 相同浓度的三种溶液:①(NH4)2CO3溶液、②NH4HCO3溶液、③NH4NO3溶液中 c(NH4+):③>①>②
B. 相同pH的溶液:①NaClO溶液、②NaHCO3溶液、③CH3COONa溶液中 c(Na+):③>②>①
C. 同浓度、同体积的溶液:①CH3COONa溶液、②NH4Cl溶液、③NaNO3溶液中 pH:②>③>①
D. 相同浓度的溶液:①氨水、②NaOH溶液、③Ba(OH)2溶液 c(H+):②>①>③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com