
����Ŀ����֪t��ʱAgCl��Ksp��2��10��10����t��ʱ��Ag2CrO4��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵����ȷ���ǣ� ��
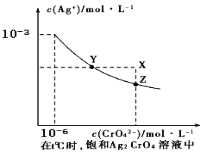
A. ��t��ʱ��Ag2CrO4��KspΪ1��10��9
B. �ڱ���Ag2CrO4��Һ�м���K2CrO4��ʹ��Һ��Y�㵽X��
C. ��t��ʱ����0.01 mol/L AgNO3��Һ�ζ�20 mL0.01 mol/LKCl��0.01 mol/L��K2CrO4�Ļ����Һ��Cl���ȳ���
D. ��t��ʱ��AgCl���ܽ�ȴ���Ag2CrO4
���𰸡�C
��������
����A����t ��ʱ��Ag2CrO4��Ksp=" c"2��Ag����c ��Cl����=1��10��12������B���ڱ���Ag2CrO4��Һ�м���K2CrO4����Һ�и����Ũ������Ag2CrO4��Ksp���䣬��Һ��������Ũ�ȼ�С������ʹ��Һ��Y�㵽X�㣬����C����t ��ʱ���������Ȼ�����������c(Ag+)c(Cl-)��Ksp��2��10��10����c(Ag+)��Ksp/ c(Cl-)��2��10��10/0.01=2��10-8mol/L��������Ag2CrO4��������c2(Ag+)c(CrO42-)��Ksp��1��10��12����c2(Ag��)��Ksp/ c(CrO42-)��1��10��12/0.01=1��10-10��c(Ag��)=1��10-5mol/L������0��01 mol/L AgNO3��Һ�ζ�20 mL0��01 mol/L KCl��0��01 mol/L��K2CrO4�Ļ����Һ��Cl���ȳ�������ȷ��D����t ��ʱ��AgCl���ܽ��С��Ag2CrO4������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס������ɶ�����Ԫ����ɵij������ʻ���������ѧ��ѧ�����������ʻ��������������ת����ϵ��![]() ����˵������ȷ����
����˵������ȷ����
A. ����Ϊ��ɫ��ζ���壬�������CO32-
B. �����Ǿ��д̼�����ζ�����壬��ס��Ҿ�����ͬ�ĵ�����
C. ���ס��Ҿ�Ϊ���ӣ��ס�������������ͬһ��Һ��һ�����ܴ�������
D. ���п�����AlO2-��Ҳ�п�����Al(OH)3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�ʱ��һ��ѹǿ�µ��ܱ������з�����Ӧ��aX(g)+bY(g)![]() cZ(g)+dW(g)����ƽ������¶Ȳ���ѹǿ������ԭ����2�������ٴﵽƽ��ʱ��W��Ũ��Ϊԭƽ��״̬��1.8��������������ȷ��
cZ(g)+dW(g)����ƽ������¶Ȳ���ѹǿ������ԭ����2�������ٴﵽƽ��ʱ��W��Ũ��Ϊԭƽ��״̬��1.8��������������ȷ��
A. ƽ������ B. (a+b)>(c+d)
C. Z�����������С D. X��ת���ʱ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ����˹�����ǣ���ͼ�ף��ܹ���ú������еļ���ﵽһ��Ũ��ʱ��ͨ����������ʾ����������˹�����ǹ���ԭ������ȼ�ϵ�صĹ���ԭ������װ������ͼ����ʾ�����еĹ���������Y2O3��Na2O��O2�����������������ƶ��������й�������ȷ�ĵ���( )

A. ��˹�����ǹ���ʱ������ڵ�·�е����ɵ缫b����缫a
B. �缫a�ķ�ӦʽΪ��CH4+5O2���D8e����CO32�� +2H2O
C. �缫b������, O2-�ɵ缫a����缫b
D. ��������������1 mol O2��ͨ��ʱ������ת��4 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������Ҫ�Ĺ���Ԫ�ء�
��1����λ��Ԫ�����ڱ��ĵ�______�壬���̬ԭ����δ�ɶԵ��Ӹ���Ϊ________��
��2��[Fe(H2NCONH2)]6(NO3)3�������������������غ���(��)����һ����Ҫ�������û�������Fe3+�ĺ�������Ų�ʽΪ_________________________________�������ǽ���Ԫ�صĵ縺���ɴ�С��˳����_____________________________��
��3������[CO(NH2)2]�����У�̼ԭ��Ϊ_______�ӻ�����������������������Ŀ֮��Ϊ_________��
��4��Co(NH3)5BrSO4���γ������ܵ������,�ṹ�ֱ�Ϊ[Co(NH3)5Br]SO4��[Co(SO4)(NH3)5]Br����֪Co3+����λ��Ϊ6��Ϊȷ���ܵ������Ľṹ���ֶ�����������������ʵ�飺�ڵ�һ���������Һ�м�����������Һ������ɫ�������ڵڶ����������Һ�м�����������Һ��������ɫ��������ڶ�������������Ϊ__________��

��5����������̼�ܽ���r-Fe���γɵ�һ�ּ�϶�����壬���ԣ��侧��Ϊ���������ṹ����ͼ��ʾ��������ʵĻ�ѧʽΪ____________���������ܶ�Ϊd g��cm-3���������������̼ԭ�ӵľ���Ϊ__________pm(�����ӵ�������ֵ��NA��ʾ��д����ļ���ʽ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����³�ѹ�£����и��������ܹ������( )
A. SO2��O2B. NO��O2
C. HBr��Cl2D. NH3��HCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ֪ʶ�ش��������⡣
��1����֪Ksp(BaCO3) =2.6��l0-9��Ksp(BaSO4)=1.1��10-10��
��BaCO3��20 mL 0.01 mol��L��1Na2CO3��Һ�е�Ksp _________������ڡ�����С�ڡ����ڡ�������20 mL 0.01 mol��L��1 BaCl2��Һ�е�Ksp
���ֽ�Ũ��Ϊ2��10-4mol/LNa2CO3��Һ��BaCl2��Һ�������ϣ�������BaCO3��������BaCl2��Һ����СŨ��Ϊ_______mol/L��
������BaSO4�������Һ�еμ�Na2CO3��Һ������BaCO3��������ʱ����Һ��c(CO32��)/c(SO42��)=___________��������λ��Ч���֣���
��2����֪25�� ʱ��Ksp[AgCl]=1.8��10��10���ֽ������Ȼ����ֱ���룺a��100mL����ˮ�У�b��100mL 0.2 mol/LAgNO3��Һ�У�c��100mL 0.1 mol/L�Ȼ�����Һ�У�d��100mL 0.1 mol/L������Һ�С���ֽ�������ͬ�¶���������Ũ���ɴ�С��˳����_______________������д��ţ���b�������ӵ�Ũ��Ϊ__________mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����(����)
A. ��ˮϡ��0.01 mol��L-1��CH3COOH��Һ,��Һ��c(OH-)��С
B. ����ʱ,0.1 mol��L-1��ijһԪ��HA��ˮ����0.1%��������,�����Һ��pH=4
C. ��ˮ��ˮϡ�ͺ�,��Һ��![]() ��ֵ����
��ֵ����
D. ������,pH��Ϊ5���������Ȼ����Һ��,ˮ�ĵ���̶���ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(NaN3)��������ȫ���ҵIJ�������Fe2O3������������NaHCO3����ȴ��������������������ײʱ���ֽ������������ʹ��ȫ����Ѹ�ٴ��Ӷ���ȫ�������ã���֪Ka(HN3)=1.8��10-5�ݡ������й�˵����ȷ����
A. NaHCO3����ȴԭ�����������ֽ⣬������ϵ������
B. Fe2O3��Na��Ӧ������������Na2O2
C. �����ʵ�����NaN3��HN3�����Һ�Լ���
D. ����6.5 gNaN3�ֽ����N2����ת��0.9 mol����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com