
【题目】据报道,摩托罗拉公司开发了一种以甲醇为原料,以KOH溶液为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月.右图是一个电化学过程的示意图.已知甲池的总反应式为: 2CH3OH+3O2+4KOH![]()
![]() 2K2CO3+6H2O
2K2CO3+6H2O
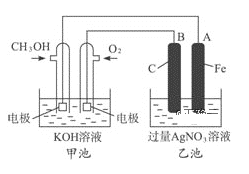
请填空:
(1)充电时:①燃料电池的正极与电源______极相连.
②阳极的电极反应式为__________________________________.
(2)放电时:负极的电极反应式为______________________________.
(3)在此过程中若完全反应,乙池中A极的质量增加324g,则甲池中理论上消耗O2______L(标准状况下).
(4)工业上用3克氢气与足量二氧化碳反应生成气态甲醇(CH3OH)和水蒸气,放出24.5千焦的热量,请写出该反应的热化学反应方程式:_________________________.
(5)用该电池为电源电解氯化镁制取金属镁,消耗甲醇1.6g,可制得金属镁______g.
【答案】正 4OH--4e-=2H2O+O2↑ CH3OH+8OH--6e-=CO32-+6H2O 16.8 3H2(g)+CO2(g)=H2O(g)+CH3OH(g)△H=-49.0kJ·mol-1 3.6.
【解析】
通过图像可知,甲池为原电池,且通入氧气的一极为正极,通入甲醇的一极为负极,则A为阴极,Fe不参与反应,B为阳极。
(1)充电时:作电解池,①燃料电池的正极产生氧气,化合价由-2变为0,失电子,则与电源的正极相连;
②燃料电池的正极作电解池的阳极,氢氧根离子失电子生成氧气,电极反应式为4OH--4e-=2H2O+O2↑;
(2)放电时:甲烷失电子与溶液中的氢氧根离子反应生成碳酸根离子和水,电极反应式为CH3OH+8OH--6e-=CO32-+6H2O;
(3)乙池为电解池,A极作阴极,Ag++e-=Ag,质量增加324g,即0.3mol,理论上生成0.75mol氧气,即标况下的16.8L;
(4)氢气与二氧化碳生成甲醇和水,方程式为3H2(g)+CO2(g)=H2O(g)+CH3OH(g),3g氢气完全反应释放24.5kJ的热量,则6g即3mol氢气释放49.0kJ,焓变为-49.0kJ·mol-1;
(5)消耗甲醇1.6g即0.05mol时,转移0.3mol电子,则生成0.15molMg,即3.6g。


科目:高中化学 来源: 题型:
【题目】已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOH ![]() CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是( )
CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是( )
①加少量烧碱溶液 ②升高温度 ③加少量冰醋酸 ④加水
A. ①② B. ②④ C. ③④ D. ①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。
回答下列问题:
(1)L的元素符号为________ ;M在元素周期表中的位置为________________;五种元素的原子半径从大到小的顺序是____________________(用元素符号表示)。
(2)Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为___,B的结构式为____________。
(3)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,
则Se的原子序数为_______,其最高价氧化物对应的水化物化学式为_______。
该族2~5周期元素单质分别与H2反应生成lmol气态氢化物的反应热如下,表
示生成1mol硒化氢反应热的是__________(填字母代号)。
a.+99.7 mol·L-1b.+29.7 mol·L-1
c.-20.6 mol·L-1d.-241.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图乙是根据图甲的电解池进行电解时某个量(纵坐标x)随时间变化的函数曲线(各电解池都用石墨作电极,不考虑电解过程中溶液浓度变化对电极反应的影响),这个量x是表示( )
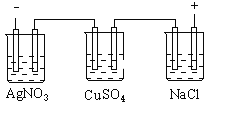
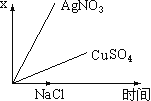
甲 乙
A. 各电池析出气体体积总数的变化B. 各电解池阳极质量的增加
C. 各电解池阴极质量的增加D. 各电极上放电的离子总数的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是
A.标准状况下,22.4L氦气含有所含的原子数约为6.02×1023
B.标准状况下,aL的二氧化碳和氮气的混合物含有的分子数约为![]() ×6.02×1023
×6.02×1023
C.22 g二氧化碳与标准状况下11.2 L 氯化氢气体含有的分子数相同
D.标准状况下,2.24L CCl4中含有的原子数约为0.5×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有25 mL 2 mol·L-1Na2CO3和75 mL 1 mol·L-1的稀盐酸:①将Na2CO3溶液缓缓滴到稀盐酸中 ②将稀盐酸缓缓滴到Na2CO3溶液中,在标准状况下产生气体的体积情况( )
A.均为0.84 L
B.均为0.56 L
C.①>②
D.②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用情性电极电解100ml0.5mol/L的CuSO4溶液、当阳极产生1.12L(标准状况)气体时,若要使电解质溶液恢复到电解前的状态,需加入的物质是( )
A. CuCO3B. CuOC. Cu(OH)2D. CuSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜铁及其化合物在日常生活和工业生产中有着重要用途。
(1)铁制炊具在潮湿的空气中易发生吸氧腐蚀而生锈,负极的电极反应式为:___,正极的电极反应式为:___。
(2)下列哪些装置可防止铁棒被腐蚀___。(填正确答案标号)
A.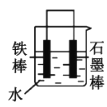 B.
B.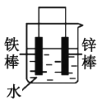 C.
C.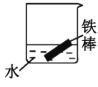 D.
D.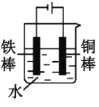
(3)高铁酸钾(K2FeO4)广泛应用于净水、电池工业等领域。工业上以钛白粉生产的副产品FeSO4制备高铁酸钾的生产流程如图:
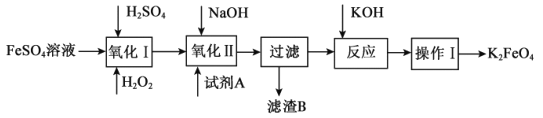
查阅资料:K2FeO4在水中溶解度很大,在碱性环境中稳定,在中性和酸性条件下不稳定。
①“氧化I”中,生成Fe3+的离子反应方程式是___。
②净水时高铁酸钾能逐渐与水反应生成絮状的Fe(OH)3,请补充并配平该反应方程式: K2FeO4+ H2O= Fe(OH)3↓+ KOH+ 。___。
(4)工业上常以铜做阳极,石墨做阴极,电解含有NaOH的NaCl水溶液制备Cu2O。
已知:该电解过程中阳极先生成难溶物CuCl,再与NaOH反应转化为Cu2O。
①写出阳极的电极反应式___,该过程中生成Cu2O的离子反应方程式为___。
②如果电解后溶液体积未发生变化,电解后溶液中的c(OH-)会___(填“变大”“变小”或“不变”)。
③若电解时电路中通过0.2mol电子,理论上生成Cu2O的质量为___g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(s)+3B(g)![]() 2C(g)+ D(g),经2minB的浓度减少0.6mol/L。对此反应速率的表示正确的是
2C(g)+ D(g),经2minB的浓度减少0.6mol/L。对此反应速率的表示正确的是
A. 用A表示的反应速率是0.4 mol/(L·min)
B. 分别用B、C、D表示的反应速率其比值是3:2:1
C. 在2min末的反应速率,用B表示是0.3mol/(L·min)
D. 在这2min内用B和C表示的反应速率的值都是逐渐减小的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com