
【题目】下列化学反应中电子转移的表示方法不正确的是( )
A.  B.
B. 
C.  D.
D. 
【答案】A
【解析】
还原剂失电子,氧化剂得电子,且得失电子总数相等,据此进行分析。
A.金属钠做还原剂,失电子;硫做氧化剂,得电子,电子得失标错,故A错误;
B.单质溴中的溴元素化合价由0价降低到-1价,得电子;碘化钾中碘元素由-1价升高到0价,失电子,根据该反应可知转移了电子2e-,电子转移的表示方法正确,故B正确;
C.锌元素由0价升高到+2价,失电子;硫酸铜中铜元素由+2价降低到0价,得电子;根据该反应可知转移了电子2e-,电子转移的表示方法正确,故C正确;
D.氧化铜中铜元素由+2价降低到0价,得电子;氢气中氢元素由0价升高到+1价,失电子;根据该反应可知转移了电子2e-,电子转移的表示方法正确,故D正确;
综上所述,本题选A。


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
【题目】在实验室里使稀盐酸与锌起反应,在标准状况时生成5.6 L氢气,计算
(1)需要锌的物质的量____?
(2)需要2 mol/L的盐酸多少mL____ ?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在配制一定物质的量浓度的NaOH溶液时,下列哪个原因会造成所配溶液浓度偏高( )
A.所用NaOH已经潮解B.有少量NaOH溶液残留在烧杯里
C.向容量瓶中加水未到刻度线D.称量时误用“左码右物”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用如图装置进行铁与水蒸气反应的实验,并检验产物的性质,请回答下列问题:
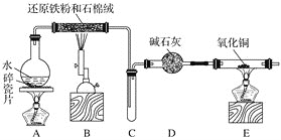
(1)A装置的作用是____________,烧瓶底部放碎瓷片的作用是_________________________。
(2)装置B中发生反应的化学方程式是____________________________________,该反应中氧化剂是__________,氧化产物是__________________。
(3)D的作用是__________________________________。
(4)E中的实验现象是____________________________。
(5)A、B两个装置中应先点燃________________处的酒精(喷)灯,点燃E处酒精灯之前应进行的操作是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁、铜等金属离子是人体内多种酶的辅因子。工业上从海水中提取镁时,先制备无水氯化镁,然后将其熔融电解,得到金属镁。
(1)以MgCl2为原料用熔融盐电解法制备镁时,常加入NaCl、KCl或CaCl2等金属氯化物,其主要作用除了降低熔点之外还有________。
(2)已知MgO的晶体结构属于NaCl型。某同学画出的MgO晶胞结构示意图如图所示,请改正图中错误:__________________。
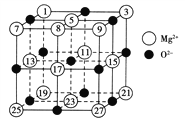
(3)Mg是第三周期元素,该周期部分元素氟化物的熔点见下表:
氟化物 | NaF | MgF2 | SiF4 |
熔点/K | 1 266 | 1 534 | 183 |
解释表中氟化物熔点差异的原因:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用如图所示装置来制取氯气,该装置由A、B、C三个基本装置组合而成,请回答下列问题:
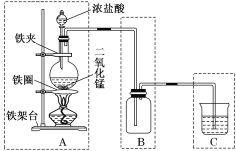
(1)说出A、B、C三个基本装置的名称:A是________装置,B是________装置,C是________装置。
(2)C装置中烧杯内所装液体是________溶液。
(3)写出A装置中反应的化学方程式_____________________________。
(4)氯气工业制法的原理为:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。
此反应的氧化剂是________,________元素的化合价升高;还原剂是_________,而________元素的化合价降低。该反应中4mol氧化剂能得到(失去)________mol电子。标准状况下,反应中产生了5.6L的氢气时,被氧化的物质的质量为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室制取氯气时,下列操作不正确的是________(填字母)。


A.装置Ⅰ可用于制取少量氯气
B.用装置Ⅱ除去氯气中的少量氯化氢
C.用装置Ⅲ制取氯气
D.用装置Ⅳ干燥氯气
(2)实验室制取干燥、纯净的氯气,除了二氧化锰、浓盐酸外还需要的试剂是____________、____________、____________。
(3)已知高锰酸钾与浓盐酸在常温下反应能产生氯气。
若用如下图所示的实验装置来制备纯净、干燥的氯气及验证它与金属的反应。每个虚线框表示一个单元装置,其中有错误的是________(填字母)。
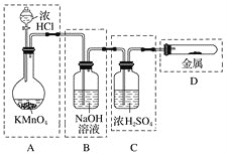
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】B元素和N元素对植物生长及人体健康有着十分重要的作用,也广泛应用于新型材料的制备。
(1)基态氮原子的外围电子排布图为________________;晶体硼单质的基本结构单元为正二十面体,其能自发地呈现多面体外形,这种性质称为晶体的__________________性。
(2)氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,与氨硼烷互为等电子体的分子、离子的化学式分别是______________、________________。 (各举一例),第二周期元素中第一电离能介于B和N之间的元素是______________(填元素符号)。
(3)血红素是吡咯(C4H5N)的重要衍生物,血红素(含Fe2+)可用于治疗缺铁性贫血。吡咯和血红素的结构如下图:

①己知吡咯中的各个原子均在同一平面内;则吡咯分子中N原子的杂化类型为________________。
②1mol吡咯分子中所含的σ键总数为__________个;分子中的大π键可用Π![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为____________。
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为____________。
③C、N、O三种元素的简单氢化物键角由小到大的顺序为_____________(填化学式),原因是__________________。
④血液中的O2是由血红素在人体内形成的血红蛋白来输送的,则血红蛋白中的Fe2+与O2是通过___________键相结合。
(4)氮化硼(BN)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图所示。已知该晶体密度为ag/cm3,根据硬球接触模型计算晶体中两个最近的N原子间的距离为:_________pm。(用含a的代数式表示,NA表示阿伏加德罗常数)

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com