
【题目】关于冰融化为水的过程判断正确的是
A. ΔH>0,ΔS>0 B. ΔH<0,ΔS>0
C. ΔH>0,ΔS<0 D. ΔH<0,ΔS<0
 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】标准状况下1.68 L 无色可燃气体在足量氧气中完全燃烧。若将产物全部通入足量澄清石灰水,得到的白色沉淀 15.0 g;若用足量碱石灰吸收所有燃烧产物,装碱石灰的干燥管增重 9.3 g若该气体由两种等物质的量的气体组成。则该气体的成分可能是( )
A. CH4和 C3H4 B. C3H6和 CO C. C3H4和 H2 D. C3H6和 CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列有关说法错误的是
A. 氢氧化铝可作抗酸药
B. 硅胶可用作袋装食品的干燥剂
C. 浓硫酸可刻蚀石英制的艺术品
D. 酱油中含有多种维生素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与能源开发、环境保护、资源利用等密切相关。下列说法正确的是
A. 为提高农作物的产量和质量,应大量使用化肥和农药
B. 绿色化学的核心是应用化学原理对环境污染进行治理
C. 实现化石燃料清洁利用,就无需开发新能源
D. 垃圾是放错地方的资源,应分类回收利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验淀粉水解产物,某学生设计了如下实验方案:

回答下列问题:
(1)试剂1是_____________;
(2)试剂2是_____________,作用是_______________________;
(3)如何检验第①步实验已基本完成_________________________________________。
(4)写出淀粉酿酒过程涉及到化学方程式:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在水溶液中能大量共存的一组离子是
A. Fe2+、H+、Cl-、NO3- B. K+、NH4+、OH-、Cl-
C. NH4+、Na+、Br-、SO42- D. Mg2+、H+、SiO32-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中既属于化合反应,又属于氧化还原反应的是( )
A. SO2+H2O2=H2SO4B. Zn+2AgNO3=Zn(NO3) 2+2Ag
C. 2HClO=2HCl+O2↑D. CO2+2NaOH=Na2CO3+H2 O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式不正确的是
A. 乙醛与银氨溶液反应:CH3CHO+2[Ag(NH3)2]++2OH-![]() CH3COO-+NH4++2Ag↓+3NH3+H2O
CH3COO-+NH4++2Ag↓+3NH3+H2O
B. 醋酸溶液与新制氢氧化铜反应:2CH3COOH+Cu(OH)2→Cu2++2CH3COO-+2H2O
C. 苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32-
D. 溴乙烷水解生成乙醇:CH3CH2Br+OH-![]() CH3CH2OH+Br-
CH3CH2OH+Br-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲酸乙酯为允许使用的食用香料,又称蚁酸乙酯,有辛辣的刺激味和菠萝样的果香香气,还有强烈朗姆酒似香气,并略带苦味。
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH
②有关有机物的沸点如下
试剂 | 乙醚 | 乙醇 | 甲酸 | 甲酸乙酯 |
沸点(℃) | 34.7 | 78.5 | 100.5 | 54.4 |
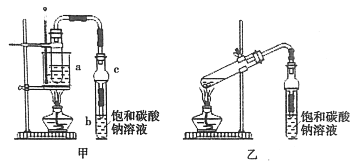
(1)制备粗品
将4mL乙醇、3mL甲酸和2mL浓硫酸加入试管a中,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管b内得到甲酸乙酯的粗品。
①实验时,加入数滴浓硫酸即能起催化作用,但实际用量多于此量,原因是__________;浓硫酸用量又不能过多,原因是_________。
②球形干燥管C的作用是__________。
③若用乙装置制备甲酸乙酯,其缺点有__________。
(2)制备精品
①反应结束后,从试管b中分离出甲酸乙酯粗品所用的主要仪器__________。
②从b中分离出的甲酸乙酯中常含有少量的乙醇、乙醚和水,应先加入无水氯化钙,除去______,然后再通过_________操作得到甲酸乙酯。
③某同学用装有饱和氢氧化钠的试管收集甲酸乙酯,几乎没有收集到产物。原因是______________(用化学方程式解释)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com