
二氧化硫和氮氧化物(NOx)对大气污染日趋严重,研究消除大气污染的方法是化学工作者的重要课题,目前有很多种方法消除大气污染。
(1)可利用甲烷催化还原NOx的方法处理NOx,反应如下:
CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g);△H= -574 kJ·mol-1
CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g);△H= -1160 kJ·mol-1
则CH4(g)+2NO2(g)= N2(g)+CO2(g)+2H2O(g);△H= ;
(2)降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:2NO(g)+2CO(g) N2(g)+2CO2(g);△H<0。
N2(g)+2CO2(g);△H<0。
若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,15分钟后达到平衡,反应过程中各物质的浓度变化如图甲所示,则平衡常数K= (小数点后保留3位);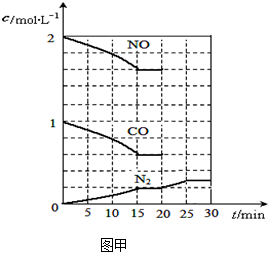
①若保持温度不变,20min时再向容器中充入CO气体0.6mol,平衡将 移动(填“向左”、“向右”或“不”);
②若保持温度不变,20min时向原平衡容器中充入CO、N2各0.6mol,平衡将 移动(填“向左”、“向右”或“不”);
③20min时,若改变反应条件,导致N2浓度发生如图所示的变化,则改变的条件可能是
(填字母);
| A.加入催化剂 | B.降低温度 | C.缩小容器体积 | D.增加CO2的量 |
(1)△H=-867 kJ·mol–1 (3分)
(2)K=0.035(或带单位:L/mol)(3分);向右、不移动; B(各2分)
(3)2Fe3++SO2+2H2O=2Fe2++SO42-+4H+(3分)
解析试题分析:(1) ①CH4(g) + 4NO2(g) =" 4NO(g)" + CO2(g) + 2H2O(g) △H=" –574" kJ·mol–1;
②CH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g) △H=" –" 1160 kJ·mol–1;
依据盖斯定律计算①+ ②得到:CH4(g) + 2NO2(g) = N2(g) + CO2(g) + 2H2O(g) △H=" –867" kJ·mol–1;
故答案为:△H= –867 kJ·mol–1;
(2)依据图象分析,15min时达到平衡时N2浓度为0.2mol·L–1,NO平衡浓度为1.6mol·L–1,CO浓度为0.6 mol·L–1,CO2浓度为0.4 mol·L–1,反应2NO(g) + 2CO(g)  N2(g) + 2CO2(g)的平衡常数
N2(g) + 2CO2(g)的平衡常数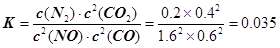 。故答案为:0.035。①若保持温度不变,20min时再向容器中充入CO气体0.6mol,此时c(CO) =" 1.2" mol·L–1,而生成物浓度不变,根据平衡移动原理,平衡将正反应方向移动。②若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,浓度分别为c(NO)="1.6" mol·L–1,c(CO)="0.6" mol·L–1 + 0.6 mol·L–1 =" 1.2" mol·L–1,c(N2) =" 0.2" mol·L–1 + 0.6 mol·L–1 =" 0.8" mol·L–1,c(CO2) =" 0.4" mol·L–1;
。故答案为:0.035。①若保持温度不变,20min时再向容器中充入CO气体0.6mol,此时c(CO) =" 1.2" mol·L–1,而生成物浓度不变,根据平衡移动原理,平衡将正反应方向移动。②若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,浓度分别为c(NO)="1.6" mol·L–1,c(CO)="0.6" mol·L–1 + 0.6 mol·L–1 =" 1.2" mol·L–1,c(N2) =" 0.2" mol·L–1 + 0.6 mol·L–1 =" 0.8" mol·L–1,c(CO2) =" 0.4" mol·L–1;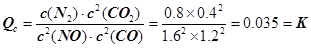 ,平衡不动。③如图甲所示,20min时,改变反应条件,导致反应速率减小,氮气浓度增大,平衡正向移动。加入催化剂,平衡不移动,A不合题;反应是气体体积减小的放热反应,降温可使平衡正向移动,氮气浓度增大,B符合题意;缩小容器体积虽然可使平衡正向移动,但改变条件的瞬间,N2浓度增大,与图中描绘的情况不符,C不合题意;增加CO2的量,平衡逆向移动,N2浓度减小,D也不合题。故答案为:B。
,平衡不动。③如图甲所示,20min时,改变反应条件,导致反应速率减小,氮气浓度增大,平衡正向移动。加入催化剂,平衡不移动,A不合题;反应是气体体积减小的放热反应,降温可使平衡正向移动,氮气浓度增大,B符合题意;缩小容器体积虽然可使平衡正向移动,但改变条件的瞬间,N2浓度增大,与图中描绘的情况不符,C不合题意;增加CO2的量,平衡逆向移动,N2浓度减小,D也不合题。故答案为:B。
(3) 总反应的离子方程式为:2SO2+O2+2H2O=4H+ + 2SO42-,总反应减去反应4Fe2+ + O2+ 4H+ =4Fe3+ + 2H2O即得另一离子方程式:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+。
考点:本题考查热化学方程式和盖斯定律的计算应用,化学平衡影响因素分析,平衡常数的计算方法,平衡移动原理的应用,离子方程式的书写。


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:填空题
氯气及其化合物在工农业生产和人类生活中都有着重要的应用。
(1)Ca(ClO)2、NaClO、NaClO2等含氯化合物都是常用的消毒剂和漂白剂,是因为它们都具有 性,请写出工业上用氯气与NaOH溶液反应生产消毒剂NaClO的离子方程式 。
(2)棕黄色强刺激性气体Cl2O为国际公认高效安全灭菌消毒剂之一,实验室可用潮湿的Cl2与Na2CO3反应制取少量Cl2O和NaHCO3的离子方程式 。
(3)黄色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,此反应的离子方程式为 。
②ClO2遇浓盐酸会生成Cl2,每生成1 mol Cl2转移电子的物质的量为 。
③ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为 。
(4)用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应4HCl+O2 2Cl2+2H2O,可实现氯的循环利用。
2Cl2+2H2O,可实现氯的循环利用。
已知:①上述反应中,4 mol HCl被氧化放出115.6 kJ的热量。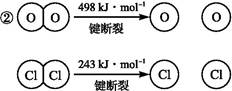
则断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为 kJ,H2O中H—O键比HCl中H—Cl键(填“强”或“弱”) 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某溶液仅含下列离子中的5种(不考虑水的电离及离子的水解)且各种离子物质的量均为1 mol 。
阳离子:Na+ 、Mg2+ 、Fe3+ 、Al3+ 、Fe2+ ;阴离子:OH—、CO32—、Cl—、NO3—、SO42—。
①若向溶液中加入KSCN溶液无明显变化;
②若向原溶液中加入稀盐酸,有无色气体生成,溶液中阴离子种类不变; 请推断:
(1)原溶液中含有阳离子 含有阴离子
(2)向原溶液中加入足量稀盐酸发生反应的离子方程式
(3)若向原溶液中加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体
质量为 g。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有A、B、C、D四种溶液,它们是烧碱、硫酸、碳酸氢铵、氯化铜溶液中的某一种。各取少量,将其两两混合,其中A、B混合有蓝色絮状沉淀生成, C 与足量B或D混合均有无色气体产生。根据题意回答下列问题:
(1)B、C分别是 、
(2)向A中滴加B,离子方程式:
向C中滴加D,离子方程式:
(3)少量B和C混合,现象:________,离子方程式:_______________________________。
(4)上述三个反应均属于________________反应(填基本反应类型),反应发生的条件的不同点是 ;相同点是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
KMnO4是一种重要的氧化剂。
(1)①在酸性条件下KMnO4的氧化性会增强。用来酸化KMnO4溶液的最佳试剂是 。
a.硝酸 b.硫酸 c.盐酸
②将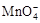 氧化C2O42?的离子方程式补充完整:
氧化C2O42?的离子方程式补充完整:
□MnO4? +□C2O42?+□ ==□Mn2+ +□CO2↑+□ 。
(2)某同学为了探究KMnO4溶液和Na2C2O4(草酸钠)溶液的反应过程,进行如下实验:
①配制100 mL 0.0400 mol·L-1的Na2C2O4溶液,除用到托盘天平、药匙、烧杯、量筒、玻璃棒等仪器外,还必须用到的玻璃仪器是 。
②将KMnO4溶液逐滴滴入一定体积的酸性Na2C2O4溶液中(温度相同,并不断振荡),记录的现象如下:
| 滴入KMnO4溶液的次序 | KMnO4溶液紫色褪去所需的时间 |
| 先滴入第1滴 | 60 s |
| 褪色后,再滴入第2滴 | 15 s |
| 褪色后,再滴入第3滴 | 3 s |
| 褪色后,再滴入第4滴 | 1 s |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)现有以下物质:①NaCl晶体 ②SO2 ③稀硫酸 ④石墨 ⑤BaSO4固体 ⑥蔗糖(C12H22O11) ⑦酒精 ⑧熔融的KNO3 ⑨CaO ⑩纯净的醋酸
请回答下列问题(用序号):
以上物质中能导电的是 ;以上物质中属于电解质的是 。
(2)按要求写出下列对应的方程式:
(①电离方程式、②化学方程式、③离子方程式)
①Al2(SO4)3:
②CO2+2OH-=CO32-+H2O:
③NaHCO3与NaHSO4溶液反应:
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
按要求填空
(一)、X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y的一种单质具有特殊臭味,Z与X原子最处层电子数相同。回答下列问题:
(1)由上述元素组成的化合物中,既含有极性共价键又含有离子键的化合物的电子式 ;
(2)X和Y组成的化合物中,有一种既含有极性共价键又含有非极性共价键。此化合物可将碱性工业废水中的CNˉ氧化为碳酸盐和氨,相应的离子方程式为
(二)、在一定条件下,RO3nˉ和Iˉ发生反应,离子方程式为: RO3nˉ+6Iˉ+6H+==Rˉ+3I2+3H2O
RO3nˉ-中R元素的化合价为 ,R元素的原子最外层电子有 个。
(三)、Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1︰16,则x值是
(四)、已知M2On2ˉ可与R2ˉ作用,R2ˉ被氧化为R的单质,M2On2ˉ的还原产物中,M为+3价,又知c(M2On2ˉ)=0.3mol/L的溶液100mL可与c(R2ˉ)=0.6mol/L的溶液150mL恰好完全反应,则n值为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
在Na+浓度为0.5mol/L的某澄清溶液中,还可能含有下表中的若干种离子:
| 阳离子 | K+、Ag+、Mg2+、Ba2+ |
| 阴离子 | NO3-、CO32-、SiO32-、SO42- |
| 序号 | 实验内容 | 实验结果 |
| Ⅰ | 向该溶液中加入足量稀HCl | 产生白色沉淀并放出0.56L气体 |
| Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4g |
| Ⅲ | 在Ⅱ的滤液中滴加BaC12溶液 | 无明显现象 |
| 阴离子 | NO3- | CO32- | SiO32- | SO42- |
| c/mol·L-1 | | | | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4 mL 0.5 mol/L的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式:______________________________________________。
(2)实验②的化学反应中转移电子的物质的量是________。
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com