
Na2FeO4是一种高效多功能水处理剂,既能消毒杀菌,又能除去悬浮物杂质。一种制备Na2FeO4的反原理为2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑,下列有关说法正确的是
A.反应中氧化剂是Na2O2,还原剂是FeSO4
B.生成2 mol Na2FeO4时,反应中共有10 mol电子转移
C.Na2FeO4的氧化性大于Na2O2
D.Na2FeO4净水过程中,既有氧化还原反应发生,又有非氧化还原反应发生
BD
【解析】
试题分析:A、根据方程式可知铁元素化合价从+2价升高到+6价,失去4个电子,硫酸亚铁是还原剂。过氧化钠中氧元素化合价从—1价部分升高到0价,部分降低到—2价,因此过氧化钠既是氧化剂,也是还原剂,A错误;B、生成2 mol Na2FeO4时,生成1mol氧气,则反应中共有2mol×4+1mol×2=10 mol电子转移,B正确;C、氧化剂的氧化性强于氧化产物的氧化性,则过氧化钠的氧化性强于高铁酸钠,C错误;D、高铁酸钠具有氧化性,在Na2FeO4净水过程中,有氧化还原反应发生,生成的还原产物铁离子水解转化为氢氧化铁胶体而净水,则又有非氧化还原反应发生,D正确,答案选BD。
考点:考查氧化还原反应


科目:高中化学 来源:2014-2015学年浙江省名校新高考研究联盟高三上学期联考化学试卷(解析版) 题型:选择题
“地沟油”在一定条件下,能发生如下反应,化学方程式为:

下列叙述错误的是
A.“地沟油”主要成分是高级脂肪酸的甘油酯
B.生物柴油是不同酯组成的混合物
C.生物柴油属于化石燃料
D.“地沟油”可用于制备生物柴油
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市崇明县高三上学期期末考试化学试卷(解析版) 题型:选择题
向100mL 0.1mol? L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol ·L-1Ba(OH)2溶液。随着Ba(OH)2溶液体积(V)的变化,沉淀总物质的量(n)的变化如右图所示。下列叙述正确的是
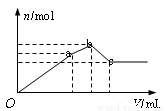
A.a点的沉淀总物质的量为0.03mol
B.oa段发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH-= 2BaSO4↓+Al(OH)3↓;
C.ab段发生反应的离子方程式是:2NH4++SO42-+Ba2++2OH-=2NH3?H2O+ BaSO4↓
D.反应到c点时,加入Ba(OH)2溶液的总体积为250mL
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市崇明县高三上学期期末考试化学试卷(解析版) 题型:选择题
具有防腐作用的甲醛
A.分子中共有12个电子 B.能发生加聚反应
C.难溶于水易溶于酒精 D.比例模型为:
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三元月模拟测试化学试卷(解析版) 题型:填空题
(12分)某强酸性溶液X含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、NO3-中的一种或几种,取该溶液进行连续实验,实验内容如下:

根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H+外还肯定含有的离子是____________________,不能确定是否含有的离子是___________。
(2)沉淀G的化学式为_____________。
(3)①中生成A的离子方程式____________________。
(4)过滤操作中所使用到的玻璃仪器的名称为____________________。
(5)简述实验室检验气体F的方法 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三元月模拟测试化学试卷(解析版) 题型:选择题
以下根据实验现象的推断,正确的是
A.能使润湿的碘化钾淀粉试纸变蓝的气体一定是Cl2
B.能使澄清石灰水变浑浊的无色气体一定是CO2
C.在潮湿空气中能形成白雾的气态氢化物一定是HCl
D.溶于水能形成无色溶液的红棕色气体一定是NO2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三元月模拟测试化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W 的原子序数依次增大,且原子最外层电子数之和为13,X 的原子半径比Y 的小,X 与W 同主族,Z 是地壳中含量最高的元素。下列说法正确的是
A.由X 、Y组成的化合物的沸点总低于由X与Z组成的化合物的沸点
B.元素Z、W 的简单离子的电子层结构不同
C.元素Y 的简单气态氢化物的热稳定性比Z 的强
D.只含X、Y、Z 三种元素的化合物,可能是离子化合物,也可能是共价化合物
查看答案和解析>>
科目:高中化学 来源:2014--2015吉林省高一上学期期末化学试卷(解析版) 题型:填空题
(10分)某学校实验室从化学试剂商店买回18.4 mol·L-1的硫酸。现用该浓硫酸配制100 mL 1 mol·L-1的稀硫酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平。请回答下列问题:
(1)配制稀硫酸时,上述仪器中不需要使用的有______________(选填序号),还缺少的仪器有________(写仪器名称)。
(2)配制100 mL 1 mol·L-1的稀硫酸需要用量筒量取上述浓硫酸的体________mL(保留一位小数),量取浓硫酸时应选用________(选填①10 mL、②50 mL、③100 mL)规格的量筒。
(3)实验中造成所配溶液浓度偏高的原因可能是_________。
A.容量瓶中原来含有少量蒸馏水
B.未经冷却,立即转移至容量瓶并洗涤烧杯,定容
C.烧杯没有洗涤
D.向容量瓶中加水定容时眼睛一直仰视刻度线
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高一1月月考化学试卷(解析版) 题型:选择题
下列有关NaHCO3和Na2CO3性质的比较中,正确的是
A.热稳定性:Na2CO3<NaHCO3
B.常温时在水中的溶解度:Na2CO3<NaHCO3
C.等质量的NaHCO3和Na2CO3与足量稀盐酸反应产生CO2的量:Na2CO3<NaHCO3
D.等物质的量的NaHCO3和Na2CO3与足量稀盐酸反应,NaHCO3放出的CO2多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com