
| A�� | һ�������£�2molSO2��1molO2������ܱ������г�ַ�Ӧ�������еķ���������2NA | |
| B�� | ��1molCH3COONa������CH3COOH�γɵ�������Һ�У�CH3COO-��ĿΪNA�� | |
| C�� | 1 mol Na��O2��ȫ��Ӧ������Na2O��Na2O2�Ļ���ת�Ƶ�������ΪNA�� | |
| D�� | 60g���������к��еĹ��ۼ���Ϊ2NA�� |
���� A����������������ķ�ӦΪ���淴Ӧ��
B����1molCH3COONa������CH3COOH�γɵ�������Һ�У�n��CH3COO-��+n��OH-��=n��H+��+n��Na+����
C�������Ʒ�Ӧ���Ϊ+1����������
D�����������������ʵ�����Ȼ�����1mol���������к�4mol���ۼ���������
��� �⣺A����������������ķ�ӦΪ���淴Ӧ���ʲ��ܽ��г��ף��ʷ�Ӧ�������еķ��Ӹ�������2NA������A��ȷ��
B����1molCH3COONa������CH3COOH�γɵ�������Һ�У�n��CH3COO-��+n��OH-��=n��H+��+n��Na+����������Һ�����Եģ����У�n��OH-��=n��H+��������n��CH3COO-��=n��Na+��=1mol���ʴ��������ΪNA������B��ȷ��
C�������Ʒ�Ӧ���Ϊ+1�ۣ���1mol�Ʒ�Ӧ��ת��NA�����ӣ���C��ȷ��
D��60g������������ʵ���Ϊ1mol����1mol���������к�4mol���ۼ����ʺ�4NA������D����
��ѡD��
���� ���⿼�������ʵ����Ͱ���٤���������йؼ��㣬�ѶȲ���Ӧע�����ʽṹ���ص��ʽ�����ã�


 ����ѧ���ʱѧ����ϵ�д�
����ѧ���ʱѧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 8% H2O2��Һ��H+��Fe2+��SO42-��Cl- | |
| B�� | ����Fe3+����Һ��Na+��Al3+��Cl-��SCN- | |
| C�� | ʹ���ȳʺ�ɫ����Һ��Na+��NH4+��AlO2-��CO32- | |
| D�� | $\frac{{K}_{W}}{c��{H}^{+}��}$=0.1 mol•L-1����Һ��Na+��K+��CO32-��ClO- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
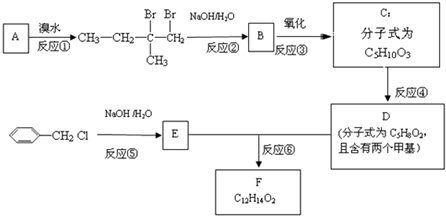
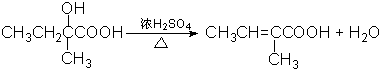 ��
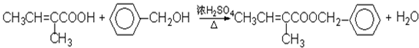
��
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ����������ԭ��Ӧ��2Ag+��aq��+Cu��s���TCu2+��aq��+2Ag��s����Ƶ�ԭ�����ͼ��ʾ����ش��������⣺
����������ԭ��Ӧ��2Ag+��aq��+Cu��s���TCu2+��aq��+2Ag��s����Ƶ�ԭ�����ͼ��ʾ����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | K3C60��ֻ�����Ӽ� | B�� | K3C60�в������ۼ� | ||
| C�� | �þ���������״̬���ܵ��� | D�� | C60��12C��Ϊͬλ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��100mL 0.1mol/L��FeSO4��Һ�У�����0.01mol Na2O2����2Fe2++2Na2O2+2H2O�T4Na++2Fe��OH��2+O2�� | |
| B�� | ��������Һ����μ���Ba��OH��2��Һ��SO42-ǡ�ó�����ȫ2Al3++3SO42-+3Ba2++6OH-�T2Al��OH��3��+3BaSO4�� | |
| C�� | ��������Һ��ͨ������CO2��CO2+H2O+2C6H5O-�T2C6H5OH+CO32- | |
| D�� | ��40mL0.5mol/LFeBr2��Һ��ͨ��448mLCl2����״������2Fe2++2Br-+2Cl2�T2Fe3++4Cl-+Br2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| Ԫ�ش��� | L | M | Q | R | T |
| ԭ�Ӱ뾶/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| ��Ҫ���ϼ� | +2 | +3 | +2 | +6��-2 | -2 |
| A�� | L2+��R2-�ĺ����������� | B�� | ������ϡ���ᷴӦ������ΪL��Q | ||
| C�� | M��T�γɵĻ������������ | D�� | �⻯��ķе�ΪH2T��H2R |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com