
【题目】下列各组离子在指定溶液中一定不能大量共存的是
A.使淀粉碘化钾试纸变蓝的溶液中:K+、SO42-、Na+、ClO-
B.使石蕊试液变红的溶液中:Al3+、Cl-、NH4+、NO3-
C.c(Al3+) = 0.1 mol/L的溶液中:AlO2-、Na+、Cl-、K+
D.![]() = 1×10-13 的溶液中:CH3COO-、CO32-、K+、SO32-
= 1×10-13 的溶液中:CH3COO-、CO32-、K+、SO32-
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知某有机物的结构简式为:![]()
(1)该有机物中所含官能团的名称是________________,________________。
(2)该有机物发生加聚反应后,所得产物的结构简式为__________________。
(3)写出该有机物使溴水褪色的化学方程式____________________________。
(4)写出该有机物发生消去反应的化学方程式(注明反应条件)_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组,在实验室里模拟用N2和H2合成氨,反应的化学方程式为N2+3H2![]() 2NH3。现用未经干燥的N2和H2按体积比V(N2)∶V(H2)=1∶3充分混合后,按如图所示的装置进行有关实验。
2NH3。现用未经干燥的N2和H2按体积比V(N2)∶V(H2)=1∶3充分混合后,按如图所示的装置进行有关实验。
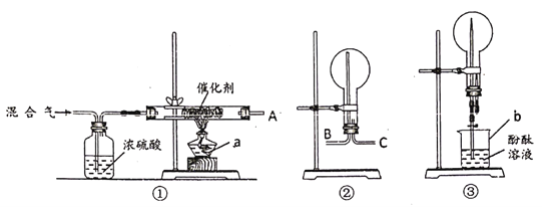
请回答下列问题:
(1)装置①中浓硫酸的作用是________。
(2)若用装置②收集反应生成的气体,A应连接装置中的________(填“B”或“C”);
(3)收集满气体后,再用装置③进行实验,当烧瓶中的液面逐渐上升,溶液呈________色。
(4)实验结束时,溶液几乎充满了烧瓶,则溶液的物质的量浓度为________mol/L(气体为标准状况下的体积)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取少量溴乙烷的装置如图所示,将生成物导入盛有冰水混合物的试管a中,实验结束发现试管a中的物质分为三层.对该实验的分析错误的是( )

A. 烧瓶中除发生取代反应可能发生消去反应、氧化还原反应等
B. 产物在a中第一层
C. a中有产物和水还含HBr、CH3CH2OH等
D. b中盛放的酸性KMnO4溶液会褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知如表数据。
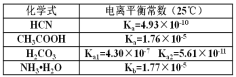
(1)25℃时,pH=11的NaCN溶液中水电离出的c(OH-)=_____molL-1。
(2)25℃时,等浓度的NaCN、Na2CO3溶液、CH3COONa三种溶液的pH值由大到小的顺序为_____。
(3)0.100molL-1NH4HCO3溶液中物质的量浓度最大的离子是_____(填化学式)。
(4)向NaCN溶液中通入少量CO2,所发生反应的化学方程式为_____。
(5)25℃1.10molL-1CH3COOH溶液中,CH3COOH的电离度约为_____。
(6)25℃时等体积等浓度的NaCl与NaCN两溶液中,离子总数NaCl_____NaCN(填“大于”、“小于”或“等于”);
(7)HCN与NaOH反应后的溶液中存在:c(Na+)=c(CN-),该溶液呈_____性(填“酸”“碱”或“中”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷有多种化合物,次磷酸(H3PO2)和次磷酸钠(NaH2PO2)常为化工生产中的还原剂。完成下列填空:
(1)H3PO2是一元中强酸,写出其电离方程式:_______;请将NaH2PO2溶液中的各离子按浓度由大到小的顺序排列:__________。
(2)室温下0.1mol/L的NaH2PO2溶液和0.1mol/L的Na2CO3溶液,pH更大的是_______,其原因是__________。
(3)化学镀银,可利用H3PO2把溶液中的Ag+还原为银的反应,已知该反应中还原剂与氧化剂的物质的量之比为1:4,则氧化产物是_______(填化学式)。
(4)工业上可用白磷(P4)与Ba(OH)2溶液反应生成PH3和Ba(H2PO2)2。写出并配平该反应的化学方程式________,若反应中转移电子6NA,用去还原剂_____mol。再向Ba(H2PO2)2溶液中加入盐酸制备H3PO2,有人说应该用硫酸代替盐酸,请说明用硫酸代替盐酸的优点:_______。
(5)下图是利用电解原理制备H3PO2的示意图(阳离子交换膜和阴离子交换膜分别只允许阳、阴离子通过;已知电极反应为:

阳极 4OH--4e→O2↑+ H2O
阴极 2H+ + 2e→H2↑):
分析在阳极室得到H3PO2原因:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物F是合成高活性、安全农药茚虫威的重要中间体。
已知:![]()
以化合物A为原料合成化合物F的流程如下:
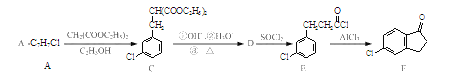
完成下列填空:
(1)写出反应A→B的化学方程式_________。
(2)写出化合物D中含氧官能团的名称_______;写出B→C的反应类型__________。
(3)某化合物是D的同分异构体,能使FeCl3溶液显紫色,且分子中只有3种不同化学环境的氢。写出该化合物的结构简式__________(任写一种)。
(4)E→F的转化中,会产生一种与F互为同分异构体且碳环上碳原子数目相同的副产物,其结构简式为________________。
(5)根据已有知识并结合所给信息,写出以化合物F和CH2(COOC2H5)2为有机反应原料制备![]() 的合成路线流程图(注明反应条件)_______。合成路线流程图示例如下:
的合成路线流程图(注明反应条件)_______。合成路线流程图示例如下:
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香料M的一种合成流程如下:
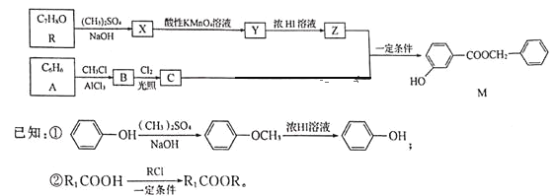
请回答下列问题:
(1)M中含碳的官能团名称是__;设计R→X和Y→Z步骤的目的是__。
(2)A→B的反应类型是___,B的名称是___。
(3)R分子中最多有__个原子共平面。
(4)R和M在下列仪器中信号完全相同的是___(填字母)。
a.质谱仪 b.元素分析仪 c.红外光谱仪 d.核磁共振氢谱仪
(5)写出C和Z反应生成M的化学方程式:___。
(6)在Y的同分异构体中,同时满足下列条件的结构有___种(不考虑立体异构)。
①能发生银镜反应
②遇氯化铁溶液发生显色反应
③1mol有机物最多能消耗3molNaOH
(7)已知苯环上有烃基时,新引入取代基主要取代邻位、对位氢原子。参照上述合成流程,设计以苯和异丙醇为原料制备Br![]() 的合成路线:___(无机试剂任选)
的合成路线:___(无机试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸俗称草酸(结构简式为HOOC﹣COOH,可简写为H2C2O4),它是一种重要的化工原料.(常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示.)
H2C2O4 | KHC2O4 | K2C2O4 | |
pH | 2.1 | 3.1 | 8.1 |
填空:
(1)写出H2C2O4的电离方程式_______.
(2)KHC2O4溶液显酸性的原因是_____;向0.1mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是______.
a.c(K+)=c(HC2O4﹣)+c(H2C2O4)+c(C2O42﹣)
b.c(Na+)=c(H2C2O4)+c(C2O42﹣)
c.c(K+)+c(Na+)=c(HC2O4﹣)+c(C2O42﹣)
d.c(K+)>c(Na+)
(3)H2C2O4与酸性高锰酸钾溶液反应,现象是有气泡(CO2)产生,紫色消失.写出反应的离子方程式______;又知该反应开始时速率较慢,随后大大加快,可能的原因是_______.
(4)某同学设计实验如图所示:两个烧杯中的试管都分别盛有2mL 0.1 mol/L H2C2O4溶液和4mL 0.1mol/L 酸性KMnO4溶液,分别混合并振荡,记录溶液褪色所需时间.该实验目的是研究________,但该实验始终没有看到溶液褪色,推测原因_______.
(5)已知草酸(H2C2O4)受热分解的化学方程式为:H2C2O4→H2O+CO↑+CO2↑,写出FeC2O4在密闭容器中高温分解的化学方程式________.

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com