
����Ŀ��������(H3PO2)��һ�־�ϸ������Ʒ������һԪ���ᣬ���н�ǿ�Ļ�ԭ�ԡ������й�˵����ȷ����
A. �ö��Ե缫���NaH2PO2��Һ����������ӦʽΪ��2H2O-4e-=O2��+4H+
B. H3PO2�����NaOH��Һ��Ӧ�����ӷ���ʽΪ��H3PO2+3OH-=PO23-+3H2O
C. ��H3PO2��Һ���뵽�����ظ������Һ�У�H3PO2�Ļ�ԭ�������ΪH3PO4
D. H3PO2����ˮ�ĵ��뷽��ʽΪH3PO2![]() H++ H2PO2-
H++ H2PO2-
���𰸡�D
��������A��H3PO2���н�ǿ�Ļ�ԭ�ԣ����ʱ��������H2PO2-ʧ���ӣ������ö��Ե缫���NaH2PO2��Һ����������ӦʽΪ��H2PO2--4e-+2H2O�TH3PO4+3H+��ѡ��A����B��һԪ������NaOH�������ʵ���1��1��Ӧ������H3PO2�����NaOH��Һ��Ӧ�����ӷ���ʽΪ��H3PO2+OH-�TH2PO2-+H2O��ѡ��B����C��H3PO2���л�ԭ�ԣ��ܱ����������������H3PO2��Һ���뵽���Ը��������Һ�У�H3PO2����������ΪH3PO4��ѡ��C����D��һԪ��������Һ�в��ֵ����һ�������ӣ���H3PO2����ˮ�ĵ��뷽��ʽΪ��H3PO2H++H2PO2-��ѡ��D��ȷ����ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ӻ�������ȡ���ʵ������У��漰�����в�����������ȷ����
A. ���������ճɻ�
B. ���˵ú�I����Һ
C. ��ȡ������ų���ı���Һ
D. ����Ⲣ���ձ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������㷺����ұ�𡢻�������ҵ����Ҫ����ұ������������ұ�����Ӽ���ռ��������������������80%���ϣ�����������л������Ĵ�����Ϊ������V2O5�����������ǴӷϷ�����(��Ҫ�ɷ�V2O5��VOSO4��K2SO4��SiO2��Fe2O3��)�л���V2O5��һ��������������ʾ��ͼ���£�
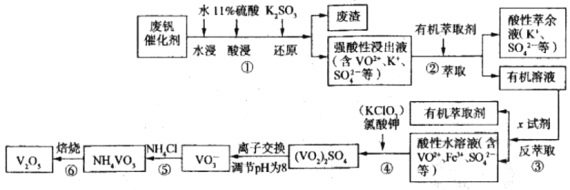
(1)���з�������Ҫ�ɷ���__________________________��
����V2O5������Ӧ�����ӷ���ʽΪ________________________________________��
(2)�������еı仯���̿ɼ�Ϊ(��ʽ�е�R��ʾVO2+��Fe3+��HA��ʾ�л���ȡ������Ҫ�ɷ�)��R2(SO4) (ˮ��)+2nHA(�л���) ![]() 2RAn(�л���)+nH2SO4(ˮ��)��
2RAn(�л���)+nH2SO4(ˮ��)��
������ȡʱ��������������ԭ����________________________________________��
ʵ���ҽ�����ȡ����ʹ�õIJ�������Ϊ________________________________________��
(3)ʵ�����õ�ԭ����V2O5ռ6%(ԭ���е����з��ѻ����V2O5)��ȡ100g�÷Ϸ���������ҵ�����IJ������ʵ�鵱����100ml0.1mol/L��KClO3��Һʱ����Һ�еķ�ǡ�ñ���ȫ�����������Ժ������û����ʧ�����ʵ���з��Ļ�������________________[M(V2O5)=182g/mol]
(4)25��ʱȡ����������������õ��������ʺ���ҺpH֮��Ĺ�ϵ���±���

���ж���ʵ������ʱ�����м��백ˮ������Һ�����pHΪ_________������������Ϊ93.1%ʱ������Fe(OH)3���������ʱ��Һ��c(Fe2+)��__________����֪��25��ʱKsp[Fe(OH)3]=2.6��10��39
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڿ��淴ӦH2(g) + I2(g)![]() 2HI(g)���ں���ʱ��H2(g)��I2(g)��ʼ��Ӧ������˵����ȷ����
2HI(g)���ں���ʱ��H2(g)��I2(g)��ʼ��Ӧ������˵����ȷ����
A. H2(g)������������HI(g)���������ʱ�Ϊ2:1
B. ����ѹǿ��ͨ���ı����ʵ����������������ɫ����
C. �����淴Ӧ���ʵı�ֵ�Ǻ㶨��
D. �ﵽƽ��ʱ����ͬ�����ʱ�ʾ�������淴Ӧ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ľ̿ĥ��ֱ��Ϊ10nm���ҵ�̿�����ٷ�ɢ��ijҺ���ɢ���У������÷�ɢϵ��������ȷ���ǣ� ��
��һ������Һ ���ж����ЧӦ ����ȫ������Ĥ �ܿ���ȫ������ֽ
A.�٢�B.�ڢ�C.�ڢ�D.�ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪H2SO3��I2��H2O == H2SO4��2HI����0.1mol Cl2ͨ��100mL�������ʵ�����HI��H2SO3�Ļ����Һ������һ���HI��������������˵����ȷ����
A. ���ʵĻ�ԭ����HI��H2SO3��HCl
B. H2SO3�����ʵ���Ũ��Ϊ0.6 mol��L��1
C. ����ͨ��0.05mol Cl2��ǡ���ܽ�HI��H2SO3��ȫ����
D. ͨ��0.1mol Cl2������Ӧ�����ӷ���ʽΪ��5Cl2��4H2SO3��2I����4H2O == 4SO42����I2��10Cl����16H��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���⻯�(NH4H)���Ȼ�淋Ľṹ���ƣ�����ˮ��Ӧ���������ɡ����й����⻯�������ȷ����
A. �����ӻ�����������Ӽ����ۼ�
B. ����ʽ��
C. ��ˮ��Ӧʱ��NH4H��������
D. ����Ͷ��������ˮ�У�ֻ����һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ�ѵ���������һ�ַ������ڷ�ˮ�м���NaClOʹNH4+��ȫת��ΪN2���÷�Ӧ�ɱ�ʾΪ2NH4++3ClO-=N2��+3Cl-+2H++3H2O������˵���У�����ȷ���ǣ� ��
A.��Ӧ�е�Ԫ�ر�����
B.��ԭ��NH4+��Cl-
C.��Ӧ����Ԫ�ر���ԭ
D.���˷��������ķ�ˮ����ֱ���ŷ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ǽ�������,���ж�������������У��ж������ڿ�ѧ���������ԵĴ���
������ʳƷ�ɴ���Ȼ�����Ƴɣ������κ����࣬������Ҳ�ɷ��Ĵ���ʳ��
���������Ϻ��ж������Σ�����Ч���������˶�ʱ���ĵ�����
�����ֿ�Ȫˮ������������IJ��ִ���Ԫ�غ���Ԫ��
�����ֿڷ�Һ���зḻ�ĸơ�����п��������Ԫ��
A. 1�� B. 2�� C. 3�� D. 4��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com