
【题目】五氧化二钒广泛用于冶金、化工等行业,主要用于冶炼钒铁、用作冶金添加剂,占五氧化二钒总消耗量的80%以上,其次是用作有机化工的催化剂。为了增加V2O5的利用率我们从废钒催化剂(主要成分V2O5、VOSO4、K2SO4、SiO2和Fe2O3等)中回收V2O5的一种生产工艺流程示意图如下:
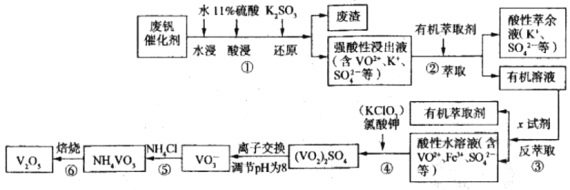
(1)①中废渣的主要成分是__________________________;
①中V2O5发生反应的离子方程式为________________________________________。
(2)②、③中的变化过程可简化为(下式中的R表示VO2+或Fe3+,HA表示有机萃取剂的主要成分):R2(SO4) (水层)+2nHA(有机层) ![]() 2RAn(有机层)+nH2SO4(水层)。
2RAn(有机层)+nH2SO4(水层)。
②中萃取时必须加入适量碱,其原因是________________________________________;
实验室进行萃取操作使用的玻璃仪器为________________________________________。
(3)实验室用的原料中V2O5占6%(原料中的所有钒已换算成V2O5)。取100g该废钒催化剂按工业生产的步骤进行实验当加入100ml0.1mol/L的KClO3溶液时,溶液中的钒恰好被完全处理,假设以后各步钒没有损失,则该实验中钒的回收率是________________[M(V2O5)=182g/mol]
(4)25℃时取样进行试验分析,得到钒沉淀率和溶液pH之间的关系如下表:

试判断在实际生产时,⑤中加入氨水调节溶液的最佳pH为_________;若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则此时溶液中c(Fe2+)≤__________。已知:25℃时Ksp[Fe(OH)3]=2.6×10-39
【答案】SiO2 V2O5+4H++SO32- = 2VO2++ SO42-+2H2O 加入碱,中和H2SO4,使平衡向正向移动 分液漏斗、烧杯 91.0% 1.7 2.6![]() 10-3 mol/L
10-3 mol/L
【解析】
生产流程:废钒催化剂(主要成分V2O5、Fe2O3和SiO2等),据物质的水溶性确定,V2O5和SiO2难溶于水。亚硫酸根具有还原性,酸性条件下,能被五氧化二钒氧化生成硫酸根离子,过滤得到滤渣为二氧化硅,强酸性浸出液含有VO2+、K+、SO42-,加入有机萃取剂萃取分液得到有机溶液中VO2+,再加入X试剂进行反萃取分液,分离出有机层,得到水层是含VO2+、Fe3+、SO42-的酸性水溶液,分析平衡R2(SO4) (水层)+2nHA(有机层) ![]() 2RAn(有机层)+nH2SO4(水层),加入的碱会和平衡中的氢离子反应促进平衡正向进行。具有氧化性的氯酸钾,能将VO2+氧化为VO2+,加入氨水,调节溶液pH到最佳值,得到NH4VO3,最后焙烧得到五氧化二钒,据此分析作答,
2RAn(有机层)+nH2SO4(水层),加入的碱会和平衡中的氢离子反应促进平衡正向进行。具有氧化性的氯酸钾,能将VO2+氧化为VO2+,加入氨水,调节溶液pH到最佳值,得到NH4VO3,最后焙烧得到五氧化二钒,据此分析作答,
(1)SiO2难溶于水、难溶于酸;根据氧化还原规律、电荷守恒、电子守恒及原子守恒配平离子方程式;
(2)从加入能反应的离子对平衡移动的影响来分析;结合萃取操作步骤选取实验仪器;
(3)根据④⑤⑥操作步骤流程图可知,氯酸钾能将VO2+氧化为VO2+,再结合物质之间的转化关系式及题意来计算钒的回收率;
(4)从沉淀率和pH关系找出最佳沉淀率,钒沉淀率为93.1%时不产生Fe(OH)3沉淀,此时溶液pH=2,计算氢氧根离子浓度,结合溶度积常数计算溶液中铁离子的浓度。
(1)上述分析可知滤渣A为SiO2,从流程图可以看出,在酸性条件下,V2O5转化为VO2+,SO32-能被V2O5氧化生成SO42-,根据氧化还原反应的规律配平该离子反应方程式为:V2O5+SO32-+4H+=2VO2++SO42-+2H2O,
故答案为:SiO2;V2O5+SO32-+4H+=2VO2++SO42-+2H2O;
(2)反萃取时,分析平衡R2(SO4) (水层)+2nHA(有机层) ![]() 2RAn(有机层)+nH2SO4(水层),为提高②中萃取百分率,则加入碱中和硫酸,可以使平衡正移,多次连续萃取。萃取分液操作时,用到的玻璃仪器有分液漏斗和烧杯;
2RAn(有机层)+nH2SO4(水层),为提高②中萃取百分率,则加入碱中和硫酸,可以使平衡正移,多次连续萃取。萃取分液操作时,用到的玻璃仪器有分液漏斗和烧杯;
故答案为:加入碱,中和H2SO4,使平衡向正向移动;分液漏斗、烧杯;
(3)根据氧化还原规律可知,当加入100ml 0.1mol/L的KClO2溶液时,溶液中的钒恰好被完全处理的离子方程式为:ClO3-+6VO2++3H2O=6VO2++6H++Cl-,再结合V2O5+SO32-+4H+=2VO2++SO42-+2H2O,从而得出关系式: 3 V2O5~6VO2+~ClO3-,因n(ClO3-) = 0.1 mol/L![]() 0.1 L = 0.01 mol,所以n(V2O5)=3
0.1 L = 0.01 mol,所以n(V2O5)=3![]() 0.01 mol = 0.03 mol 因此该实验中钒的回收率是
0.01 mol = 0.03 mol 因此该实验中钒的回收率是![]() ×100% = 91.0 %,
×100% = 91.0 %,
故答案为:91.0 %;
(4)从沉淀率和pH关系找出最佳沉淀率。若钒沉淀率为93.1%时,不产生Fe(OH)3沉淀,此时溶液pH=2,计算氢氧根离子浓度,结合溶度积常数计算溶液中铁离子的浓度。
由表中数据可知,pH = 1.7时钒的沉淀率最大为98.8%,故加入氨水调节溶液的最佳pH为为1.7。若钒沉淀率为93.1 %时不产生Fe(OH)3沉淀,此时溶液pH=2,c(OH)=1012 mol/L,Ksp[Fe(OH)3] = 2.6×10-39 =c(Fe3+)c3(OH),c(Fe3+) = ![]() =2.6×10 mol/L,
=2.6×10 mol/L,
故答案为:1.7;2.6×103 mol/L。


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:
【题目】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。

下列说法不正确的是( )
A. 生成CH3COOH总反应的原子利用率为100%
B. CH4→CH3COOH过程中,有C―H键发生断裂
C. ①→②吸收能量并形成了C―C键
D. 该催化剂选择性活化了甲烷分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:

请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为_________________________。
(2)灼烧用的仪器_________________填名称)。
(3)沉淀A的成分是______________(填化学式)。
(4)冶炼铝的化学方程式__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】晶体硅是良好的半导体材料,多晶硅主要采用SiHCl3还原工艺生产。
(1)硅原子核外有_____种能量不同的电子。氯离子的核外电子排布式为________________________。短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是________。
(2)从原子结构角度解释硅元素与氯元素的非金属性强弱________________________。
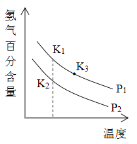
(3)900℃以上发生SiHCl3(g)+H2(g)![]() Si(s)+3HCl(g)反应,平衡时H2的百分含量随温度、压强(P)变化如图(K为不同条件时得平衡常数)。从化学反应速率角度来说明上述反应已达到平衡状态_______。
Si(s)+3HCl(g)反应,平衡时H2的百分含量随温度、压强(P)变化如图(K为不同条件时得平衡常数)。从化学反应速率角度来说明上述反应已达到平衡状态_______。
(4)若反应容器的容积为2L,10min后达到平衡,测得固体的质量增加了2.8g,则HCl的平均反应速率为______________。
(5)P1____P2(选填“>”、“<”或“=”);K1、K2、K3大小关系式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,CO和CH4燃烧的热化学方程式为:CO(g)+1/2O2=CO2(g);△H=-283KJ/mol
CH4(g)+2O2=CO2(g)+2H2O(g);△H=-890KJ/mol,现有4mol CO和CH4组成的混合气体在上述条件下完全燃烧时,释放的热量为2953KJ,则CO和CH4的体积比
A. 1:3 B. 3:1 C. 1:2 D. 2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
SO2(g)+2CO(g)![]() 2CO2(g)+S(l)△H<0 若反应在恒容的密闭容器中进行,下列有关说法正确的是
2CO2(g)+S(l)△H<0 若反应在恒容的密闭容器中进行,下列有关说法正确的是
A. 平衡前,随着反应的进行,容器内压强始终不变
B. 平衡时,其他条件不变,分离出硫,正反应速率加快
C. 平衡时,其他条件不变,升高温度可提高SO2的转化率
D. 其他条件不变,使用不同催化剂,该反应平衡常数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应A+a B(g)![]() C(g)+2 D(g)(a为化学计量数)。反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图所示。下列说法正确的是
C(g)+2 D(g)(a为化学计量数)。反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图所示。下列说法正确的是

A. T2< T1,P2< P1
B. 增加B的物质的量,B的转化率一定增大
C. 若a=2,则A为固态或液态物质
D. 该反应的正反应为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。下列有关说法正确的是
A. 用惰性电极电解NaH2PO2溶液,其阳极反应式为:2H2O-4e-=O2↑+4H+
B. H3PO2与过量NaOH溶液反应的离子方程式为:H3PO2+3OH-=PO23-+3H2O
C. 将H3PO2溶液加入到酸性重铬酸钾溶液中,H3PO2的还原产物可能为H3PO4
D. H3PO2溶于水的电离方程式为H3PO2![]() H++ H2PO2-
H++ H2PO2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是 ( )

A. 原子半径:Z> W>X>Y
B. 氧化物对应水化物的酸性:W>Z>X
C. 四种元素氢化物的沸点:W> Z>Y>X
D. 四种元素对应阴离子的还原性:W> Z>Y>X
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com