
【题目】常温下,下列溶液一定呈酸性的是
A.一定体积![]() 的NaOH溶液加水稀释
的NaOH溶液加水稀释![]() 倍
倍
B.![]()
![]() 某碱溶液和
某碱溶液和![]()
![]() 盐酸等体积混合
盐酸等体积混合
C.![]()
![]() 氨水和
氨水和![]()
![]() 氯化铵溶液等体积混合
氯化铵溶液等体积混合
D.![]() 的NaOH溶液与
的NaOH溶液与![]() 的
的![]() 溶液等体积混合
溶液等体积混合
科目:高中化学 来源: 题型:
【题目】反应mX(g)![]() nY(g)+pZ(g) ΔH,在不同温度下的平衡体系中物质Y的体积分数随压强变化的曲线如图所示,下列说法错误的是( )
nY(g)+pZ(g) ΔH,在不同温度下的平衡体系中物质Y的体积分数随压强变化的曲线如图所示,下列说法错误的是( )

A. 该反应的ΔH>0
B. m<n+p
C. B、C两点化学平衡常数:KB>KC
D. A、C两点的反应速率v(A)<v(C)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】许多金属及他们的化合物在科学研究和工业生产中具有许多用途,回答下列有关问题
![]() 下列有关的说法正确的是 ______
下列有关的说法正确的是 ______
A、第一电离能大小:![]()
B、因为晶格能CaO比KCl高,所以KCl比CaO熔点低
C、![]() 与
与![]() 的化学性质类似,分子结构也都呈直线型,相同条件下
的化学性质类似,分子结构也都呈直线型,相同条件下![]() 的溶解度更大
的溶解度更大
D、分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
![]() 镍
镍![]() 可形成多种配合物,且各种配合物有广泛的用途。某镍配合物结构如图所示,分子内含有的作用力有 ______
可形成多种配合物,且各种配合物有广泛的用途。某镍配合物结构如图所示,分子内含有的作用力有 ______ ![]() 填序号
填序号![]()

A.氢键 ![]() 离子键
离子键 ![]() 共价键 D.金属键
共价键 D.金属键 ![]() 配位键
配位键
组成该配合物分子且同属第二周期元素的电负性由大到小的顺序是 ______ ![]() 甲基
甲基![]() 中C原子的杂化方式为 ______
中C原子的杂化方式为 ______
![]() 铁和铜在生产和生活中有重要应用,基态
铁和铜在生产和生活中有重要应用,基态![]() 的M层电子排布式为 ______ ,用晶体的x射线衍射发可以测得阿伏伽德罗常数,对金属铜的测定得到以下结果:晶胞为面心立方最密堆积,边长为
的M层电子排布式为 ______ ,用晶体的x射线衍射发可以测得阿伏伽德罗常数,对金属铜的测定得到以下结果:晶胞为面心立方最密堆积,边长为![]() 提示:
提示:![]() ,
,![]() ,又知铜的密度为
,又知铜的密度为![]() ,则铜晶胞的质量是 ______
,则铜晶胞的质量是 ______ ![]() 保留两位小数
保留两位小数![]() ;阿伏加德罗常数为 ______
;阿伏加德罗常数为 ______ ![]() 保留两位小数
保留两位小数![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10mL0.1mol/LNaOH溶液中加入0.1mol/L的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是( )

A.a点溶液中:c(Na+)>c(A-)>c(H+)>c(HA)
B.a、c两点溶液中水的电离程度相同
C.b点溶液中:c(Na+)=c(A-)+c(HA)
D.c点溶液中:c(A-)>c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种以软锰矿(主要成分为MnO2、SiO2、Al2O3)和黄铁矿(FeS2、SiO2)为原料冶炼金属锰的工艺流程如图所示:

已知相关金属离子[c(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH如下:
金属离子 | Fe3+ | Mn2+ | Al3+ |
开始沉淀的pH | 2.7 | 8.3 | 3.2 |
沉淀完全的pH | 3.7 | 9.8 | 5.0 |
回答下列问题:
(1)MnO2本身不能溶于硫酸,但是在Fe2+的作用下却能溶解,写出该反应的离子方程式:____________________________。
(2)滤渣1的成分除了SiO2外,还有一种淡黄色的物质是_______________(填化学式)。
(3)除杂步骤中加入的MnCO3的作用是____________________________,该过程需调节溶液pH的范围是___________________________,若把pH调得过高,其后果是_________________________。
(4)用惰性电极进行电解,电解刚开始时阴极的电极反应式为____________________,电解后阳极的电解质溶液可返回_______________________(填“酸浸”“除杂”或“电解”)工序继续使用。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯的叠氮酸(HN3)是一种弱酸,常温下向25mL 0.1 mol/L NaOH溶液中加入0.2 mol/L HN3溶液,滴加过程中的pH值的变化曲线(溶液混合时的体积变化忽略不计)如下图。下列说法正确的是( )
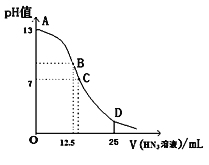
A. 该滴定过程中应用甲基橙作指示剂
B. 若B点pH=8,则c(HN3)=(10-6~10-8 )mol/L
C. 点D对应溶液中存在关系:c(HN3)>c(Na+)>c(N3-)
D. 沿曲线A→B→C的过程中,由水电离产生的c(OH-)逐渐减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,回答下列关于盐酸和醋酸溶液的问题:
①对于![]() 的盐酸和
的盐酸和![]() 的醋酸溶液的pH:盐酸______
的醋酸溶液的pH:盐酸______![]() 选填“
选填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() 醋酸,写出醋酸的电离方程式______
醋酸,写出醋酸的电离方程式______![]() 若用同浓度的NaOH溶液分别中和等体积且pH相等的盐酸和醋酸溶液,则消耗NaOH溶液的体积关系为:前者______后者
若用同浓度的NaOH溶液分别中和等体积且pH相等的盐酸和醋酸溶液,则消耗NaOH溶液的体积关系为:前者______后者![]() 选填“
选填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() .
.
②两种酸均能与氢氧化钠反应生成盐,其中醋酸能与氢氧化钠反应生成醋酸钠.实验室现有醋酸钠固体,取少量溶于水,溶液呈______![]() 选填“酸性”、“中性”或“碱性”
选填“酸性”、“中性”或“碱性”![]() ,其原因是
,其原因是![]() 用离子方程式表示
用离子方程式表示![]() ______.
______.
③向醋酸溶液中加入一定量的NaOH溶液,当测得溶液的![]() 时,溶液中离子物质的量的浓度大小关系为______;当测得溶液的
时,溶液中离子物质的量的浓度大小关系为______;当测得溶液的![]() 时,溶液中离子物质的量的浓度大小关系可能为
时,溶液中离子物质的量的浓度大小关系可能为![]() 写出一种关系即可
写出一种关系即可![]() ______.
______.
④已知![]() 时,
时,![]() 的醋酸溶液的pH约为3,向其中加入少量醋酸钠晶体,发现溶液的pH增大.对上述现象有两种不同的解释:甲同学认为醋酸钠呈碱性,所以溶液的pH增大;乙同学给出另外一种不同于甲同学的解释,请你写出乙同学可能的理由______.
的醋酸溶液的pH约为3,向其中加入少量醋酸钠晶体,发现溶液的pH增大.对上述现象有两种不同的解释:甲同学认为醋酸钠呈碱性,所以溶液的pH增大;乙同学给出另外一种不同于甲同学的解释,请你写出乙同学可能的理由______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实能用勒夏特列原理解释的是
A. 工业制硫酸采用二氧化硫催化氧化,高温可以提高单位时间SO3的产量
B. 合成氨工业中使用铁触媒做催化剂
C. 用饱和食盐水除去氯气中氯化氢杂质
D. 容器中有2HI(g)![]() H2(g)+I2(g),增大压强颜色变深
H2(g)+I2(g),增大压强颜色变深
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com