
ʵ���е����в�����ȷ����
A�����Թ�ȡ���Լ�ƿ�е�Na2CO3��Һ������ȡ�����࣬Ϊ�˲��˷ѣ��ְѹ������Լ������Լ�ƿ��
B��Ba��NO3��2 ����ˮ���ɽ�����Ba��NO3��2 �ķ�Һ����ˮ���У�����ˮ������ˮ��
C������������ʹNaCl ����Һ������ʱ��Ӧ����������NaCl ��Һȫ����������
D����Ũ��������һ�����ʵ���Ũ�ȵ�ϡ����ʱ��Ũ��������ˮ��Ӧ��ȴ�����²���ת�Ƶ�����ƿ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���������һ�и߶������в������ƻ�ѧ�Ծ��������棩 ���ͣ�������
��12�֣���2L�ܱ������У�����1 mol N2��3mol H2��һ�������·����ϳɰ���Ӧ��2minʱ�ﵽƽ�⡣���ƽ��ʱN2��ת����Ϊ40%����
��1��ƽ��ʱv ��NH3��������
��2������¶��µ�ƽ�ⳣ��K���г���ʽ�����ü���������
��3��H2��ƽ���������е��������
��4��ƽ��ʱ������ѹǿ����ʼʱѹǿ֮��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������ʵ����ѧ��һ��10�½β⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
����ӵ�����Ϊ6?02��1023 mol?1�����������в���ȷ����
A��0��1 mol OH-����6?02��1023 ������
B���Ȼ��������Ħ����������6?02��1023���Ȼ�����ӵ�����֮��
C��1 mol�����������6?02��1023��������ӵ��������
D��28 g����������ԭ����ĿΪ12?04��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ɹŰ������߶���10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
X��Y��Z�������壬��X��Y��1��2�����ʵ���֮�Ȼ�ϲ�ͨ���ܱ��������з�Ӧ��X��2Y 2Z�����ﵽ��ѧƽ��ʱ����Ӧ�������ʵ����������������ʵ�����ȣ���ʱx��ת������
2Z�����ﵽ��ѧƽ��ʱ����Ӧ�������ʵ����������������ʵ�����ȣ���ʱx��ת������
A��70% B��60% C��50% D��40%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ɹŰ�������һ��10���¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
���ܶ�Ϊ1��84g/mL����������Ϊ98%��Ũ��������100 ml 3��0mol/L ϡ�����ʵ�鲽�����£��ټ�������Ũ�������� ����ȡһ�������Ũ���� ��ϡ�� ��ת�� ��ϴ�� ���� ��ҡ��
��1������Ũ���������� ��
��2���ڢ۲�ʵ��IJ����� ��
��3���ڢ�ʵ��IJ����� ��
��4����������������Ƶ�ϡ����Ũ���к�Ӱ�죿������ĸ��дa��ƫ�� b��ƫ�� c����Ӱ�죩
A�����õ�Ũ���᳤ʱ��������ܷⲻ�õ�������
B������ƿ������ϴ�Ӻ������������ˮ
C�����ù����ձ���������δϴ��
D����ȡŨ����ʱ������Ͳ�ϵĿ̶�ȡ��Ũ����
E������ʱ���μ�����ˮ����ʹҺ���Ը��ڿ̶��ߣ�����������ˮʹҺ�氼����̶�������
F�����ݺ�ҡ�ȣ�����Һ�潵�ͣ��ֲ�������ˮ�����´ﵽ�̶���
��5����ʵ�����˷�ʱ��ĵط��ǽ�ϡ�ͺ��������ȴ�����£�Ϊ�˽�Լʱ�䣬�����еļ�
��ϡ������ȴ�ķ�����_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
ijʵ��С����0��50 mol��L-1NaOH��Һ��0��50 mol��L-1������Һ�����к��ȵIJⶨ��
������0��50 mol��L-1NaOH��Һ
��1����ʵ���д�ԼҪʹ��245mLNaOH��Һ��������Ҫ����NaOH���� g��
��2������ͼ��ѡ�����NaOH��������Ҫ�������ǣ�����ĸ���� ��
���� | ������ƽ �������룩 | С�ձ� | ����ǯ | ������ | ҩ�� | ��Ͳ |
���� |
|
|
|
|
|
|
��� | a | b | c | d | e | f |
�ⶨϡ�����ϡ���������к��ȵ�ʵ��װ����ͼ��ʾ��
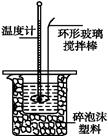
��1��д���÷�Ӧ�к��ȵ��Ȼ�ѧ����ʽ�����к���Ϊ57��3 kJ��mol-1�� ��
��2��ȡ50 mLNaOH��Һ��30 mL������Һ����ʵ�飬ʵ���������±���
������� | ��ʼ�¶�t1/�� | ��ֹ�¶� t2/�� | �¶Ȳ�ƽ��ֵ ��t2��t1��/�� | ||
H2SO4 | NaOH | ƽ��ֵ | |||
1 | 26��2 | 26��0 | 26��1 | 29��6 | |
2 | 27��0 | 27��4 | 27��2 | 31��2 | |
3 | 25��9 | 25��9 | 25��9 | 29��8 | |
4 | 26��4 | 26��2 | 26��3 | 30��4 | |
���ϱ��е��¶Ȳ�ƽ��ֵΪ �档
�ڽ�����Ϊ0��50 mol��L-1 NaOH��Һ��0��50 mol��L-1������Һ���ܶȶ���1 g��cm-3���кͺ�������Һ�ı�����c=��4��18�� J����g���棩-1�����к��Ȧ�H= ��ȡС�����һλ����
������ʵ����ֵ�����57��3 kJ��mol-1��ƫ�����ƫ���ԭ������ǣ�����ĸ�� ��
a��ʵ��װ�ñ��¡�����Ч����
b����ȡNaOH��Һ�����ʱ���Ӷ���
c���ֶ�ΰ�NaOH��Һ����ʢ�������С�ձ���
d�����¶ȼƲⶨNaOH��Һ��ʼ�¶Ⱥ�ֱ�ӲⶨH2SO4��Һ���¶�
��ʵ���и���60mL0��5mol/L�����50mL0��55moi/L�������ƽ��з�Ӧ��������ʵ����ȣ����ų������� ������Ȼ���ȣ���ͬ��������ĵ��к��� �������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����Ȼ�ѧ����ʽ�У���ȷ����
A�������ȼ����Ϊ890��3kJ/mol�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��
CH4��g��+2O2��g��==CO2��g��+2H2O��g����H=-890��3kJ/mol
B��500�桢30MPa�£���0��5mol N2��1��5molH2�����ܱյ������г�ַ�Ӧ����NH3��g��������19��3kJ�����Ȼ�ѧ����ʽΪ��N2��g��+3H2��g�� 2NH3��g����H=-38��6kJ/mol
2NH3��g����H=-38��6kJ/mol
C��NaOH��s��+1/2 H2SO4��Ũ��==1/2Na2SO4��aq��+H2O��l����H=-57��3kJ/mol
D��2��00gC2H2������ȫȼ������Һ̬ˮ�Ͷ�����̼���壬�ų�99��6kJ���������÷�Ӧ���Ȼ�ѧ����ʽΪ��2C2H2��g��+5O2��g��==4CO2��g��+2H2O��l����H=-2589��6kJ/moL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ������ѧ�ڵڶ��μ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA ��ʾ�����ӵ�������ֵ������˵����ȷ����
A��2��8 g һ����̼����ϩ�Ļ��������������̼ԭ����ĿΪ0��1NA
B����״����5��6 L N2O ���������ĵ�����Ϊ5��5NA
C���ö��Ե缫���CuCl2��Һ�����õ�0��1NA ��Cu ԭ��ʱ����������2��24 L ����
D��0��1 mol��L-1 ��NaCl ��Һ�У�Na+��Cl-������ĿΪ0��2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���Ĵ�������ѧ��һ��10�½β⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
���к� NaCl��Na2SO4��NaNO3�Ļ����Һ�� ��������ʵ�����̼����ʵ����Լ�����ת��Ϊ��Ӧ�ij�������壬ʵ�� Cl����SO42���� NO3-������룺�����Լ� 1��2��4 �ֱ�Ϊ
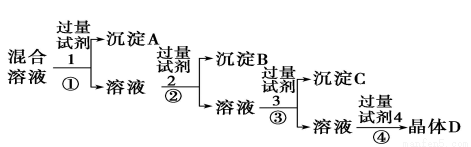
A����������Һ ���ᱵ��Һ ϡ����
B���Ȼ�����Һ ϡ���� ��������Һ
C������������Һ ��������Һ ϡ����
D���Ȼ�����Һ ��������Һ ϡ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com