
【题目】Cl2是一种重要的化工原料, 氯气极其相关产品在生产生活中应用广泛。结合氯气的相关知识解决下列问题;
(1)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上生产漂白粉的主要化学方程式是______________________;漂白粉的有效成分是(填化学式)_________。漂白粉在空气中长期存放会变质而失效的原理是(用化学方程式说明) _____________。
(2)实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是 MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O 由于氯气有毒所以实验室通常用___________________溶液吸收尾气(填化学式),反应的化学方程式为_____________________。
MnCl2+Cl2↑+2H2O 由于氯气有毒所以实验室通常用___________________溶液吸收尾气(填化学式),反应的化学方程式为_____________________。
(3)氯气是一种常用的消毒剂,新制氯水含多种微粒并表现出不同的性质(用化学式或离子符号填写):
使氯水呈黄绿色的是________;能使AgNO3溶液产生白色沉淀的是________;能使紫色石蕊试液显红色的是________;能使红纸褪色的是________。
【答案】2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O Ca(ClO)2 Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO、2HClO![]() 2HCl+O2↑ NaOH Cl2+2NaOH=NaCl+NaClO+H2O Cl2 Cl- H+ HClO
2HCl+O2↑ NaOH Cl2+2NaOH=NaCl+NaClO+H2O Cl2 Cl- H+ HClO
【解析】
(1)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上生产漂白粉利用的是氯气与氢氧化钙反应,反应的化学方程式是2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;漂白粉的有效成分是次氯酸钙,化学式为Ca(ClO)2。漂白粉在空气中长期存放会变质是因为次氯酸钙吸收空气中的水和二氧化碳生成次氯酸,次氯酸不稳定分解而失效,反应的化学方程式为Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO、2HClO![]() 2HCl+O2↑。
2HCl+O2↑。
(2由于氯气有毒,所以实验室通常用NaOH溶液吸收尾气,反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O。
(3)氯气是一种常用的消毒剂,新制氯水含多种微粒并表现出不同的性质。由于氯气是黄绿色气体,则使氯水呈黄绿色的是Cl2;氯离子能与银离子结合生成氯化银白色沉淀,能使AgNO3溶液产生白色沉淀的是Cl-;酸能使紫色的石蕊试液显红色,则能使紫色石蕊试液显红色的是H+;次氯酸具有漂白性,则能使红纸褪色的是HClO。


科目:高中化学 来源: 题型:
【题目】人们用NH4Cl溶液来处理废切削液,使NaNO2转化为无毒物质。该反应分两步进行:第一步:NaNO2+NH4Cl===NaCl+NH4NO2 第二步:NH4NO2![]() N2↑+2H2O,下列叙述中正确的是
N2↑+2H2O,下列叙述中正确的是
①两步反应中N元素都被氧化 ②NH4Cl在反应中充当还原剂
③NaNO2在反应中充当氧化剂 ④第二步中只有氮元素的化合价发生了变化
⑤NH4NO2既是氧化剂又是还原剂
A. ①③ B. ①④ C. ②③④ D. ④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】开发新能源是解决环境污染的重要举措,其中甲醇、乙醇、甲烷都是优质的清洁燃料,可制作燃料电池。
(1)已知:①C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ΔH1=-1366.8kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566.0kJ/mol
③H2O(g)=H2O(l) ΔH3=-44 kJ/mol。
乙醇不完全燃烧生成一氧化碳和液态水的热化学方程式为:______________________。
(2)可利用甲醇燃烧反应设计一个燃料电池。如下图1,用Pt作电极材料,用氢氧化钾溶液作电解质溶液,在两个电极上分别充入甲醇和氧气。
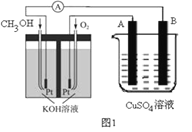
①写出燃料电池负极的电极反应式_________________。
②若利用该燃料电池提供电源,与图1右边烧杯相连,在铁件表面镀铜,则铁件应是_______极(填“A”或“B”);当铁件的质量增重6.4g时,燃料电池中消耗氧气的标准状况下体积为________L。
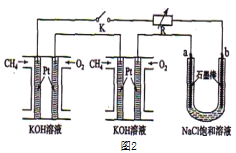
(3)某研究小组将两个甲烷燃料电池串联后如上图2作为电源,进行饱和氯化钠溶液电解实验若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上通过电解池的电量表达式为_____________(法拉第常数F=9.65×l04C/ mol),最多能产生的氯气体积为_____L(标准状况)。
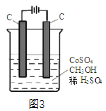
(4)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+在阳极氧化成Co3+,生成的Co3+将甲醇氧化成CO2和H+(用石墨烯除去Co2+),现用如图3所示装置模拟上述过程,则Co2+在阳极的电极反应式为________________________除去甲醇的离子方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向盛有Cl2的三个集气瓶甲、乙、丙中各注入下列液体中的一种,经过振荡,现象如下图所示,则甲、乙、丙中注入的液体分别是
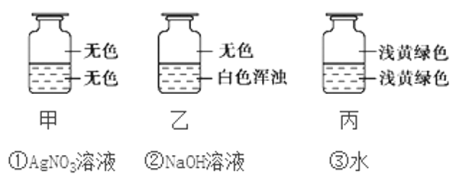
A. ②①③ B. ①②③
C. ③②① D. ①③②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】波义耳在《怀疑的化学家》一书中说:“在火的单独作用下,玻璃容器中的水银会丧失其原有的银色,变成一种红色物质;而无须使用任何附加试剂,用这种红色物质也可以得到汞”。该过程可表示为:![]() 。下列说法错误的是
。下列说法错误的是
A. 波义耳所描述的变化属于氧化还原反应 B. 此反应可粗略测定空气中氧气的含量
C. 波义耳所描述的变化是一个可逆的化学反应 D. 用热分解法可由氧化汞制得单质汞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.(1)键线式![]() 表示的有机物名称为__________。
表示的有机物名称为__________。
(2)A和B两种有机物可以互溶,其有关性质如表所示:
密度(20℃) | 熔点(℃) | 沸点(℃) | 溶解性 | |
A | 0.7137 g/mL | -116.6 | 34.5 | 不溶于水 |
B | 0.7893 g/mL | -117.3 | 78.5 | 与水以任意比混溶 |
要除去B中混有的少量A,可采用_________方法。
A.蒸馏 B.过滤 C.萃取 D.加水充分振荡,分液
Ⅱ.(1)扁桃酸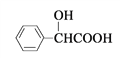 有多种同分异构体,属于甲酸酯且含酚羟基的同分异构体共有_______种。
有多种同分异构体,属于甲酸酯且含酚羟基的同分异构体共有_______种。
(2)分子式为C9H12 且属于苯的同系物的同分异构体的数目为_______
III.有下列各组物质:
(A)S2和S4
(B) ![]() 和
和![]()
(C)CH4和C8H18
(D) 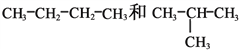
(E)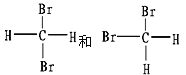
①_________组两物质互为同素异形体;
②_________组两物质互为同系物
IV.配平下列化学方程式,只需将配平后草酸的系数、二氧化氯的系数填入答题页上。
KClO3+______H2C2O4+H2SO4![]() _____ClO2↑+K2SO4+CO2↑+H2O
_____ClO2↑+K2SO4+CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫单质及其化合物在化工生成等领域应用广泛。
(1)工业尾气中的SO2一直是环境污染的主要原因之一,工业上常采用如下方法降低尾气中的含硫量:
①方法1:燃煤中加入生石灰,将SO2转化为CaSO3,再氧化为CaSO4
已知:a. CaO(s)+CO(g) =CaCO3(s) ΔH=-178.3kJ·mol-1
b.2CaCO3(s)+2SO2(g)+O2(g)=2CaSO4(s)+2CO2(g) ΔH=-2762.2kJ·mol-1
c.2CaSO3(s)+O2(g)=2CaSO4(s) ΔH=-2314.8kJ·mol-1
写出CaO(s)与SO2(g)反应生成CaSO3(s)的热化学方程式:_________________________________。
②方法2:用氨水将SO2转化为NH4HSO3,再氧化为( NH4)2SO4。
实验测得NH4HSO3溶液中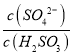 = 1500,则溶液的pH为______________(已知:H2SO3的Ka1=1.5×10-2,Ka2=1.0×10-7)。
= 1500,则溶液的pH为______________(已知:H2SO3的Ka1=1.5×10-2,Ka2=1.0×10-7)。
(2)煤制得的化工原料气中含有羰基硫(0=C=S),该物质可转化为H2S,反应为COS(g) +H2(g)![]() H2S (g)+CO(g) ΔH>0。
H2S (g)+CO(g) ΔH>0。
①恒温恒容条件下,密闭容器中发生上述反应,下列事实不能说明反应达到平衡状态的是__________
(填字母)。
a.COS的浓度保持不变 b.化学平衡常数不再改变
c.混合气体的密度不再改变 d.形成2molH-S键的同时形成1mol H-H键
②T1℃时,在恒容的密闭容器中,将定量的CO和H2S混合加热并达到下列平衡:H2S(g)+ CO(s) ![]() COS(g)+H2(g),K=0 25,则该温度下反应COS(g)+H2(g)=H2S(g)+ CO(s)的平衡常数K=__________。
COS(g)+H2(g),K=0 25,则该温度下反应COS(g)+H2(g)=H2S(g)+ CO(s)的平衡常数K=__________。
T1℃时,向容积为10 L的恒容密闭容器中充入1mol COS(g)和1molH2(g),达到平衡时COS的转化率为______________________。
(3)过二硫酸(H2S2O8)是一种强氧化性酸,其结构式为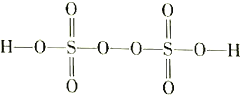 。
。
①在Ag+催化作用下,S2O82-能与Mn2+在水溶液中发生反应生成SO42-和MnO4-,1mol S2O82-能氧化的Mn2+的物质的量为_________mol。
②工业上可用惰性电极电解硫酸和硫酸铵混合溶液制备过二硫酸铵。则阳极的电极反应式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于非氧化还原反应的是
A. 2Na + Cl2 === 2NaCl B. MnO2 + 4HCl(浓) ![]() MnCl2 + Cl2↑ + 2H2O
MnCl2 + Cl2↑ + 2H2O
C. 2KI+Cl2===2KCl+I2 D. MgO+2HCl===MgCl2+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com