
【题目】为分离废磷酸亚铁锂电池的正极材料(主要含LiFePO4和铝箔)中的金属,将正极材料粉碎后进行如下流程所示的转化:

已知LiFePO4不溶于水和碱,能溶于强酸。
(1)“碱溶”时的离子方程式为___。
(2)向滤液Ⅰ中通入过量CO2会析出Al(OH)3沉淀,写出该反应的离子方程式:____。
(3)“酸浸”时溶液中Fe2+发生反应的离子方程式为_____。
(4)检验“沉铁”后所得溶液中是否存在Fe3+的方法是____。
(5)以Fe(OH)3为原料可以制取FeSO4晶体,还需的试剂有____。
(6)“沉锂”时,检验Li+是否沉淀完全的方法是____。
【答案】2Al+2OH-+2H2O![]() 2AlO2-+3H2↑ AlO2-+2H2O+CO2
2AlO2-+3H2↑ AlO2-+2H2O+CO2![]() Al(OH)3↓+HCO3- 2Fe2++2H++H2O2
Al(OH)3↓+HCO3- 2Fe2++2H++H2O2![]() 2Fe3++2H2O 取少量沉铁后所得上层溶液,向其中滴加KSCN溶液,若溶液变红色,则存在Fe3+,若溶液不变红,则不存在Fe3+ 硫酸、铁粉 静置,向上层清液中继续滴加Na2CO3溶液,若无沉淀生成,则Li+沉淀完全
2Fe3++2H2O 取少量沉铁后所得上层溶液,向其中滴加KSCN溶液,若溶液变红色,则存在Fe3+,若溶液不变红,则不存在Fe3+ 硫酸、铁粉 静置,向上层清液中继续滴加Na2CO3溶液,若无沉淀生成,则Li+沉淀完全
【解析】
废磷酸亚铁锂电池的正极材料(主要含LiFePO4和铝箔),加入NaOH溶液,铝箔与NaOH溶液反应生成偏铝酸钠和水,所以滤液Ⅰ为NaAlO2,LiFePO4不溶于水和碱,所以滤渣Ⅰ为LiFePO4,LiFePO4能溶于强酸,加入H2SO4、H2O2,其中的Fe2+被氧化为Fe3+,加入NaOH溶液,生成Fe(OH)3沉淀,再加入Na2CO3溶液,Li+转化为Li2CO3沉淀,据此答题。
(1)“碱溶”时,正极材料粉末中的铝箔与NaOH溶液反应生成偏铝酸钠和水,化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑。
(2)滤液Ⅰ为NaAlO2溶液,通入过量CO2会生成Al(OH)3沉淀,反应的化学方程式为:AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-,故答案为:AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-。
(3)“酸浸”时溶液中的Fe2+在酸性条件下被H2O2氧化为Fe3+,反应的离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O,故答案为:2Fe2++2H++H2O2=2Fe3++2H2O。
(4)检验“沉铁”后所得溶液中是否存在Fe3+的方法是取少量沉铁后所得上层溶液,向其中滴加KSCN溶液,若溶液变红色,则存在Fe3+,若溶液不变红,则不存在Fe3+,故答案为:取少量沉铁后所得上层溶液,向其中滴加KSCN溶液,若溶液变红色,则存在Fe3+,若溶液不变红,则不存在Fe3+。
(5)先将Fe(OH)3与H2SO4反应生成硫酸铁,硫酸铁与铁粉反应生成硫酸亚铁,故答案为:硫酸、铁粉。
(6)“沉锂”时,检验Li+是否沉淀完全的方法是静置,向上层清液中继续滴加Na2CO3溶液,若无沉淀生成,则Li+沉淀完全,故答案为:静置,向上层清液中继续滴加Na2CO3溶液,若无沉淀生成,则Li+沉淀完全。


科目:高中化学 来源: 题型:
【题目】用25%的稀H2SO4溶液与铁块反应制取氢气,下列措施能加快反应速率的是
A. 适当降低温度
B. 将铁块改为铁粉
C. 将所用硫酸改为98.3%浓硫酸
D. 滴加少量氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将0.05 mol Na2CO3固体溶于水配成100 mL溶液,向溶液中加入下列物质,有关结论正确的是( )
加入物质 | 结论 | |
A | 50 mL 1 mol·L-1H2SO4 | 反应结束后,c(Na+)=c(SO |
B | 0.05 mol CaO | 溶液中 |
C | 50 mL H2O | 由水电离出的c(H+)·c(OH-)不变 |
D | 0.1 mol NaHSO4固体 | 反应完全后,溶液pH减小,c(Na+)不变 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米CdSe(硒化镉)可用作光学材料。在一定条件下,由Na2SO3和Se(硒,与S为同族元素)反应生成Na2SeSO3(硒代硫酸钠);再由CdCl2形成的配合物与Na2SeSO3反应制得CdSe纳米颗粒。流程图如下:
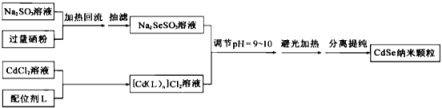
注:①CdCl2能与配位剂L形成配合物[Cd(L)n]Cl2
[Cd(L)n]Cl2=[Cd(L)n]2++2Cl-;[Cd(L)n]2+Cd2++nL
②纳米颗粒通常指平均粒径为1~100nm的粒子
请回答:
(1)下图加热回流装置中,仪器a的名称是______,进水口为_____(填1或2)
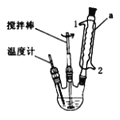
(2)研究表明,CdSe的生成分两步:①SeSO32-在碱性条件下生成HSe-;②HSe-与Cd2+反应生成CdSe。完成第①步反应的离子方程式 SeSO32-+_________=HSe-+__________。写出第②步反应的离子方程式_________________________________________。
(3)CdSe纳米颗粒的大小影响其发光性质。某研究小组在一定配位剂浓度下,探究了避光加热步骤中反应时间和温度对纳米颗粒平均粒径的影响,如图2所示;同时探究了某温度下配位剂浓度对纳米颗粒平均粒径的影响,如图3所示。
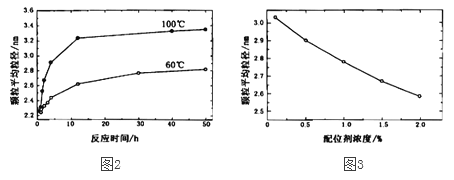
下列说法正确的是__________。
A.改变反应温度和反应时间,可以得到不同发光性质的CdSe纳米颗粒
B.在图2所示的两种温度下,只有60℃反应条件下可得到2.7 nm的CdSe纳米颗粒
C.在其它条件不变时,若要得到较大的CdSe纳米颗粒,可采用降低温度的方法
D.若要在60℃得到3.0 nm的CdSe纳米颗粒,可尝试降低配位剂浓度的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如图所示。C为常见的调味品,D是常见的无色液体。E、F、H和J均为气体,其中H和J为单质,且两者在一定条件下可生成E。
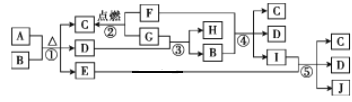
(1)物质的性质决定物质的用途。物质I的溶液可用作家用消毒剂、漂白液,是因为物质I具有__性。
(2)写出反应①的化学方程式:_____。
(3)写出反应③的化学方程式,并用单线桥表示电子转移的方向和数目:___。
(4)写出反应④的离子方程式:____。
(5)写出反应⑤的化学方程式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰[(CN)2]的化学性质与卤素(X2)很相似,化学上称之为拟卤素,其氧化性介于Br2和I2之间,下列有关反应方程式不正确的是
A. (CN)2和NaOH溶液反应:(CN)2+2OH-=CN-+CNO-+H2O
B. MnO2和HCN反应:MnO2+4HCN(浓)![]() Mn(CN)2+(CN)2↑+2H2O
Mn(CN)2+(CN)2↑+2H2O
C. 向KCN溶液中加入碘水:I2+2KCN=2KI+(CN)2
D. 在NaBr和KCN混合溶液中通入少量Cl2:Cl2+2CN-=2Cl-+(CN)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含铁化合物在生活生产中应用广泛。如高铁酸盐(FeO42—)被科学家们公认为绿色消毒剂,在强碱性溶液中比较稳定;聚合硫酸铁则是一种高效絮凝剂。
(1)KClO饱和溶液与Fe(NO3)3饱和溶液反应可制备K2FeO4,两种溶液的混合方式为_______________,反应的离子方程为__________________________________________。
(2)高铁酸盐有极强的氧化性,能迅速有效地去除淤泥中的臭味物质,自身被还原成新生态的Fe(OH)3。已知Ksp[Fe(OH)3]=1.0×10-38。若要使溶液中Fe3+沉淀完全(使其浓度小于10-5 mol·L-1),需调节溶液的pH>________。
(3)聚合硫酸铁[Fex(OH)y(SO4)z]的组成可通过下列实验测定:
①称取一定质量的聚合硫酸铁配成100.00 mL溶液A;
②准确量取20.00 mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65 g;
③准确量取20.00 mL溶液A,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并配成250.00 mL溶液B;
④准确量取25.00 mL溶液B,用0.1000 mol·L-1的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液8.00 mL。
通过计算确定该聚合硫酸铁的化学式(写出计算过程) ______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期元素, 它们的原子序数由A到E依次增大,已知A和B原子有相同的电子层数, 且A的L层电子数是K层电子数的两倍, C在空气中燃烧时呈现黄色火焰, C的单质在高温下与B的单质充分反应, 可以得到与E单质颜色相同的淡黄色固态化合物。D为原子核内有12个中子的二价金属,当2 .4克D与盐酸反应时,在标准状况下放出气体2.24L。
试根据以上叙述回答:
(1)写出元素名称:A_____E____,写出D的原子符号____(标出质子数和质量数)
(2)画出C的原子结构示意图 _________。
(3)写出AB2与C2B2反应的化学方程式___________。
(4)比较B和E的气态氢化物的稳定性(用化学式回答):________ 。
(5)判断C元素和D元素的金属性强弱,简要地说明你的一个判断依据:________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com