
【题目】室温下,将0.1mol·L-1盐酸滴入20mL 0.1 mol·L-1氨水中,溶液pH随加入盐酸体积的变化曲线如图所示。下列有关说法不正确的是( )
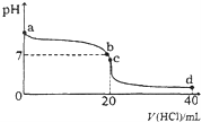
A. a点的pH>7,但Kw仍为1.0×1014
B. b点所示溶液中c(Cl)=c(NH4+)
C. C点溶液pH<7,其原因是NH4++H2O![]() NH3·H2O+H+
NH3·H2O+H+
D. d点所示溶液中离子浓度由大到小的排序是:c(Cl)>c(NH4+)>c(H+)>c(OH)
【答案】D
【解析】A、Kw只受温度的影响,故a点溶液的Kw仍为1.0×10-14,A正确;B、在b点,溶液的pH=7,故有c(H+)>c(OH),根据电荷守恒可知有c(Cl)=c(NH4+),B正确;C、在c点溶液中,加入的盐酸的体积为20mL,能将氨水恰好完全中和,故所得的溶液为NH4Cl溶液,溶液pH<7,其原因是NH4+在溶液中会水解:NH4++H2O![]() NH3·H2O+H+,C正确;D、在d点,加入的盐酸的体积为40mL,盐酸过量,所得的溶液为等浓度的HCl和NH4Cl的混合物,溶液显酸性,且由于NH4+水解,故NH4+的浓度小于H+浓度,正确的顺序为:c(Cl)>c(H+)>c(NH4+)>c(OH),D错误,答案选D。
NH3·H2O+H+,C正确;D、在d点,加入的盐酸的体积为40mL,盐酸过量,所得的溶液为等浓度的HCl和NH4Cl的混合物,溶液显酸性,且由于NH4+水解,故NH4+的浓度小于H+浓度,正确的顺序为:c(Cl)>c(H+)>c(NH4+)>c(OH),D错误,答案选D。


科目:高中化学 来源: 题型:
【题目】本题为《化学反应原理(选修4)》选做题。
(l)T℃时,在1L密闭容器中A气体与B气体反应生成C气体。反应过程中A、B、C的浓度随时间t的变化如图所示。

该反应的化学方程式为____________。在2分钟内用A的浓度变化表示的平均反应速率为___________mol·L一l·min一l。
(2)一定条件下,上述反应达到化学平衡状态的标志是_____(填字母代号)。
A.v(正)=v(逆)=0
B.各物质的浓度不再变化
C.单位时间内消耗1molA,同时生成3molB
(3)若该反应放出热量,升高温度时,化学反应速率______(填“增大”或“减小”),平衡向______(填“正”或“逆”)反应方向移动。
(4)下图是电解NaCl溶液的示意图。请回答下列问题:
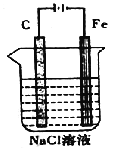
① 石墨电极上的反应式为_____________;
② 电解一段时间后,溶液的pH______(填“增大”“减小”或“不变”)。
(5)水溶液中的离子平衡是化学反应原理的重要内容。请回答下列问题:
① 常温下,0.1mol/LNH4Cl溶液呈______(填“酸”“碱”或“中”)性,溶液中c(NH4+)____c(Cl-)(填“>”“< ”或“=”);
② 已知:20℃时,Ksp(AgCl)=1.1×10-10, Ksp(AgBr)=2.0×10-13。在浓度均为0.01mol/L的NaCl和NaBr混合溶液中,逐滴加入AgNO3溶液,先产生的沉淀是_____(填“AgCl”或“AgBr ”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲使0.1mol/L的NaHCO3溶液中c(H+)、c(CO32-)、c(HCO3-)都减少,( )
A. 通入二氧化碳气体 B. 加入氢氧化钠固体
C. 通入氯化氢气体 D. 加入饱和石灰水溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y是原子核电荷数不大于18的元素。若X、Y两元素化合物组成是YX3,已知X原子的最外层电子数为a+2,次外层电子数为a+3;Y原子的最外层电子数为b-3,次外层电子数为b。则a和b的值分别是
A. 3、2 B. 2、3 C. 5、6 D. 5、8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Ti的基态原子价电子排布式为________________。
②Fe的基态原子共有________种不同能级的电子。
(2)制备CrO2Cl2的反应为K2Cr2O7+3CCl4===2KCl+2CrO2Cl2+3COCl2↑。
①上述化学方程式中非金属元素电负性由大到小的顺序是____________(用元素符号表示)。
②COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为________,中心原子的杂化方式为________。
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中Ni2+和Fe2+的离子半径分别为6.9×10-2 nm和7.8×10-2 nm。则熔点:NiO________(填“>”、“<”或“=”)FeO。
(4)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式_____________________________。

若该晶体的密度是ρg·cm-3,则两个最近的Fe原子间的距离为________________cm。(阿伏加德罗常数用NA表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com