
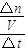 ���㷴Ӧ���ʣ�
���㷴Ӧ���ʣ�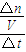 =
= =0.1mol/��L��min������B����
=0.1mol/��L��min������B����


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
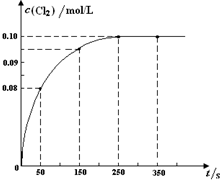 ��2013?��������ģ���¶�ΪTʱ����2L�����ܱ������г���1mol PCl5������PCl5��g��?PCl3��g��+Cl2��g����Ӧ����Ӧ������c��Cl2�� ��ʱ��仯��������ͼ��ʾ������˵������ȷ���ǣ�������
��2013?��������ģ���¶�ΪTʱ����2L�����ܱ������г���1mol PCl5������PCl5��g��?PCl3��g��+Cl2��g����Ӧ����Ӧ������c��Cl2�� ��ʱ��仯��������ͼ��ʾ������˵������ȷ���ǣ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��12�֣�ij�¶�ʱ����2L�ܱ���������̬����CO��H2��Ӧ������̬����Z�����ǵ����ʵ�����ʱ��ı仯���±���ʾ��
| t��min | CO/mol | H2/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.10 |
| 3 | 0.75 | 0.50 | 0.25 |
| 5 | 0.65 | 0.30 | 0.35 |
| 7 | 0.55 | 0.10 | 0.45 |
| 9 | 0.55 | 0.10 | 0.45 |
| 10 | 0.55 | 0.10 | 0.45 |
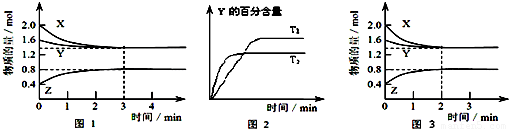
��1���������ϱ������ݣ�����ͼ�л���CO��z�����ʵ�����Ũ�ȣ�c����ʱ�䣨t���仯�����ߣ�
��2����ϵ�з�����Ӧ�Ļ�ѧ����ʽ�� ��
��3����3��5 minʱ���ڲ���Z��ƽ����Ӧ���ʣ� ��
��4��ͼ2��ʾ�÷�Ӧ���й����������ı仯������a��ʾ��ʹ�ô���ʱ��Ӧ�������仯������b��ʾʹ�ô�����������仯���÷�Ӧ�� ������ȡ����ȡ�����Ӧ����Ӧ���Ȼ�ѧ����ʽ�� ��
��5�����������£����д�ʩ����ʹn��CH3OH����n��CO��������� ��ѡ����ţ���
a�������¶� b��ʹ�ô��� C���ٳ���2 mol H2 d���ٳ���2 mol He
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ��㶫ʡ��������ɽ��������ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�������
2012��2��27���������ƽ��롰200��������ʱ����������β���ѳ�Ϊ��Ҫ�Ŀ�����Ⱦ�
��1��������ȼ������ʱ����Ӧ��N2(g)+O2(g) 2NO(g)���ǵ�������β���к���NO��ԭ��֮һ��T��ʱ����2L�ܱ������г���4mol N2��6molO2��5min���ƽ��ʱNO���ʵ���Ϊ4mol���÷�Ӧ������v(N 2)Ϊ ������������µ�ƽ�ⳣ����д��������̣���
2NO(g)���ǵ�������β���к���NO��ԭ��֮һ��T��ʱ����2L�ܱ������г���4mol N2��6molO2��5min���ƽ��ʱNO���ʵ���Ϊ4mol���÷�Ӧ������v(N 2)Ϊ ������������µ�ƽ�ⳣ����д��������̣���
��2�����º��ݣ���˵����Ӧ 2NO(g)  N2(g)+O2(g) �ﵽƽ����� ������ţ���
N2(g)+O2(g) �ﵽƽ����� ������ţ���
A��NO��N2��O2��Ũ��֮��Ϊ2��1��1
B��N2��Ũ�Ȳ��ٷ����仯
C����λʱ��������2 mol NO��ͬʱ����1 mol N2
D�������������ܶȲ��ٷ����仯
��3��H2��CO���Դ���ԭNO�Դﵽ������Ⱦ��Ŀ�ģ�
����֪��N2(g)+ O2(g) = 2NO(g) ��H = +180.5kJ/mol
H2(g)+1/2O2(g) = H2O(l) ��H = ��285.8kJ/mol
��H2(g)��NO(g)��Ӧ����N2(g)��H2O(l)���Ȼ�ѧ����ʽΪ ��
�ڵ�����һ��ʱ�������������ı���������ѧ��Ӧ���ʡ���ͼ�Ƿ�Ӧ��2NO(g) + 2CO(g)  2CO2(g)+ N2(g) ��NO��Ũ�����¶�(T)�����������(S)��ʱ��(t)�ı仯���ߣ��ݴ��жϸ÷�Ӧ�ġ�H
0 (�����������������ȷ����)���������ı����S1��S2
������ͼ�л���NO��Ũ����T1��S2 �����´ﵽƽ������еı仯���ߣ���ע��������
2CO2(g)+ N2(g) ��NO��Ũ�����¶�(T)�����������(S)��ʱ��(t)�ı仯���ߣ��ݴ��жϸ÷�Ӧ�ġ�H
0 (�����������������ȷ����)���������ı����S1��S2
������ͼ�л���NO��Ũ����T1��S2 �����´ﵽƽ������еı仯���ߣ���ע��������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010��ӱ�ʡ��ɽ�и�����ѧ�������Ի�ѧ���� ���ͣ������
��12�֣�ij�¶�ʱ����2L�ܱ���������̬����CO��H2��Ӧ������̬����Z�����ǵ����ʵ�����ʱ��ı仯���±���ʾ��
|
t��min |
CO/mol |
H2/mol |
Z/mol |
|
0 |
1.00 |
1.00 |
0.00 |
|
1 |
0.90 |
0.80 |
0.10 |
|
3 |
0.75 |
0.50 |
0.25 |
|
5 |
0.65 |
0.30 |
0.35 |
|
7 |
0.55 |
0.10 |
0.45 |
|
9 |
0.55 |
0.10 |
0.45 |
|
10 |
0.55 |
0.10 |
0.45 |
��1���������ϱ������ݣ�����ͼ�л���CO��z�����ʵ�����Ũ�ȣ�c����ʱ�䣨t���仯�����ߣ�

��2����ϵ�з�����Ӧ�Ļ�ѧ����ʽ�� ��
��3����3��5 minʱ���ڲ���Z��ƽ����Ӧ���ʣ� ��
��4��ͼ2��ʾ�÷�Ӧ���й����������ı仯������a��ʾ��ʹ�ô���ʱ��Ӧ�������仯������b��ʾʹ�ô�����������仯���÷�Ӧ�� ������ȡ����ȡ�����Ӧ����Ӧ���Ȼ�ѧ����ʽ�� ��
��5�����������£����д�ʩ����ʹn��CH3OH����n��CO��������� ��ѡ����ţ���
a�������¶� b��ʹ�ô��� C���ٳ���2 mol H2 d���ٳ���2 mol He
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�¶�ʱ����2L�ܱ���������̬����CO��H2��Ӧ������̬����Z�����ǵ����ʵ�����ʱ��ı仯���±���ʾ��
| t��min | CO/mol | H2/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.10 |
| 3 | 0.75 | 0.50 | 0.25 |
| 5 | 0.65 | 0.30 | 0.35 |
| 7 | 0.55 | 0.10 | 0.45 |
| 9 | 0.55 | 0.10 | 0.45 |
| 10 | 0.55 | 0.10 | 0.45 |
��1���������ϱ������ݣ�����ͼ�л���CO��z�����ʵ�����Ũ�ȣ�c����ʱ�䣨t���仯�����ߣ�

��2����ϵ�з�����Ӧ�Ļ�ѧ����ʽ�� ��
��3����3��5 minʱ���ڲ���Z��ƽ����Ӧ���ʣ� ��
��4��ͼ2��ʾ�÷�Ӧ���й����������ı仯������a��ʾ��ʹ�ô���ʱ��Ӧ�������仯������b��ʾʹ�ô�����������仯���÷�Ӧ�� ������ȡ����ȡ�����Ӧ����Ӧ���Ȼ�ѧ����ʽ�� ��
��5�����������£����д�ʩ����ʹn��CH3OH����n��CO��������� ��ѡ����ţ���
a�������¶� b��ʹ�ô��� C���ٳ���2 mol H2 d���ٳ���2 mol He
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com