
(10分)现有部分短周期元素的性质或原子结构如下表:
|
元素编号 |
元素性质或原子结构 |
|
X |
X+具有与Ne原子相同的电子层结构 |
|
Y |
最外层电子数是次外层的一半,其最高正价与最低负价的绝对值相等 |
|
Z |
常温下单质为双原子分子,其氢化物水溶液呈碱性 |
|
T |
元素单质的颜色是黄绿色的气体 |
(1) Y在周期表中的位置是 ,Z的原子结构示意图是 。
(2) X元素与T元素形成化合物的电子式是 。
(3) X的最高价氧化物对应水化物的化学式是 ,化学键类型有 。
(4) Y和Z的最高价氧化物对应的水化物中酸性较强的是 (填化学式)
写出可以验证该结论的一个简单易行的实验方案
。
(1)第3周期第ⅣA族(2分), 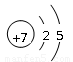 (1分)
(1分)
(2) (1分)
(1分)
(3)NaOH,离子键、极性共价键 (各1分)
(4)HNO3(1分),向Na2SiO3溶液中滴加HNO3溶液,产生白色沉淀。(2分)
【解析】X+具有与Ne原子相同的电子层结构,则X是Na。最高正价与最低负价的绝对值相等,说明属于第ⅣA,又因为最外层电子数是次外层的一半,所以Y是Si。氢化物水溶液呈碱性只有氨气,所以Z是N。单质的颜色是黄绿色的气体的是氯气,则T是Cl。一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间形成共价键。所以氯化钠中含有的是离子键,氢氧化钠中含有离子键和极性键。根据元素周期律可判断,N的非金属性强于Si,所以硝酸的酸性强于硅酸的,可以利用较强的酸来制取较弱的酸来验证。


科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| T | K层和M层上电子数之和等于L层上电数子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| A | 该元素的一种原子,原子核中没有中子 |
| B | 有三个电子层,且K、M层电子数之和等于L层电子数 |
| C | 单质为双原子分子,其氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
| E | 1mol E的单质与足量的稀盐酸反应,可得到氢气33.6L (标准状况) |



查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是次外层电子数的3倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 第三周期元素的简单离子中半径最小 |
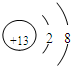
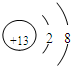
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 元素编号 | 元素性质或原子结构 |
| A | 有三个电子层,K、M层电子数之和等于L层电子数 |
| B | 短周期中金属性最强 |
| C | 常温下单质为双原子分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |






| O2 |
| O2 |
| H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | L层p电子数比s电子数多2个 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |




 Al(OH)3
Al(OH)3 Al3++3OH-
Al3++3OH- Al(OH)3
Al(OH)3 Al3++3OH-
Al3++3OH-查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com