
【题目】25℃时,向某Na2CO3溶液中加入稀盐酸,溶液中含碳微粒的物质的量分数(φ)随溶液pH变化的部分情况如图所示。下列说法中正确的是
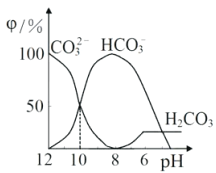
A. pH=7时, c(Na+)=(Cl- )+c(HCO3-)+2c(CO32-)
B. pH=8时,c(Na+)=c(C1-)
C. pH=12时, c(Na+ )>c(OH- )>c(CO32-)>c(HCO3-)>c(H+)
D. 25℃时,CO32-+H2O![]() HCO3-+OH-的水解平衡常数Kh=10-10mol·L-1
HCO3-+OH-的水解平衡常数Kh=10-10mol·L-1
【答案】A
【解析】
A、由电荷守恒可知,c(Na+)+c(H+)=(OH- )+Cl- )+c(HCO3-)+2c(CO32-), pH=7时,c(H+)=(OH- ),则c(Na+)=(Cl- )+c(HCO3-)+2c(CO32-),故A正确;
B、据图可知,pH=8时溶液中溶质为碳酸氢钠和氯化钠,则溶液中c(Cl-)<c(Na+),故B错误;
C、pH=12时,溶液为Na2CO3溶液,碳酸根离子水解生成碳酸氢根离子和氢氧根离子,碳酸氢根离子水解生成碳酸和氢氧根离子, 则c(Na+ )>c(CO32-)>c(OH- )>c(HCO3-)>c(H+),故C错误;
D、CO32-的水解常数Kh=c(HCO3-)c(OH-)/c(CO32-),据图可知,当溶液中c(HCO3-):c(CO32-)=1:1时,溶液的pH=10,c(H+)=10-10mol·L-1,由Kw可知c(OH-)=10-4mol·L-1,则Kh=c(HCO3-)c(OH-)/c(CO32-)=c(OH-)=10-4mol·L-1,故D错误;
故选A。


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸混合溶液100mL,逐渐加入铁粉,产生气体的量随铁粉加入量的变化如图所示.下列说法错误的是( )

A.H2SO4浓度为4mol/L
B.溶液中最终溶质为FeSO4
C.原混合酸中NO3﹣浓度为0.2mol/L
D.AB段反应为:Fe+2Fe3+→3Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石油和煤可以得到有机化工生产中需要的众多原料,例如由石油得到的乙烯和由煤得到的苯可制聚苯乙烯。生产过程如下:
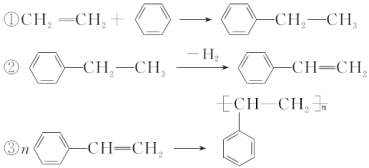
下列说法不正确的是( )
A. 通过裂解可以从石油中获得更多的乙烯
B. 通过煤的干馏不能直接得到纯净的苯
C. 制聚苯乙烯的反应①为加成反应
D. 反应①②③的原子利用率都达到了100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于常温下pH=2的醋酸溶液,下列叙述正确的是( )
A.c(H+)=c(CH3COO-)+c(OH-)
B.加水稀释时![]() 减小
减小
C.与pH=12的NaOH溶液等体积混合后,溶液呈中性
D.加入冰醋酸可增大醋酸的电离度,电离常数Ka变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种钌(Ru)基配合物光敏染料敏化太阳能电池的示意图如下。
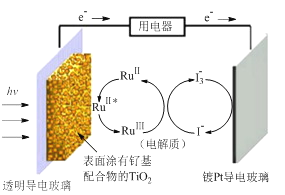
电池工作时发生的反应为:
RuII ![]() RuII *(激发态)
RuII *(激发态)
RuII *→RuIII+e-
I3-+ 2e-→3I-
RuIII+3I-→RuII++ I3-
下列关于该电池叙述错误的是 ( )
A. 电池中镀Pt导电玻璃为正极
B. 电池工作时,I-离子在镀Pt导电玻璃电极上放电
C. 电池工作时,电解质中I-和I3-浓度不会减少
D. 电池工作时,是将太阳能转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2Cl2)是一种重要的化工原料,常用作橡胶硫化剂,改变生橡胶受热发黏、遇冷变硬的性质。查阅资料可知S2Cl2具有下列性质:
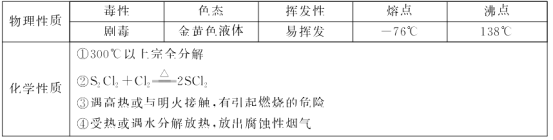
(1)制取少量S2Cl2
实验室可利用硫与少量氯气在110~140℃反应制得S2Cl2粗品,氯气过量则会生成SCl2。
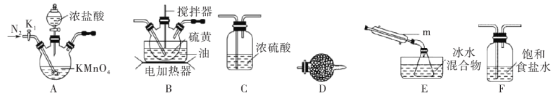
①仪器m的名称为___,装置F中试剂的作用是___。
②装置连接顺序:A→___→___→___→E→D。
③实验前打开K1,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是___。
④为了提高S2Cl2的纯度,实验的关键是控制好温度和___。
(2)少量S2Cl2泄漏时应喷水雾减慢其挥发(或扩散),并产生酸性悬浊液。但不要对泄漏物或泄漏点直接喷水,其原因是___。
(3)S2Cl2遇水会生成SO2、HCl两种气体,某同学设计了如下实验方案来测定该混合气体SO2的体积分数。
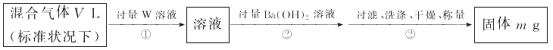
①W溶液可以是___ (填标号)。
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为___(用含V、m的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已省略)。下列说法不正确的是
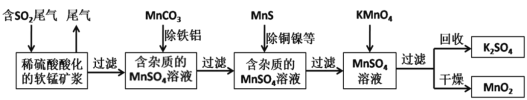
A.上述流程中多次涉及到过滤操作,实验室进行过滤操作时需用到的硅酸盐材质仪器有:玻璃棒、烧杯、漏斗
B.用MnCO3能除去溶液中的Al3+和Fe3+,其原因是MnCO3消耗了溶液中的酸,促进Al3+和Fe3+水解生成氢氧化物沉淀
C.实验室用一定量的NaOH溶液和酚酞试液就可以准确测定燃煤尾气中的SO2含量
D.MnSO4溶液→MnO2过程中,应控制溶液pH不能太小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一体积恒定容器中,反应2A(g)+B(g)![]() 2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、2 mol和4 mol。保持温度和容积不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是( )
2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、2 mol和4 mol。保持温度和容积不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是( )
A.均减半B.均加倍C.均增加1 molD.均减少1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二胺(H2NCH2CH2NH2)是二元弱碱,在水中的电离原理类似于氨。常温下,向乙二胺溶液中滴加稀盐酸,溶液的pH随离子浓度变化关系如图所示。下列叙述不正确的是( )
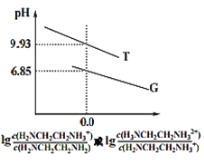
A.Kb2[H2NCH2CH2NH2]的数量级为10-8
B.曲线G代表pH与lg![]() 的变化关系
的变化关系
C.H3NCH2CH2NH2Cl溶液中c(H+)>c(OH-)
D.0.01mol·L-1H2NCH2CH2NH2电离度约为10%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com