
【题目】用惰性电极电解CuSO4溶液。若阳极上产生气体的物质的量为0.010 0 mol,则阴极上析出Cu的质量为 ( )
A.0.64 g
B.1.28 g
C.2.56 g
D.5.12 g
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
A. 与碱反应生成盐和水的物质均属于酸
B. 在离子方程式中盐类均要以离子形式表示
C. 离子反应总是向着溶液中反应物离子浓度减小的方向进行
D. Al2(SO4)3在水溶液中的电离方程式是Al2(SO4)3===Al3++SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废水中常含有一定量的Cr2O ![]() 和CrO
和CrO ![]() ,它们会对人类及生态系统产生很大损害,必须进行处理.常用的处理方法有两种. 方法1:还原沉淀法
,它们会对人类及生态系统产生很大损害,必须进行处理.常用的处理方法有两种. 方法1:还原沉淀法
该法的工艺流程为④③②①
CrO ![]()
![]() Cr2O72﹣
Cr2O72﹣ ![]() Cr3+
Cr3+ ![]() Cr(OH)3↓
Cr(OH)3↓
其中第①步存在平衡:2CrO42(黄色)+2H+Cr2O72﹣(橙色)+H2O
(1)若平衡体系的pH=2,该溶液显色.
(2)能说明第①步反应达平衡状态的是 . a.Cr2O ![]() 和CrO42的浓度相同
和CrO42的浓度相同
b.2v(Cr2O ![]() )=v(CrO42)
)=v(CrO42)
c.溶液的颜色不变
(3)第②步中,还原1 mol Cr2O72﹣离子,需要mol的FeSO47H2O.
(4)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)Cr3+(aq)+3OH﹣(aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)c3(OH﹣)=10﹣32 , 要使c(Cr3+)降至10﹣5 mol/L,溶液的pH应调至 .
方法2:电解法
该法用Fe做电极电解含 Cr2O72﹣的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀.
(5)用Fe做电极的原因为 .
(6)在阴极附近溶液pH升高的原因是(用电极反应解释) , 溶液中同时生成的沉淀还有 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4)是一种易溶于水的二元中强酸,在水中它的存在形态有H2C2O4、HC2O4—、C2O42—,各形态的分布系数(浓度分数)α随溶液pH变化的关系如图所示:
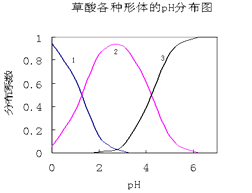
(1)图中曲线1表示________________的分布系数变化。
(2)现有物质的量浓度均为0.1mol/L的下列溶液:
a. Na2C2O4 b. NaHC2O4 c. H2C2O4 d. (NH4)2C2O4 e. NH4HC2O4
已知NaHC2O4溶液显酸性。
①NH4HC2O4显_____性(填“酸”、“碱”或“中”)
②Na2C2O4溶液中,![]() ____2 (填“>”、“=”、“<”), 原因是______________________________________________(用离子方程式表示)。
____2 (填“>”、“=”、“<”), 原因是______________________________________________(用离子方程式表示)。
③常温下,向10 mL 0. 1 mol/L H2C2O4溶液中滴加0.1 mol/L NaOH溶液,随着NaOH溶液体积的增加,当溶液中c(Na+)=2c(C2O42-)+c(HC2O4-)时,溶液显_______性(填“酸”、“碱”或“中”),且V(NaOH)______10 mL(填“>”、“=”或“<”)。
④五种溶液中c(H2C2O4)由大到小排列的顺序是 ________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D为原子序数依次增大的前四周期元素,元素A原子最外层电子数比内层多3个,元素B基态原子核外有2个未成对电子,元素C的最高价和最低价代数和等于0,元素D位于周期表ⅥB族。
(1)判断离子AB2-离子的空间构型为__________。A、B、C 3种元素第一电离能由大到小的顺序为__________________ 。(用相应的元素符号表示)
(2)元素A、C形成的化合物熔点很高,但比B、C形成的化合物熔点低,其原因是_________。
(3)在A的氢化物(A2H4)分子中,A原子轨道的杂化类型是___________。
(4)元素B与D形成的一种化合物广泛应用于录音磁带上,其晶胞如右图所示。该化合物的化学式为___________。

(5)向D的氯化物DCl3溶液中滴加氨水可形成配合物[D(NH3)3(H2O)Cl2]Cl。
①离子D3+的核外电子排布式为_________________。
②1 mol该配合物中含配位键的数目为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是利用二甲苯的一种同分异构体制备新型染料M的合成路线图.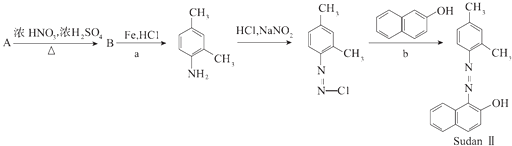
(1)a反应所属反应类型为 , b反应生成另一小分子是 .
(2)写出B的结构简式 .
(3)C与A互为同分异构体,含有两个不相邻的取代基,C的一氯取代产物最多可能有种;D是其中一种,苯环上含有三个取代基,D与酸性高锰酸钾反应得E,E在一定条件下能与乙二醇反应生成高分子化合物F,F是一种优良的高分子材料.写出下列反应的化学方程式:①E与过量热NaOH溶液反应 . ②E→F .
(4)新型染料M在一定条件下可降解生成  和另一种含氮有机分子G,G分子既能与氢氧化钠溶液反应,也能与盐酸反应.G分子中氮元素的质量分数为 .
和另一种含氮有机分子G,G分子既能与氢氧化钠溶液反应,也能与盐酸反应.G分子中氮元素的质量分数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种短周期元素在周期表中的位置关系如图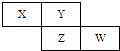
(1)Ⅰ若Z元素原子的最外层电子数是电子层数的2倍①W在周期表中的位置为 .
②Y和Z元素可组成的化合物的化学式为 .
③写出铜和X的最高价氧化物水化物的稀溶液反应的离子方程式为 .
④W最高价氧化物水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有28mol电子转移时,共产生9mol气体,写出该反应的化学方程式 .
(2)Ⅱ若Y和Z的核外电子数之和为22①Y的气态氢化物电子式为 , 工业合成该物质的化学方程式为 .
②将X的最高价氧化物通入到苯酚钠溶液中,实验现象是 .
③X单质与W的最高价氧化物水化物的浓溶液反应,当电子转移0.4mol时,产生气体体积(标准状况下)是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分类是化学学习和研究的常用手段,下列关于物质分类的正确组合是( )
酸 | 碱 | 盐 | 氧化物 | |
A | HNO3 | NaOH | NaCl | H2O |
B | HCl | CaO | Na2CO3 | NH3 |
C | H2SO4 | Ba(OH)2 | CO2 | Na2O2 |
D | H3PO4 | KOH | Al(OH)3 | BaSO4 |
A. AB. BC. CD. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com