
【题目】(1)氯化铁水解的离子方程式为 ,其溶液中离子浓度大小顺序为 。现向氯化铁溶液中加入碳酸钙粉末,发现碳酸钙逐渐溶解,并产生无色气体,其反应的离子方程式为: 。同时有红褐色沉淀生成,其原因是 。
(2)水玻璃在工业上可作粘合剂,它与NH4Cl溶液接触时,会很快凝结,用离子方程式表示其原因为 。
(3)下列各物质的溶液物质的量浓度均为0.1mol/L:①HCl ②NaOH ③Na2CO3 ④CH3COONa ⑤NH4Cl ⑥H2SO4 ⑦KCl ⑧CH3COOH ,它们 pH 由小到大的排列顺序为: 。
(4)常温下,pH=5的盐酸和pH=9的氢氧化钠溶液以体积比11∶9混合,则混合液的pH= 。
【答案】(1)Fe3+ + 3H2O![]() Fe(OH)3 + 3H+ ;c(Cl﹣)>c(Fe3+)>c(H+)>c(OH﹣);
Fe(OH)3 + 3H+ ;c(Cl﹣)>c(Fe3+)>c(H+)>c(OH﹣);
CaCO3 + 2H+ = Ca2+ + H2O +CO2 ↑; 碳酸钙消耗H+,促进氯化铁的水解,使水解产物 Fe(OH)3大量生成,形成红褐色沉淀。
(2)SiO32-+2NH4+ =2NH3 +H2SiO3 ↓
(3)⑥①⑧⑤⑦④③②
(4)6
【解析】
试题分析:(1)氯化铁溶液中Fe3+水解的离子方程式为Fe3++3H2O![]() 3H++Fe(OH)3;向氯化铁溶液中加入碳酸钙粉末,发现碳酸钙逐渐溶解,并产生无色气体,是由于Fe3+水解造成的酸性与碳酸钙反应的结果,即2H++CaCO3=Ca2++CO2↑+H2O;碳酸钙消耗了H+,使Fe3+水解平衡向右不断移动,造成Fe(OH)3不断增加,至出现红褐色沉淀。
3H++Fe(OH)3;向氯化铁溶液中加入碳酸钙粉末,发现碳酸钙逐渐溶解,并产生无色气体,是由于Fe3+水解造成的酸性与碳酸钙反应的结果,即2H++CaCO3=Ca2++CO2↑+H2O;碳酸钙消耗了H+,使Fe3+水解平衡向右不断移动,造成Fe(OH)3不断增加,至出现红褐色沉淀。
(2)氯化铵溶液中铵根离子水解显酸性,水玻璃与其溶液中氢离子结合生成硅酸胶体而凝结,水玻璃与NH4Cl溶液反应生成氯化钠、硅酸、氨气,离子反应为SiO32—+ 2NH4+ = 2NH3+ H2SiO3 ↓;
(3)酸性溶液:①HCl为一元强酸;⑤NH4Cl溶液中,铵根离子水解,溶液显示酸性;⑥H2SO4为二元强酸;⑧CH3COOH为一元弱酸;溶液的pH:⑥<①<⑧<⑤。碱性溶液:②NaOH为一元强碱;③Na2CO3为强碱弱酸盐,溶液显示碱性;④CH3COONa为强碱弱酸盐,溶液显示碱性,由于酸性醋酸大于碳酸,则醋酸根离子的水解程度小于碳酸根离子,则醋酸钠溶液中氢氧根离子浓度小于碳酸钠,溶液的pH:④<③<②。⑦KCl是强酸强碱盐,其溶液呈中性;通过以上分析知,这几种溶液的pH由小到大的排列顺序是:⑥①⑧⑤⑦④③②。
(4)pH=5的盐酸中c(H+)=10-5mol/L,pH=9的氢氧化钠中c(OH-)=![]() mol/L=10-5mol/L,二者以体积比11:9混合,则盐酸过量,溶液呈酸性,混合溶液中c(H+)=
mol/L=10-5mol/L,二者以体积比11:9混合,则盐酸过量,溶液呈酸性,混合溶液中c(H+)=![]() mol/L=10-6mol/L,则溶液的pH=6。
mol/L=10-6mol/L,则溶液的pH=6。


科目:高中化学 来源: 题型:
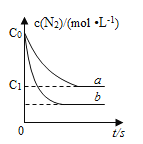
【题目】汽车尾气中,产生NO的反应为:N2(g)+O2(g)![]() 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化。下列叙述正确的是( )
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化。下列叙述正确的是( )
A.温度T下,该反应的平衡常数K=![]()
B.温度T下,随着反应的进行,混合气体的密度减小
C.曲线b对应的条件改变可能是加入了催化剂
D.若曲线b对应的条件改变是温度,可判断该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在陶瓷器皿表面的釉质中含有极微量的Pb、Cd、Sb等有毒金属盐类,为防止中毒,不能长期盛放下列物质的是( )
A. 食盐 B. 酱油
C. 蔗糖 D. 食醋
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密度为0.910 g·cm-3的氨水,质量分数为25.0%,该氨水用等体积的水稀释后,所得溶液的质量分数为
A.等于12.5% B.大于12.5% C.小于12.5% D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温、恒容的密闭容器中进行反应A(g)═B(g)+C(g),若反应物的浓度由2molL﹣1降到0.8molL﹣1需要20s,那么反应物浓度再由0.8molL﹣1降到0.2molL﹣1所需要的时间为( )
A. 10 s B. 大于10 s C. 小于10 s D. 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.SO2、CO2、SiO2中的S、C、Si均为sp3杂化
B.H3O+、NH4+、[Cu(NH3)4]2+均含有配位键
C.SO32—、CO32—、SiO32—均为平面三角形
D.石墨、新型高分子导电材料、聚乙烯、金属晶体均含有金属键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将锌片和铜片用导线连接后放入稀硫酸溶液中,发生原电池反应,下列叙述错误的是( )。
A. 溶液的pH增大 B. 溶液中的Zn2+浓度增大
C. 溶液中的SO![]() 浓度增大 D. 溶液的密度增大
浓度增大 D. 溶液的密度增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com