
【题目】乙酸(CH3COOH)和甲酸甲酯(HCOOCH3)的关系是( )
A.同分异构体
B.同素异形体
C.同位素
D.同一种物质
科目:高中化学 来源: 题型:
【题目】电石中的CaC2与H2O反应可用于制C2H2:CaC2+2H2O→C2H2↑+Ca(OH)2。通过排水测量出反应产生的气体的体积,从而可测定电石中碳化钙的含量。
(1)若使用下列仪器和导管组装实验装置,如下所示:
仪器和 导管 |
|
|
|
仪器和 导管 |
|
|
|
每个橡皮塞都打了两个孔 | |||
如果所制气体从左向右通过时,上述仪器和导管从左到右直接连接的顺序是(填仪器与导管的序号):
________接________接________接________接________接________。
(2)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次):
①称取一定量电石,置于仪器3中,塞紧橡皮塞。
②检查装置的气密性。
③在仪器6和5中注入适量水。
④待仪器3恢复到室温时,量取仪器4中水的体积(导管2中水忽略不计)。
⑤慢慢开启仪器6的活塞,使水逐滴滴下至不产生气体为止,关闭活塞。
正确的操作顺序是(用操作编号填空)________。
(3)若实验产生的气体有难闻的气味,且测定结果偏大,这是因为电石中含有________杂质。
(4)若实验时称取电石为1.60 g,测量出排水的体积后,折算成标准状况下乙炔的体积为448 mL,求此电石中碳化钙的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的NaOH溶液;③加入稍过量的BaCl2溶液;④滴入稀盐酸至无气泡产生;⑤过滤。正确的操作顺序是( )
A. ③②①⑤④ B. ①②③⑤④ C. ②③⑤①④⑤ D. ③⑤②①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种元素的原子电子层结构如下:
A.1s22s22p63s23p63d54s1;B.1s22s22p63s2;C.1s22s22p6;D.1s22s22p63s23p;E.[Ar]4s1。
试回答:
(1)哪个式子是错误的________,它违背了________。
(2)哪个式子表示稀有气体原子________。
(3)A的元素符号是________,写出其价电子排布的轨道表示式________。
(4)B和E的金属性强弱关系为________(用元素符号表示),可以说明这一事实的依据是(写出2点)________________________ _。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各组物质中,不满足图示转化关系的是( ) 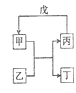
选项 | 甲 | 乙 | 丙 | 戊 |
A | NH3 | O2 | NO | H2O |
B | Fe | H2O | H2 | Fe2O3 |
C | Al(OH)3 | NaOH溶液 | NaAlO2溶液 | 过量CO2 |
D | Na2O2 | CO2 | O2 | Na |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解质溶液在电解质储罐和电池间不断循环.下列说法不正确的是( ) 
A.放电时左侧电解质储罐中的离子总浓度增大
B.充电时电极a连接电源的负极
C.放电时负极的电极反应式为Zn﹣2e﹣═Zn2+
D.阳离子交换膜可阻止Br2与Zn直接发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组通过查阅资料,设计了如下图所示的方法以含镍废催化剂为原料来制备NiSO47H2O.已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%). 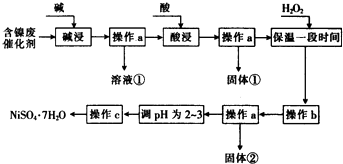
部分阳离子以氢氧化物形式沉淀时的pH如下:
沉淀物 | 开始沉淀时的pH | 完全沉淀时的pH |
Al(OH)3 | 3.8 | 5.2 |
Fe(OH)3 | 2.7 | 3.2 |
Fe(OH)2 | 7.6 | 9.7 |
Ni(OH)2 | 7.1 | 9.2 |
(1)“碱浸”过程中发生反应的离子方程式是
(2)“酸浸”时所加入的酸是(填化学式).
(3)加入H2O2时发生反应的离子方程式为
(4)操作b为调节溶液的pH,你认为pH的调控范围是
(5)产品晶体中有时会混有少量绿矾(FeSO47H2O),其原因可能是(写出一点即可).
(6)NiS047H2O可用于制备镍氢电池(NiMH),镍氢电池目前已经成为混合动力汽车的一种主要电池类型.NiMH中的M表示储氢金属或合金.该电池在充电过程中总反应的化学方程式是Ni(OH)2+M=NiOOH+MH,则NiMH电池放电过程中,正极的电极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某非金属元素R的氢化物及其氧化物、盐之间具有如下转化关系(部分产物省略):氢化物 ![]() B
B ![]() C,下列判断中正确的是( )
C,下列判断中正确的是( )
A.若R是硫元素、则C是Na2SO3
B.若R是硅元素、则C是Na2Si03
C.若R是碳元素、则C是Na2CO3
D.若R是氯元素、则C是NaCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com