
【题目】现实验室需要450 mL 0.5 mol/L的NaOH溶液和500 mL 0.2 mol/L的H2SO4溶液。
请回答下列问题:
Ⅰ.配制NaOH溶液
【1】根据计算,用托盘天平称取NaOH固体的质量应为_____g。
A.0.9B.9.0C.10D.10.0
Ⅱ.配制稀H2SO4
某同学欲用质量分数为98%的浓硫酸(密度ρ=1.84 g/cm3)配制所需的稀H2SO4。可供选用的仪器有:①胶头滴管;②玻璃棒;③烧杯;④量筒;⑤500 mL容量瓶;⑥圆底烧瓶
【2】以上仪器中不需要的是
A.①B.②C.③D.⑥
【3】用量筒量取所需浓硫酸的体积应为_______mL。
A.5.4B.5.5C.18.4D.27.2
【4】如果实验室有10 mL、20 mL、50 mL的量筒,应选用_______mL量筒量取。
A.10B.20C.50D.以上都可以
【5】下列操作会使所配制的溶液浓度偏高的是
A.容量瓶中原来有少量蒸馏水未作处理
B.定容时仰视容量瓶刻度线
C.用量筒量取浓硫酸时仰视读数
D.定容时,不慎加水超过刻度线,又用滴管将多出部分吸出
【答案】
【1】D
【2】D
【3】A
【4】A
【5】C
【解析】
I.1. 根据配制物质的量浓度溶液的要求,选择合适的容量瓶,然后根据n=c·V及m=n·M计算NaOH的质量;
II.2. 用浓硫酸配制稀硫酸,根据配制溶液的步骤确定使用的仪器,进而可确定不需要使用的仪器;
3. 根据稀释前后溶质的物质的量不变,计算需要浓硫酸的体积;
4. 根据选择仪器的标准“大而近”分析;
5.根据c=![]() 分析实验误差。
分析实验误差。
【1】实验室没有规格是450 mL的容量瓶,根据选择仪器的标准“大而近”的原则,应该选择500 mL的容量瓶,则配制500 mL 0.5 mol/L的NaOH溶液,需要NaOH的物质的量为n(NaOH)=c·V=0.5 mol/L×0.5 L=0.25 mol,则需称量的NaOH的质量m(NaOH)= n·M=0.25 mol×40 g/mol=10.0 g,故合理选项是D。
【2】用浓硫酸配制稀硫酸,由于硫酸为液体物质,要使用量筒量取,用一定规格的量筒量取浓硫酸后,沿烧杯内壁缓慢转移至盛有一定量水烧杯中,并用玻璃棒不断搅拌,使热量迅速扩散,当冷却至室温后,通过玻璃棒转移溶液至规格是500 mL的容量瓶中,再洗涤烧杯内壁和玻璃棒2-3次,洗涤液也转移至容量瓶中,加水定容,当液面至离刻度线1-2 cm时,改用胶头滴管滴加至凹液面最低处与刻度线相切,然后盖上瓶塞,上下颠倒,反复摇匀,就得到500 mL 0.2 mol/L的H2SO4溶液,因此在给出的仪器中不需要的是⑥圆底烧瓶,故合理选项是D。
【3】质量分数为98%、密度ρ=1.84 g/cm3的浓硫酸的物质的量浓度c=![]() mol/L=18.4 mol/L,要500 mL 0.2 mol/L的H2SO4溶液,需要溶质的物质的量n(H2SO4)= c·V=0.2 mol/L×0.5 L=0.1 mol,因此需要浓硫酸的体积V(H2SO4)=
mol/L=18.4 mol/L,要500 mL 0.2 mol/L的H2SO4溶液,需要溶质的物质的量n(H2SO4)= c·V=0.2 mol/L×0.5 L=0.1 mol,因此需要浓硫酸的体积V(H2SO4)=![]() =0.0054 L=5.4 mL,故合理选项是A。
=0.0054 L=5.4 mL,故合理选项是A。
【4】需要量取5.4 mL浓硫酸,由于仪器的规格越接近量取液体的体积数值,量取的溶液体积误差越小,所以要选择使用10 mL的量筒来量取浓硫酸,故合理选项是A。
【5】A. 容量瓶中原来有少量蒸馏水未作处理,由于不影响溶质的物质的量及溶液的体积,因此对配制溶液的浓度不产生任何影响,A不符合题意;
B. 定容时仰视容量瓶刻度线,则溶液的体积偏大,根据c=![]() 可知,会使溶液的浓度偏低,B不符合题意;
可知,会使溶液的浓度偏低,B不符合题意;
C. 用量筒量取浓硫酸时仰视读数,则溶质的物质的量偏多,根据c=![]() 可知,会使溶液的浓度偏高,C符合题意;
可知,会使溶液的浓度偏高,C符合题意;
D. 定容时,不慎加水超过刻度线,又用滴管将多出部分吸出,由于溶液的体积偏大,导致配制的溶液浓度偏低,D不符合题意;
故合理选项是C。
本题考查了物质的量浓度的溶液的配制的知识。固体溶质用天平称量,液体溶质用量筒量取,要结合配制溶液的体积先确定是否有一样体积的容量瓶,然后根据“大而近”的原则选择仪器,结合配制溶液的步骤确定使用的仪器,物质质量或体积数值要结合仪器的精确度书写,根据物质的量浓度定义式分析具体操作引起的误差,若操作使溶质物质的量偏大或溶液的体积偏小,则配制的溶液浓度偏高;反之则浓度偏低。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】如图是一种利用锂电池“固定CO2”的电化学装置,在催化剂的作用下,该电化学装置放电时可将CO2转化为C和Li2CO3,充电时选用合适催化剂,仅使Li2CO3发生氧化反应释放出CO2和02。下列说法中正确的是

A. 该电池充电时,阳极反应式为:C+2Li2CO3-4e-=3CO2↑+4Li
B. 该电池放电时,Li+向电极X方向移动
C. 该电池充电时,电极Y与外接直流电源的负极相连
D. 该电池放电时,每转移4mol电子,理论上生成1molC
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对各电解质溶液的分析正确的是( )
A.硫酸铁溶液中能大量共存的离子:K+、Na+、NO3-、CO32-
B.Ca(HCO3)2溶液与过量NaOH溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
C.0.1molL﹣1Na2S溶液中存在:c(OH-)=c(H+)+c(HS﹣)+2c(H2S)
D.NH4HSO4溶液呈酸性的主要原因是:NH4++H2O![]() NH3H2O+H+
NH3H2O+H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将4molA(g)和2molB(g)充入2L恒容密闭容器中,发生2A(g)+B(g) ![]() 2C(g),一段时间达到平衡,反应过程中测定的数据如下表。下列说法正确的是
2C(g),一段时间达到平衡,反应过程中测定的数据如下表。下列说法正确的是
t/min | 2 | 4 | 8 | 9 |
n(B)/mol | 1.5 | 1.2 | 1.0 | 1.0 |
A.该温度下反应的平衡常数K=1.0
B.反应0~4 min的平均速率υ(C)=0.4 molL﹣1min﹣1
C.其他条件不变,升高温度反应的平衡常数增大,则该反应为吸热反应
D.其他条件不变,再充入4molA(g),达到新平衡时A的浓度减小,B的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.将FeCl3溶液和Fe2(SO4)3溶液分别加热、蒸干、灼烧,所得固体成分相同
B.水解反应NH4++H2O![]() NH3H2O+H+达到平衡后,升高温度平衡逆向移动
NH3H2O+H+达到平衡后,升高温度平衡逆向移动
C.CH3COONa溶液中加入CH3COOH能促进CH3COO-水解
D.常温下,浓度均为0.1molL-1 NaCN和HCN混合液的pH=9,则c(HCN)>c(Na+)>c(CN﹣)>c(OH﹣)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的化工原料,在生产生活中有广泛的应用。
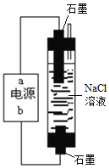
(1)一种环保型家用“84”消毒液的发生装置如右图,电源的b极为________极,电解制取NaClO的离子反应方程式为_______。
(2)用CO和Cl2在高温、活性炭催化作用下合成光气:Cl2(g)+CO(g) ![]() COCl2(g) H=-108 kJ·mol-1。t℃时,在5 L恒容密闭容器中加入0.6 mol CO和0.45 mol Cl2,CO和COCl2的浓度在不同时刻的变化状况如图所示。
COCl2(g) H=-108 kJ·mol-1。t℃时,在5 L恒容密闭容器中加入0.6 mol CO和0.45 mol Cl2,CO和COCl2的浓度在不同时刻的变化状况如图所示。
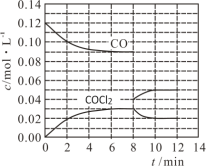
在0~6 min内υ(Cl2)=____________________,第8 min时改变的条件是________________。在第12 min时升高温度,重新达到平衡时,COCl2的体积分数将________(填“增大”“不变”或“减小”)。
(3)氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强。25℃时氯气——氯水体系中存在以下平衡关系:
![]() Cl2(g)
Cl2(g) ![]()
![]() Cl2(aq) K1=10-0.6
Cl2(aq) K1=10-0.6
Cl2(aq) + H2O![]() HClO + H+ +Cl- K2=10-3.4
HClO + H+ +Cl- K2=10-3.4
HClO ![]() H+ + ClO- Ka
H+ + ClO- Ka
其中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。
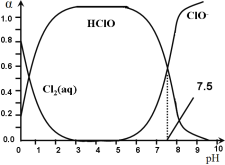
则①Ka = __________;
②Cl2(g) + H2O ![]() HClO + H+ +Cl- K = __________;
HClO + H+ +Cl- K = __________;
③用氯处理饮用水时,pH=6.5时杀菌效果比pH=7.5时___(填“好”、“差”或“相同”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.4g NaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是( )
A.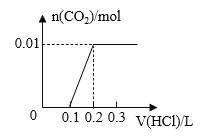 B.
B.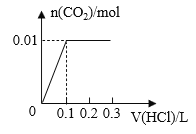
C.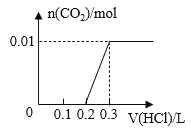 D.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如图所示的实验装置,通过测量反应产生的CO2和H2O的质量,来确定该混合物中各组分的质量分数。

(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是__________。
②称取样品,并将其放入硬质玻璃管中,称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是________。
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为________、________。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是_______________。
②E处干燥管中盛放的药品是碱石灰,其作用是_____________,如果实验中没有该装置,则会导致测量结果NaHCO3的质量_____________(填“偏大”“偏小”或“无影响”)。
③若样品质量为w g,反应后C、D装置增加的质量分别为m1g、m2g,则混合物中Na2CO3·10H2O的质量分数为________(用含w、m1、m2的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据实验事实得出的结论正确的是
实验事实 | 结论 | |
A | 某物质在熔融态下能导电 | 该物质一定是电解质 |
B | 某溶液中加入BaCl2溶液有白色沉淀生成 | 该溶液中一定含有SO42- |
C | SO2的水溶液能导电 | SO2为电解质 |
D | 已知:Cl2+2FeCl2=2FeCl3反应能发生 | 氧化性:Cl2>FeCl3 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com