
将0.5L 1mol/L FeCl3溶液加水稀释至1L ,所得溶液中氯离子的物质的量浓度是
A.3mol/L B.2mol/L C.1.5mol/L D.1mol/L
 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源:2015-2016学年河北省高二上学期第一次月考化学试卷(解析版) 题型:选择题
关于下图所示的原电池,下列说法正确的是
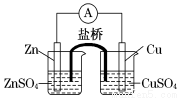
A.电子沿着盐桥从锌电极流向铜电极
B.盐桥中的阳离子向硫酸铜溶液中迁移
C.电流从锌电极通过电流计流向铜电极
D.铜电极上发生的电极反应是2H++2e-===H2↑
查看答案和解析>>
科目:高中化学 来源:2016届湖南省衡阳市高三上学期第一次月考化学试卷(解析版) 题型:选择题
二氯化二硫(S2C12)是广泛用于橡胶工业的硫化剂,其分子结构如图所示。常温下,S2C12是一种橙黄色液体,遇水易水解,并产生能使品红褪色的气体,化学方程式为: 2S2C12+2H2O=SO2↑+3S↓+4HCl。下列说法中错误的是
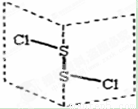
A.S2C12的结构式为Cl—S—S—Cl
B.反应中SO2是还原产物,S是氧化产物
C.S2C12为含有极性键和非极性键的分子
D.反应中,生成1molSO2,转移电子为3mol
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省双鸭山市高三上第一次月考化学试卷(解析版) 题型:选择题
下列有关说法中,不正确的是
A.焰火的五彩缤纷是某些金属元素的性质的展现
B.SiO2可用于制造光导纤维,其性质稳定,不溶于强酸、强碱
C.“光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关
D.根据分散质微粒直径大小可以将分散系分为溶液、胶体和浊液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一入学摸底化学试卷(解析版) 题型:计算题
(6分)将5.1g镁铝合金投入过量盐酸中充分反应,得到500mL溶液和5.6L标准状况下的H2。计算:
(1)合金中镁和铝的质量之比;
(2)所得溶液中Mg2+的物质的量浓度。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一9月检测化学试卷(解析版) 题型:填空题
氧化还原滴定与酸碱中和滴定一样是化学实验室常用的定量测定方法。某氧化还原滴定的反应体系中有反应物和生成物共六种,MnSO4、KMnO4、K2SO4、H2SO3、H2SO4、H2O,其中H2SO3的还原性最强,KMnO4 的氧化性最强。对此反应体系:
(1)被氧化的元素是_______;发生还原反应的过程是________→______。
(2)请用这六种物质组织一个合理的化学反应,写出它的离子方程式:_______
(3)反应中H2 SO4 是_______ (填编号)
A,氧化剂 B.氧化产物 C.生成物 D.反应物
(4)当有20mL 0.1mol/L的氧化剂参加反应时,电子转移数目是_______ 。
(5)用标准KMnO4 溶液滴定H 2 SO3 时,滴定终点时颜色变化是_______。
(6)滴定过程中.下列图像所表示的关系正确的是_______(填编号)。 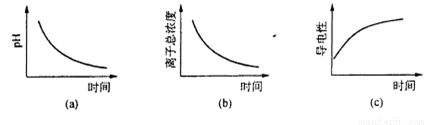
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二9月检测化学试卷(解析版) 题型:选择题
为了科学饮食,了解一些与食品相关的化学知识是必要的。
(1)油炸虾条、薯片等容易挤碎的食品,不宜选用真空袋装,而应采用充气袋装。下列气体中不应该充入的是________。
A.氮气 B.二氧化碳 C.空气 D.氧气
(2)为使以面粉为原料的面包松软可口,通常用碳酸氢钠作发泡剂,因为它________。
①热稳定性差 ②增加甜味 ③产生二氧化碳 ④提供钠离子
A.②③ B.①③ C.①④ D.③④
(3)能直接鉴别氯化钠和葡萄糖两种未知浓度溶液的方法是________。
A.观察颜色 B.测量比重 C.加热灼烧 D.分别闻味
(4)苯甲酸钠是常用的食品防腐剂,其结构简式如图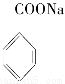 。以下对苯甲酸钠描述错误的是________。
。以下对苯甲酸钠描述错误的是________。
A.属于盐类 B.能溶于水 C.属于烃类 D.不易分解
查看答案和解析>>
科目:高中化学 来源:2016届云南省高三第一次月考试卷化学试卷(解析版) 题型:填空题
(10分)N2O5是一种新型硝化剂,其性质和制备受到人们的关注。
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是 。
(2)一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g) 4NO2(g)+O2(g);ΔH>0
4NO2(g)+O2(g);ΔH>0
①反应达到平衡后,若再通入一定量氮气,则N2O5的转化率将 (填“增大”、“减小”、“不变”)。
②下表为反应在T1温度下的部分实验数据:
t/s | 0 | 500 | 1000 |
c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.48 |
则500 s内N2O5的分解速率为 。
③在T2温度下,反应1000 s时测得NO2的浓度为4.98 mol·L-1,则T2 T1(填>、<或=)。
(3)现以H2、O2、熔融Na2CO3组成的燃料电池采用电解法制备N2O5,装置如图所示,其中Y为CO2。

写出石墨Ⅰ电极上发生反应的电极反应式 ,
N2O5在电解池的 区生成(填“阳极”或“阴极”)。
查看答案和解析>>
科目:高中化学 来源:2016届广东省等六校高三第一次联考化学试卷(解析版) 题型:选择题
已知下列反应: 反应Ⅰ:Co2O3 + 6HCl(浓) 2CoCl2 + Cl2↑+ 3H2O
2CoCl2 + Cl2↑+ 3H2O
反应Ⅱ:5Cl2 + I2 + 6H2O 10HCl + 2HIO3 下列说法正确的是
10HCl + 2HIO3 下列说法正确的是
A.反应Ⅰ中HCl是氧化剂 B.反应Ⅱ中Cl2发生氧化反应
C.还原性:CoCl2 > HCl > I2 D.氧化性:Co2O3 > Cl2 >HIO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com