
【题目】粉煤灰是燃煤电厂的废渣,主要成分为SiO2、Al2O3、Fe2O3和C等。实验室模拟工业从粉煤灰提取活性Al2O3,其流程如下图:

已知烧结过程的产物主要是:NaAlO2、Ca2SiO4、NaFeO2和Na2SiO3等。
(1)写出烧结过程中铝元素转化的化学方程式 。
(2)操作a为冷却、研磨,其中研磨的目的是 。
(3)浸出过程中,NaFeO2可完全水解,水解反应的离子方程式为 。
(4)操作b的名称是 ,所用的玻璃仪器有 、 和烧杯。
(5)“碳化”时生成沉淀,沉淀的化学式为 。
【答案】(1)Al2O3+Na2CO3![]() 2NaAlO2+CO2↑
2NaAlO2+CO2↑
(2)提高烧结产物浸出率
(3)FeO2-+2H2O=Fe(OH)3↓+OH-
(4)过滤 漏斗、玻璃棒
(5)Al(OH)3
【解析】
试题分析:(1)根据题给工艺流程和信息知,烧结过程中氧化铝和碳酸钠反应生成偏铝酸钠和二氧化碳,化学方程式为Al2O3+Na2CO3![]() 2NaAlO2+CO2↑。
2NaAlO2+CO2↑。
(2)操作a为冷却、研磨,其中研磨的目的是增大反应物的接触面积,提高烧结产物浸出率。
(3)NaFeO2完全水解生成氢氧化铁沉淀和氢氧化钠,水解反应的离子方程式为FeO2-+2H2O=Fe(OH)3↓+OH-。
(4)操作b为分离固液混合物的操作,名称是过滤,所用的玻璃仪器有漏斗、玻璃棒和烧杯。
(5)根据题给流程知,“碳化”过程为偏铝酸钠溶液中通入二氧化碳,生成沉淀的化学式为Al(OH)3。


科目:高中化学 来源: 题型:
【题目】I、请根据如下图所示转化关系回答有关问题。A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有强氧化性。
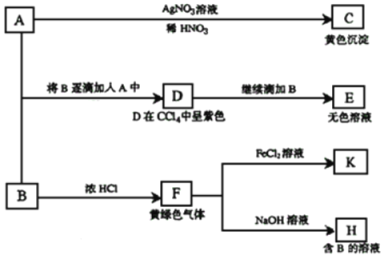
(1)写出A、B的化学式:A ,B 。
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式: , 。
(3)写出将SO2气体通入K溶液中发生反应的离子方程式: 。
II、(1)将0.4gNaOH和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。在如下图所示坐标系中画出能正确表示加入盐酸的体积和生成CO2的物质的量的关系图像。

(2)将18.4gNaOH和NaHCO3固体混合物,在密闭容器中加热到约250℃,经充分反应后排出气体,冷却,称得剩余固体质量为16.6g。试计算混合物中NaOH的质量分数。(请写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、关于工业转化图(见下图):

1、①反应类型: ④反应类型: 。
2、实验室制备乙烯的反应条件是 ;反应温度过低会产生副产物: (写结构简式);
II、现拟分离混有乙醇、乙酸和水的乙酸乙酯粗产品,下图是分离操作步骤的流程图,试填写图中试剂的化学式及分离方法

(1)试剂b是 ;
(2)分离方法①是: ;分离方法②是: ;
(3)A是: ;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是中学化学常见单质, X、Y、Z、M、N、W、H、K是常见化合物,X是B和C的化合产物,它们之间有如下转化关系(反应物和产物中的H2O已略去):
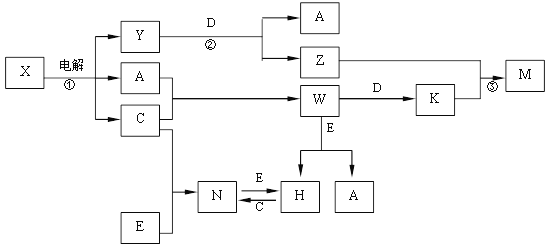
(1)Y的电子式为 ,构成E单质的元素在周期表中位于第 周期第 族
(2)反应①的离子方程式为
反应②的离子方程式为
反应③的离子方程式为
(3)某工厂用C制漂白粉。
①写出制漂白粉的化学方程式
②为测定该工厂制得的漂白粉中有效成分的含量,某小组进行了如下实验:称取漂白粉2.0g,研磨后溶解,配制成250mL溶液,取出25.00mL加入到锥形瓶中,再加入过量的KI溶液和过量的硫酸,此时发生的离子方程式为:
静置。待完全反应后,用0.1mol·L-1的Na2S2O3溶液做标准溶液滴定反应生成的碘,已知反应式为:2Na2S2O3+I2=Na2S4O6+2NaI,共用去Na2S2O3溶液20.00mL。则该漂白粉中有效成分的质量分数为 (保留到小数点后两位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比是化学学习与研究的常用方法。已知:NaH是一种离子化合物,与水反应放出氢气。下列关于铯(Cs)及其化合物的叙述不正确的是( )
A.无水醋酸铯的化学式为CH3COOCs,易溶于水,其水溶液显碱性
B.碳酸氢铯加热即分解生成碳酸铯、二氧化碳和水
C.在Na、K、Rb、Cs中,Cs熔点最高,密度最大
D.CsH是离子化合物,与水反应可以生成H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于糖类、油脂和蛋白质的性质说法正确的是
A.糖类物质中含C、H、O元素,都有甜味
B.油脂是高分子化合物,热值较大
C.在蛋白质溶液中加入CuSO4溶液后有物质析出,加水后该物质溶解
D.葡萄糖能与银氨溶液反应,可用作制镜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.漂白粉、液氯、干冰均为混合物 B.16O和18O互为同位素
C.稀硫酸、氨水均为电解质 D.溶于水能电离出H+的物质一定是酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上生产高氯酸时,还同时生产了一种常见的重要含氯消毒剂和漂白剂亚氯酸钠(NaClO2),其工艺流程如下:
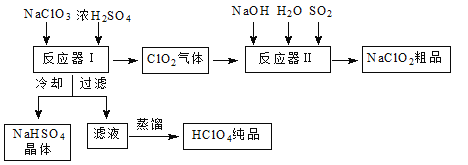
已知:①NaHSO4溶解度随温度的升高而增大,适当条件下可结晶析出。
②高氯酸是至今为止人们已知酸中的最强酸,沸点90 ℃。
请回答下列问题:
(1)反应器Ⅰ中发生反应的化学方程式为 ,冷却的目的是 ,能用蒸馏法分离出高氯酸的原因是___________________。
(2)反应器Ⅱ中发生反应的离子方程式为__________________。
(3)通入反应器Ⅱ中的SO2用H2O2代替同样能生成NaClO2,请简要说明双氧水在反应中能代替SO2的原因是_________________________。
(4)Ca(ClO)2、ClO2、NaClO2等含氯化合物都是常用的消毒剂和漂白剂,是因为它们都具有________________,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com