
科目:高中化学 来源: 题型:阅读理解
 下面是某化学课外活动小组研究浓H2SO4的氧化性的结论并进行了实验验证:
下面是某化学课外活动小组研究浓H2SO4的氧化性的结论并进行了实验验证:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用氨气做喷泉实验主要是利用氨气的水溶液呈碱性这一性质 | B、某溶液中加入氯化钡溶液和稀硝酸,生成白色沉淀,说明溶液中一定含有SO42- | C、浓HNO3与浓H2SO4在空气中长期露置,溶液质量均减轻 | D、配制一定物质的量浓度溶液,定容时俯视刻度线会导致所配溶液浓度偏大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
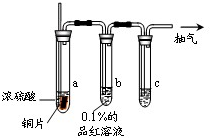 某实验小组同学为了探究铜与浓硫酸的反应,对教材中的装置进行简单改进,在大试管a中加了一根长玻璃导管(见图,图中夹持仪器和加热仪器没有画出).根据题意完成下列填空:
某实验小组同学为了探究铜与浓硫酸的反应,对教材中的装置进行简单改进,在大试管a中加了一根长玻璃导管(见图,图中夹持仪器和加热仪器没有画出).根据题意完成下列填空:| △ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com