
【题目】用如图所示的装置及NaOH溶液、铁屑、稀H2SO4等试剂可以制得白色的Fe(OH)2沉淀。

(1)在试管Ⅰ里加入的试剂是____________________。
(2)在试管Ⅱ里加入的试剂是____________。
(3)为了制得白色Fe(OH)2沉淀,正确的操作顺序是______ (填下列序号)
①打开止水夹 ②检验试管Ⅱ出口处排出的H2的纯度 ③夹紧止水夹 ④在试管Ⅰ和Ⅱ中加入试剂,塞紧塞子
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是:_________________________________________________
【答案】 稀 H2SO4 铁屑 NaOH溶液 ④①②③ 试管Ⅰ中反应生成的H2充满了试管Ⅰ和试管Ⅱ,且外界空气不容易进入。
【解析】根据如图所示的装置及所提供的NaOH溶液、铁屑、稀H2SO4等试剂制得白色的Fe(OH)2沉淀,可以推断该实验的原理是:先在左边的试管中加入铁屑和稀硫酸反应制备硫酸亚铁溶液和氢气,打开止水夹,生成的氢气将盛有氢氧化钠溶液的右边的试管中的空气排出,检验右管排出的气体为纯净的氢气后,关闭止水夹,左管生成的氢气将适量硫酸亚铁溶液排入右管与氢氧化钠溶液反应生成氢氧化亚铁,再关闭止水夹,生成的氢氧化亚铁在氢气的保护下可以防止被氧气氧化,在较长的时间内能观察到白色。
(1)在试管Ⅰ里加入的试剂是稀 H2SO4 、铁屑。
(2)在试管Ⅱ里加入的试剂是NaOH溶液。
(3)为了制得白色Fe(OH)2沉淀,正确的操作顺序是:在试管Ⅰ和Ⅱ中加入试剂,塞紧塞子;打开止水夹;检验试管Ⅱ出口处排出的H2的纯度;。所以填④①②③。
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是:试管Ⅰ中反应生成的H2充满了试管Ⅰ和试管Ⅱ,且外界空气不容易进入。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】鉴别甲烷和氢气两种无色气体的正确方法是
A. 通入溴水 B. 点燃后罩上干燥的冷烧杯
C. 通入澄清石灰水 D. 点燃后罩上内壁涂有澄清石灰水的烧杯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A1.44g完全燃烧生成2.16g H2O,生成的CO2恰好与200mL 1mol/LKOH溶液作用生成正盐,将A试样进行检测所得质谱图如下图。

(1)请写出A的最简式_____________。
(2)请写出A的分子式______________。
(3)若A的一氯代物只有一种,写出A的结构简式并用系统命名法,A的结构简式为_____________系统命名_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴(Co)是重要的稀有金属,在工业和科技领域具有广泛的用途。从某含钴工业废料中回收钴的工艺流程如下:
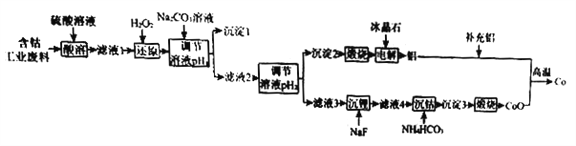
已知:
含钴废料的成分 | |||||
成分 | Al | Li | Co2O3 | Fe2O3 | 其他不溶于强酸的杂质 |
质量分数/% | 10.5 | 0.35 | 65.6 | 9.6 | 13.95 |
Ⅱ.实验中部分离子开始沉淀和沉淀完全的pH | |||
金属离子 | Fe3+ | Co2+ | Al3+ |
开始沉淀的pH | 1.9 | 7.15 | 3.4 |
沉淀完全的pH | 3.2 | 9.15 | 4.7 |
Ⅲ.离子浓度小于等于1.0×10-5 mol·L-1时,认为该离子沉淀完全。
请回答下列问题:
(1)NaF的电子式为____________。
(2)“沉淀1”的化学式为____________________。“调节溶液pH2”的范围为_________________。
(3)“还原”时发生反应的离子方程式为_______________________。
“沉钴”时发生反应的离子方程式为________________________。
(4)制备Co时,“补充铝”的原因为_________________________。
(5)已知:l0-0.9≈0.13,则 A1(OH)3 的溶度积常数 Ksp=_____________________。
(6)Li-SOCl2电池可用于心脏起搏器,该电池的总反应可表示为::4Li+2SOCl2=4LiCl+S+SO2,其正极反应式为_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产生活密切相关。下列说法错误的是
A. 臭氧、醋酸、双氧水都能杀菌消毒
B. 塑料的老化是因为其主要成分在空气中发生了缓慢的加成反应
C. “以火烧之,紫青烟起,乃真硝石(KNO3)",“紫青烟”是因为发生了焰色反应
D. 有人称“一带一路”是“现代丝绸之路”,丝绸的主要成分是蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能够成功的是
A. 只用溴水一种试剂可鉴别甲苯、乙烯、乙醇、四氯化碳四种物质
B. 将乙醇加热到170 ℃可制得乙烯
C. 用乙醇、冰醋酸及pH=0的硫酸加热可制乙酸乙酯
D. 苯与溴水在FeBr3的催化下制取溴苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 室温下,用pH试纸测定浓度为0.1 mol ·L-1 NaClO溶液的pH
B. 将4 mL 0.01mol ·L-1 KSCN溶液与1 mL 0.01 mol ·L-1 FeCl2溶液充分混合;再继续加入KSCN溶液,溶液颜色加深,证明溶液中存在平衡Fe3++ 3SCN-![]() Fe(SCN)3
Fe(SCN)3
C. 测定中和反应的反应热时,将碱的稀溶液缓慢倒入酸的稀溶液中,所测反应后混合液温度值偏小
D. 测定Na 2SO4溶液与Na2CO3溶液的酸碱性,说明非金属性:S>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酯分子式为C6H12O2,该酯水解后生成A和B,B是A的同分异构体的氧化产物,该酯为 ( )
A. CH3CH(CH3)COOC2H5 B. CH3CH2COO(CH2)2CH3
C. CH3COO(CH2)3CH3 D. CH3CH2COOCH(CH3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在恒容密闭容器中发生反应NO2(g)+SO2(g)![]() SO3(g)+NO(g)。下列能说明反应达到平衡状态的是
SO3(g)+NO(g)。下列能说明反应达到平衡状态的是
A. 体系的压强保持不变
B. 混合气体的密度保持不变
C. 混合气体的颜色保持不变
D. 每消耗1molSO3的同时生成1molNO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com