
有关杂化轨道的说法不正确的是
A.杂化前后的轨道数不变,但轨道的形状发生了改变
B.sp3、sp2、sp杂化轨道的夹角分别为109°28′、120°、180°
C.四面体形、三角锥形、V形分子的结构可以用sp3杂化轨道解释
D.杂化轨道全部参加形成化学键
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:
右图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法正确的是( )
A.该试剂的物质的量浓度为9.2 mol·L—1
B.该硫酸50 mL与足量的铜反应可得到标准状况下SO2 10.3 L
C.配制200 mL 4.6 mol·L—1的稀硫酸需取该硫酸50 mL
D.该硫酸与等体积的水混合所得溶液的质量分数小于49%

查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.焓是与内能有关的物理量,当反应在恒压条件下进行时,反应热效应等于焓
B.当能量变化以热的形式表现时,将反应分为放热反应和吸热反应
C.测定中和反应的反应热时,为提高实验准确性,使用稍过量的碱
D.新能源有太阳能、氢能、风能、生物质能等,它们都是可再生的
查看答案和解析>>
科目:高中化学 来源: 题型:
新型高能钠硫电池以熔融的钠、硫为电极,以导电的陶瓷为固体电解质。该电池放电时为原电池,充电时为电解池,反应原理为:2Na+xS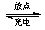 Na2Sx。
Na2Sx。
(1)放电时Na发生_______反应,S作________极。
(2)充电时Na所在电极与直流电源的__________极相连。
(3)放电时负极反应为___________________________________________________;
充电时阳极反应为__________________________________________________。
(4)用此电池作电源电解饱和NaCl溶液,当阳极产生33.6 L(标准状况)气体时,消耗金属Na的质量为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于氢键,下列说法正确的是
A.含氢元素的化合物中一定有氢键
B.因为分子间存在氢键的缘故, 比
比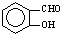 熔沸点高
熔沸点高
C.由于氢键比范德华力强,所以H2O分子比H2S分子稳定
D.“可燃冰”——甲烷水合物(例如:8CH4·46H2O)中CH4与H2O之间存在氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于丙烯( )的说法错误的是
)的说法错误的是
A.丙烯分子有8个σ键,1个π键
B.丙烯分子中3个碳原子都是 杂化
杂化
C.丙烯分子存在非极性键
D.丙烯分子中3个碳原子在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期主族元素X、Y、Z、R、W的原子序数逐渐增大,X原子的p轨道半充满,且X、Y、Z同周期,Y与R的价电子数相同。
(1)在化合物YZ2中中心原子的VSEPR模型为_______________,Y与Na的离子半径由小到大的顺序为______________;
(2)X 的常见氢化物的空间构型是_____________,它的另一氢化物 X2H4 是一种火箭燃料的成分,其电子式是___________________;
(3)R、W两元素电负性较强的是(写元素符号) _______;写出证明这一结论的一个
实验事实(用化学方程式表示) ;
(4)W的含氧酸有多种,写出其中两种的分子式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
金属钙线是炼制优质钢材的脱氧脱磷剂,某钙线的主要成分为金属M和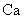 ,并含有3.5%(质量分数)
,并含有3.5%(质量分数)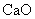 .
.
(1)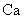 元素在周期表中位置是 ,其原子结构示意图 .
元素在周期表中位置是 ,其原子结构示意图 .
(2)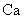 与最活跃的非金属元素A形成化合物D,D的电子式为 ,D的沸点比A与
与最活跃的非金属元素A形成化合物D,D的电子式为 ,D的沸点比A与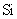 形成的化合物E的沸点 .
形成的化合物E的沸点 .
(3)配平用钙线氧脱鳞的化学方程式:
P+ FeO+ CaO
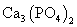 + Fe
+ Fe
(4)将钙线试样溶于稀盐酸后,加入过量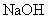 溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色
溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色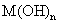 .则金属M为______;检测
.则金属M为______;检测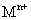 的方法是_____(用离子方程式表达).
的方法是_____(用离子方程式表达).
(5)取1.6g钙线试样,与水充分反映,生成224ml.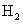 (标准状况),在想溶液中通入适量的
(标准状况),在想溶液中通入适量的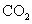 ,最多能得到
,最多能得到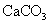 g.
g.

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com